名校
解题方法
1 . 某学习小组在做氢气的制备实验时,用高纯锌粒和稀硫酸为反应物,结果发现反应速率较慢。下列措施不能加快制氢气速率的是
| A.将稀硫酸换成质量分数为98%的浓硫酸 | B.向反应液中加入适量的碳粉 |
| C.改换合适的装置并适当加热 | D.将锌粒换成质量相等的锌粉 |
您最近半年使用:0次
名校
解题方法
2 . 某实验小组为探究外界条件对化学反应速率的影响进行如下实验:
实验1:探究常温下影响等质量金属与酸反应生成氢气速率的因素:
(1)实验I、Ⅱ探究的是___________ 对反应速率的影响。
(2)实验I、Ⅲ及相应实验现象得到的结论是___________ 。
(3)实验1中三组的反应速率由快到慢的顺序可能是___________ (填编号)。
(4)甲同学在进行实验Ⅲ时又加入了少量硫酸铜固体,发现生成气体速率明显加快,试分析其原因:___________ 。
实验2:探究影响反应 的因素。(编号Ⅳ为对照组)
的因素。(编号Ⅳ为对照组)
(5)请写出表中
___________ 。
(6)实验Ⅵ研究“温度对该反应速率的影响”,请填写合理的数据。①:___________ ;②:___________ ;③:___________ 。
(7)该小组同学依据实V条件进行反应并测定其化学反应速率,所得数据如图所示。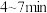 内用
内用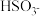 表示的平均反应速率为
表示的平均反应速率为___________  。(写出计算过程)
。(写出计算过程)
实验1:探究常温下影响等质量金属与酸反应生成氢气速率的因素:
| 实验编号 | 金属 | c(酸)/( ) ) | 溶液体积/ |
| I | 铁粉 |  硫酸 硫酸 | 10 |
| Ⅱ | 铁粉 |  盐酸 盐酸 | 10 |
| Ⅲ | 铁块 |  硫酸 硫酸 | 10 |
(1)实验I、Ⅱ探究的是
(2)实验I、Ⅲ及相应实验现象得到的结论是
(3)实验1中三组的反应速率由快到慢的顺序可能是
(4)甲同学在进行实验Ⅲ时又加入了少量硫酸铜固体,发现生成气体速率明显加快,试分析其原因:
实验2:探究影响反应
 的因素。(编号Ⅳ为对照组)
的因素。(编号Ⅳ为对照组)| 实验编号 |  溶液的体积/ 溶液的体积/ | 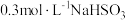 溶液的体积/ 溶液的体积/ | 水的体积/ | 反应温度 |
| Ⅳ | 10 | 10 | 0 |  |
| V | 10 | 5 | a |  |
| Ⅵ | ① | ② | ③ |  |
(5)请写出表中

(6)实验Ⅵ研究“温度对该反应速率的影响”,请填写合理的数据。①:
(7)该小组同学依据实V条件进行反应并测定其化学反应速率,所得数据如图所示。
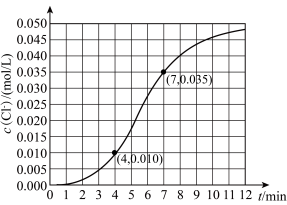
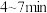 内用
内用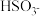 表示的平均反应速率为
表示的平均反应速率为 。(写出计算过程)
。(写出计算过程)
您最近半年使用:0次
名校
解题方法
3 . Ⅰ.断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A—B的键能。下表列出了一些化学键的键能(E):
请回答下列问题:
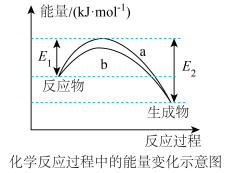
(1)如图表示某反应的能量变化关系,则此反应_______ (填“吸收”或“放出”)_______ kJ能量(用含有a、b的关系式表示)。 O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=_______ 。
(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为_______ 。
Ⅱ.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(4)该实验探究的是_______ 因素对化学反应速率的影响。如下图一,相同时间内针筒中所得的CO2体积大小关系是_______ (填实验序号)。 =
=_______ (假设混合液体积为50mL)。
(6)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定_______ 来比较化学反应速率。
(7)小组同学发现反应速率总是如上图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②_______ 。
| 化学键 | H—H | Cl—Cl | O=O | C—Cl | C—H | O—H | H—Cl |
| E/(kJ·mol-1) | 436 | 247 | x | 330 | 413 | 463 | 431 |
(1)如图表示某反应的能量变化关系,则此反应
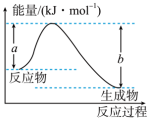
 O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为
Ⅱ.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.1mol·L-1H2C2O4溶液 | 30mL 0.1 mol·L-1KMnO4溶液 |
| ② | 20mL 0.2mol·L-1H2C2O4溶液 | 30mL 0.1mol·L-1KMnO4溶液 |
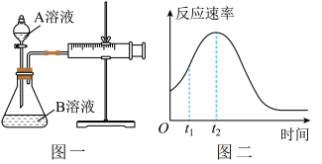
 =
=(6)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定
(7)小组同学发现反应速率总是如上图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②
您最近半年使用:0次
名校
4 . 化学与生产、生活密切相关。下列事实与化学反应速率无关的
| A.用炉灶燃烧含硫蜂窝煤时加入生石灰 |
| B.做糕点时,在面粉中加入酵母菌发酵 |
| C.在糕点包装内放置除氧剂可以延长食品保质期 |
D.燃烧黄铁矿制备 气体时,把矿石粉碎成颗粒状 气体时,把矿石粉碎成颗粒状 |
您最近半年使用:0次
名校
5 . 在生产和生活中,人们关注化学反应进行的快慢和程度,以提高生产效率和调控反应条件。
Ⅰ.合成氨的反应对人类解决粮食问题贡献巨大,反应为 。
。
(1)德国化学家F·Haber利用 和
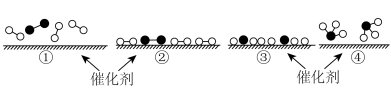
和 在催化剂表面合成氨气而获得诺贝尔奖,该反应的能量变化及微观历程的示意图如下,用
在催化剂表面合成氨气而获得诺贝尔奖,该反应的能量变化及微观历程的示意图如下,用 、
、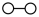 、
、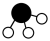 分别
分别 、
、 、
、 。
。_______ 。
A.氢气燃烧 B.氯化铵与 的反应
的反应
C.锌片与稀硫酸的反应 D.钠与冷水的反应
②下列说法正确的是_______ 。
A.使用催化剂,可以加快合成氨的反应速率
B.②→③过程,是吸热过程且只有H-H键断裂
C.③→④过程,N原子和H原子形成了含有极性键的
D.合成氨反应中,反应物断键吸收能量大于生成物成键释放的能量
(2)一定温度下,向恒容的密闭容器中充入一定量的 和
和 发生反应,测得各组分浓度随时间变化如图所示。
发生反应,测得各组分浓度随时间变化如图所示。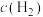 变化的曲线是
变化的曲线是_______ (填“A”“B”或“C”)。
②下列能说明该反应达到平衡状态的是_______ (填序号)。
a.容器中的压强不随时间变化
b.
c.容器中混合气体的密度不随时间变化
d.单位时间内生成3mol 的同时生成2mol
的同时生成2mol
e.容器内 的质量分数不变
的质量分数不变
(3)一定条件下,将2mol 和3mol
和3mol 通入2L的恒容密闭容器中,10min后达到化学平衡,测得
通入2L的恒容密闭容器中,10min后达到化学平衡,测得 的物质的量为2.4mol,则10min内
的物质的量为2.4mol,则10min内 的平均反应速率为
的平均反应速率为_______ , 的转化率是
的转化率是_______ ,混合气中 的物质的量分数是
的物质的量分数是_______ 。
Ⅱ.探究一定条件下反应物浓度对硫代硫酸钠( )与硫酸反应速率的影响。
)与硫酸反应速率的影响。
【查阅资料】
a. 易溶于水,能与硫酸发生反应:
易溶于水,能与硫酸发生反应: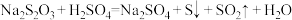
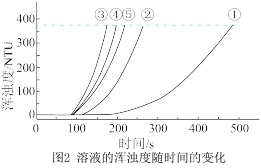
b.浊度计用于测量浑浊度的变化。产生的沉淀越多,浑浊度(单位为NTU)值越大。
【实验过程】
实验数据:
(4)选用浊度计进行测量,原因是 溶液与
溶液与 溶液反应生成了
溶液反应生成了_______ 。
(5)实验③中,x=_______ 。
(6)实验①、②、③的目的是_______ 。
(7)通过比较①、②、③与③、④、⑤两组实验,可推断:反应物浓度的改变对 与硫酸反应的化学反应速率的影响,
与硫酸反应的化学反应速率的影响, 溶液浓度的改变影响更大。该推断的证据是
溶液浓度的改变影响更大。该推断的证据是_______ 。
Ⅰ.合成氨的反应对人类解决粮食问题贡献巨大,反应为
 。
。(1)德国化学家F·Haber利用
 和
和 在催化剂表面合成氨气而获得诺贝尔奖,该反应的能量变化及微观历程的示意图如下,用
在催化剂表面合成氨气而获得诺贝尔奖,该反应的能量变化及微观历程的示意图如下,用 、
、 、
、 分别
分别 、
、 、
、 。
。
A.氢气燃烧 B.氯化铵与
 的反应
的反应C.锌片与稀硫酸的反应 D.钠与冷水的反应
②下列说法正确的是
A.使用催化剂,可以加快合成氨的反应速率
B.②→③过程,是吸热过程且只有H-H键断裂
C.③→④过程,N原子和H原子形成了含有极性键的

D.合成氨反应中,反应物断键吸收能量大于生成物成键释放的能量
(2)一定温度下,向恒容的密闭容器中充入一定量的
 和
和 发生反应,测得各组分浓度随时间变化如图所示。
发生反应,测得各组分浓度随时间变化如图所示。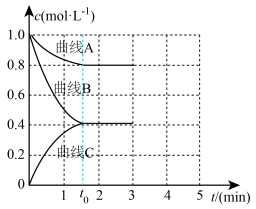
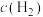 变化的曲线是
变化的曲线是②下列能说明该反应达到平衡状态的是
a.容器中的压强不随时间变化
b.

c.容器中混合气体的密度不随时间变化
d.单位时间内生成3mol
 的同时生成2mol
的同时生成2mol
e.容器内
 的质量分数不变
的质量分数不变(3)一定条件下,将2mol
 和3mol
和3mol 通入2L的恒容密闭容器中,10min后达到化学平衡,测得
通入2L的恒容密闭容器中,10min后达到化学平衡,测得 的物质的量为2.4mol,则10min内
的物质的量为2.4mol,则10min内 的平均反应速率为
的平均反应速率为 的转化率是
的转化率是 的物质的量分数是
的物质的量分数是Ⅱ.探究一定条件下反应物浓度对硫代硫酸钠(
 )与硫酸反应速率的影响。
)与硫酸反应速率的影响。【查阅资料】
a.
 易溶于水,能与硫酸发生反应:
易溶于水,能与硫酸发生反应: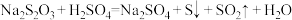
b.浊度计用于测量浑浊度的变化。产生的沉淀越多,浑浊度(单位为NTU)值越大。
【实验过程】
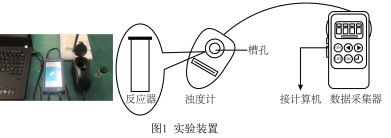
| 实验编号 |  溶液 溶液 |  溶液 溶液 | 蒸馏水 | ||
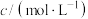 | V/mL | 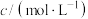 | V/mL | V/mL | |
| ① | 0.1 | 1.5 | 0.1 | 3.5 | 10 |
| ② | 0.1 | 2.5 | 0.1 | 3.5 | 9 |
| ③ | 0.1 | 3.5 | 0.1 | 3.5 | x |
| ④ | 0.1 | 3.5 | 0.1 | 2.5 | 9 |
| ⑤ | 0.1 | 3.5 | 0.1 | 1.5 | 10 |
(4)选用浊度计进行测量,原因是
 溶液与
溶液与 溶液反应生成了
溶液反应生成了(5)实验③中,x=
(6)实验①、②、③的目的是
(7)通过比较①、②、③与③、④、⑤两组实验,可推断:反应物浓度的改变对
 与硫酸反应的化学反应速率的影响,
与硫酸反应的化学反应速率的影响, 溶液浓度的改变影响更大。该推断的证据是
溶液浓度的改变影响更大。该推断的证据是
您最近半年使用:0次
名校
6 . 探究 2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+l0CO2↑+8H2O 反应速率的影响因素,有关实验数据如下表所示:
下列说法不正确的是
| 编号 | 温度℃ | 催化剂(g) | 酸性KMnO4溶液 | H2C2O4溶液 | KMnO4溶液褪色平均时间(min) | ||
| 体积(mL) | 浓度(mol/L) | 体积(mL) | 浓度(mol/L) | ||||
| 1 | 25 | 0.5 | 4 | 0.1 | 8 | 0.2 | 12.7 |
| 2 | 80 | 0.5 | 4 | 0.1 | 8 | 0.2 | a |
| 3 | 25 | 0.5 | 4 | 0.01 | 8 | 0.2 | 6.7 |
| 4 | 25 | 0 | 4 | 0.01 | 8 | 0.2 | b |
| A.a<12.7,b>6.7 |
| B.可通过比较收集相同体积CO2所消耗的时间来判断反应速率快慢 |
| C.用H2C2O4表示该反应速率,v(实验1)约为6.6×l0-3 mol·L-1·min-1 |
| D.用KMnO4表示该反应速率,v(实验3)>v(实验1) |
您最近半年使用:0次
名校
解题方法
7 . 下列说法不正确的是
| A.将纯铁放入稀硫酸中,反应缓慢,再加入少量硫酸铜溶液,可加快产生氢气的速率 |
| B.稀盐酸跟锌片反应,加入少量的氯化钠溶液,反应速率不变 |
C.反应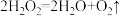 ,加入 ,加入 或升高温度都能加快 或升高温度都能加快 的生成速率 的生成速率 |
D.铁片和稀硫酸反应制取氢气时,改用 的硫酸不可加快产生氢气的速率 的硫酸不可加快产生氢气的速率 |
您最近半年使用:0次
名校
解题方法
8 . I、一定温度时,在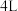 密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示:
密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示:________________ , 时刻M的转化率为
时刻M的转化率为________________ 。
(2)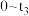 时间内用M表示的化学反应速率为
时间内用M表示的化学反应速率为________  /(
/(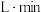 ).
).
(3)下列能表示上述反应达到化学平衡状态的是________(填编号)。
Ⅱ、一定条件下,在容积为 的密闭容器中发生反应:
的密闭容器中发生反应: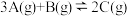 。开始时加入
。开始时加入 、
、 、
、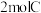 ,在
,在 末测得C的物质的量是
末测得C的物质的量是 。
。
(4)用B的浓度变化表示反应的平均速率:________________ 。
(5)在 末,A的浓度为
末,A的浓度为________________ 。
(6)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”):
①充入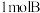 ,化学反应速率
,化学反应速率________________ ;
②将容器的容积变为 ,化学反应速率
,化学反应速率________________ ;
③升高温度,化学反应速率________________ 。
 密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示:
密闭容器中,某反应中的气体M和气体N的物质的量随时间变化的曲线如图所示: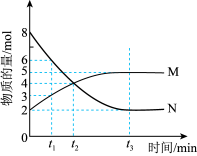
 时刻M的转化率为
时刻M的转化率为(2)
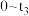 时间内用M表示的化学反应速率为
时间内用M表示的化学反应速率为 /(
/(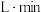 ).
).(3)下列能表示上述反应达到化学平衡状态的是________(填编号)。
A. | B.M与N的物质的量之比保持不变 |
| C.容器中压强保持不变 | D.混合气体密度保持不变 |
Ⅱ、一定条件下,在容积为
 的密闭容器中发生反应:
的密闭容器中发生反应: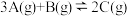 。开始时加入
。开始时加入 、
、 、
、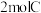 ,在
,在 末测得C的物质的量是
末测得C的物质的量是 。
。(4)用B的浓度变化表示反应的平均速率:
(5)在
 末,A的浓度为
末,A的浓度为(6)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”):
①充入
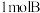 ,化学反应速率
,化学反应速率②将容器的容积变为
 ,化学反应速率
,化学反应速率③升高温度,化学反应速率
您最近半年使用:0次
名校
解题方法
9 . 下列四支试管中,分别盛有等量的锌、酸溶液,其中生成 的反应速率最快的是
的反应速率最快的是
 的反应速率最快的是
的反应速率最快的是试管 | 酸及浓度 | 温度 | 锌的状态 |
① |
|
| 粉末状 |
② |
|
| 粉末状 |
③ |
|
| 粉末状 |
④ |
|
| 大块状 |
| A.① | B.② | C.③ | D.④ |
您最近半年使用:0次
名校
解题方法
10 . 下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是
| A.Cu能与浓硝酸反应,而不与浓盐酸反应 |
| B.Cu与浓硝酸反应比与稀硝酸反应快 |
C. 与 与 在常温、常压下不反应,放电时可反应 在常温、常压下不反应,放电时可反应 |
D.加热时, 与浓盐酸反应,而不与稀盐酸反应 与浓盐酸反应,而不与稀盐酸反应 |
您最近半年使用:0次

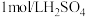 溶液
溶液
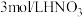 溶液
溶液
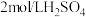 溶液
溶液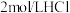 溶液
溶液

