名校
1 . 一定量的锌与过量的稀H2SO4反应制取氢气,一定温度下为减慢反应速率而又不影响生成氢气的量,可向其中加入
| A.醋酸钠固体 | B.铁粉 | C.K2SO4溶液 | D.KNO3溶液 |
您最近半年使用:0次
名校
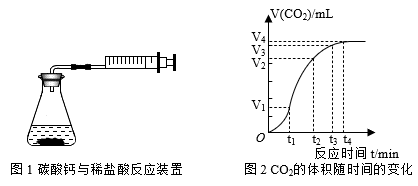
2 . 为了研究碳酸钙粉末与稀盐酸反应的反应速率,某同学利用图1所示装置通过实验测定反应中生成的 的体积随反应时间变化的情况,绘制出图2所示的曲线。已知该反应是放热反应,下列说法正确的是
的体积随反应时间变化的情况,绘制出图2所示的曲线。已知该反应是放热反应,下列说法正确的是
 的体积随反应时间变化的情况,绘制出图2所示的曲线。已知该反应是放热反应,下列说法正确的是
的体积随反应时间变化的情况,绘制出图2所示的曲线。已知该反应是放热反应,下列说法正确的是
A. 段反应速率大于 段反应速率大于 段的主要原因是此阶段盐酸的浓度较大 段的主要原因是此阶段盐酸的浓度较大 |
B. 段反应速率小于 段反应速率小于 段的主要原因是此阶段反应体系的温度降低 段的主要原因是此阶段反应体系的温度降低 |
C. 时刻不再产生气体,表明碳酸钙已经完全消耗 时刻不再产生气体,表明碳酸钙已经完全消耗 |
| D.微热锥形瓶时活塞向右移动,停止加热后活塞恢复至原位置,则装置气密性良好 |
您最近半年使用:0次
2020-12-30更新
|
211次组卷
|
4卷引用:河北省邯郸市2021届高三上学期期末质量检测化学试题
3 . 25℃时,在体积为2L的密闭容器中,气态物质A、B、C的物质的量n(mol)随时间t的变化如下图1所示.已知达平衡后,降低温度,A的转化率将增大。
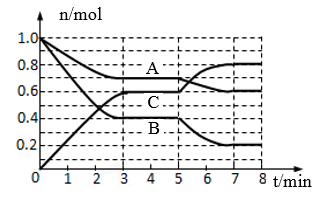
(1)从反应开始到达第一次平衡时的平均速率v(A)为_____ .
(2)根据上图数据,写出该反应的化学方程式_____ ;求出此反应在25℃的平衡常数K=_____ (保留2位小数).
(3)在5~7min内,若K值不变,则此处曲线变化的原因是_____ .
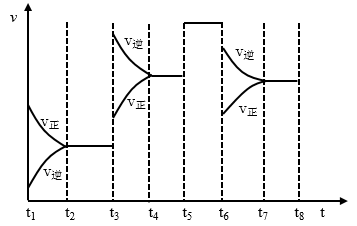
(4)下图表示此反应的反应速率v和时间t的关系图,根据上图判断,在t3和t5时刻改变的外界条件分别是_____ 和_____ ;A的转化率最大的一段时间是_____ 。

(1)从反应开始到达第一次平衡时的平均速率v(A)为
(2)根据上图数据,写出该反应的化学方程式
(3)在5~7min内,若K值不变,则此处曲线变化的原因是
(4)下图表示此反应的反应速率v和时间t的关系图,根据上图判断,在t3和t5时刻改变的外界条件分别是

您最近半年使用:0次
2020-12-29更新
|
168次组卷
|
2卷引用:陕西省宝鸡市渭滨中学2019-2020学年高二上学期期中考试化学试题
解题方法
4 . 某研究小组为了研究不同条件下金属铝粉在过量稀硫酸中的溶解性能,设计如下实验。已知:c(H2SO4)=4.5 mol·L-1,反应均需要搅拌60 min。
(1)实验①和②的目的是_________________________________________
为了获得铝粉溶解量,还需要测量的数据是__________________________________ 。
(2)实验①和③是为了研究硫酸的浓度对该反应的影响,则t1=_______ ℃.
(3)实验③和④是为了研究加入CuSO4溶液对该反应的影响,则 V2=_________ mL.
研究表明,在相同条件下加入少量CuSO4有利于Al的溶解。原因是___________________ 。
(4)纯铝与稀硫酸反应生成氢气的速率—时间图象如图所示:
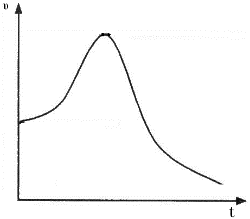
其原因为___________________________
| 编 号 | 温度 /℃ | 加入某盐 | H2SO4 体积/ml | H2O 体积 /ml | 铝粉 加入量/g | 铝粉 溶解量/g |
| ① | 20 | 不加 | 40 | 0 | 2.0050 | 0.0307 |
| ② | 80 | 不加 | 40 | 0 | 2.0050 | 0.1184 |
| ③ | t1 | 不加 | 20 | V1 | 2.0050 | / |
| ④ | t2 | 5ml 0.01 mol·L-1 CuSO4溶液 | 20 | V2 | 2.0050 | / |
为了获得铝粉溶解量,还需要测量的数据是
(2)实验①和③是为了研究硫酸的浓度对该反应的影响,则t1=
(3)实验③和④是为了研究加入CuSO4溶液对该反应的影响,则 V2=
研究表明,在相同条件下加入少量CuSO4有利于Al的溶解。原因是
(4)纯铝与稀硫酸反应生成氢气的速率—时间图象如图所示:

其原因为
您最近半年使用:0次
名校
解题方法
5 . 某实验小组用硫酸酸化的高锰酸钾溶液与草酸溶液反应测定单位时间内生成 的量来探究影响反应速率的因素。设计实验方案如表:
的量来探究影响反应速率的因素。设计实验方案如表:
(1)图1装置中盛放A溶液的仪器名称是___ ,检验该装置气密性的方法为___ 。
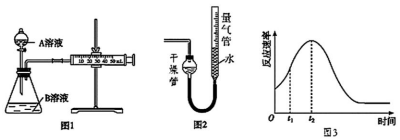
(2)硫酸酸化的高锰酸钾溶液与草酸溶液反应的化学反应方程式为__________ 。
(3)此实验探究的是_____ 因素对化学反应速率的影响,若实验②在40 s末收集了2mol CO2(标准状况下)则在40 s内v( )=
)=_____ (忽略溶液混合前后体积的变化)。
(4)小组同学将上图的气体收集装置改为图2,实验完毕冷却后,读数时发现量气管液面高于干燥管液面,为得到准确数据,采取的操作是:__________ 。
(5)除了通过测定单位时间内生成CO2的体积来比较反应速率,本实验还可以通过测定_____ 来比较化学反应速率。
(6)同学们在实验中发现反应速率总是如图3所示,探究时间内速率变快的主要原因可能是:_____ 。
A.该反应放热 B.生成的Mn2+起催化作用 C.K2SO4浓度增大
 的量来探究影响反应速率的因素。设计实验方案如表:
的量来探究影响反应速率的因素。设计实验方案如表:| 实验序号 | A溶液 | B溶液 |
| ① | 20 mL 0.1 mol/LH2C2O4溶液 | 30 mL0.2 mol/LKMnO4溶液 |
| ② | 20 mL溶液0.2 mol/LH2C2O4溶液 | 30 mL0.2 mol/LKMnO4溶液 |

(2)硫酸酸化的高锰酸钾溶液与草酸溶液反应的化学反应方程式为
(3)此实验探究的是
 )=
)=(4)小组同学将上图的气体收集装置改为图2,实验完毕冷却后,读数时发现量气管液面高于干燥管液面,为得到准确数据,采取的操作是:
(5)除了通过测定单位时间内生成CO2的体积来比较反应速率,本实验还可以通过测定
(6)同学们在实验中发现反应速率总是如图3所示,探究时间内速率变快的主要原因可能是:
A.该反应放热 B.生成的Mn2+起催化作用 C.K2SO4浓度增大
您最近半年使用:0次
2020-12-27更新
|
161次组卷
|
3卷引用:四川省双流中学2019-2020学年高二3月月考化学试题
名校
解题方法
6 . 不同条件下,用O2氧化一定浓度的FeCl2溶液过程中所测的实验数据如图所示。下列分析或推测不合理的是


| A.一定时间内,Fe2+的氧化率随时间延长而逐渐增大 |
| B.由①和②可知,pH越大,Fe2+氧化速率越快 |
| C.由①和③可知,温度越高,Fe2+氧化速率越快 |
| D.氧化过程的离子方程式为:4Fe2++O2+4H+=4Fe3++2H2O |
您最近半年使用:0次
2020-12-24更新
|
221次组卷
|
5卷引用:重庆复旦中学2020-2021学年度高二上学期第二次段考化学试题
重庆复旦中学2020-2021学年度高二上学期第二次段考化学试题(已下线)练习5 影响化学反应速率的因素-2020-2021学年【补习教材·寒假作业】高二化学(人教版)吉林省白山市抚松县第一中学2021-2022学年高二上学期第一次月考化学试题河南省洛阳市2021-2022学年高二上期期中考试化学试题四川省盐亭中学2022-2023学年高二上学期期中教学质量监测(理科)化学试题
名校
解题方法
7 . 某含硫酸的酸性工业废水中含有K2Cr2O7.光照下,草酸(H2C2O4)能将其中的Cr2O 转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在25℃下,控制光照强度、废水样品、初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成了以下实验设计表。
转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在25℃下,控制光照强度、废水样品、初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成了以下实验设计表。
测得实验①和②溶液中的Cr2O 浓度随时间变化关系如图所示。
浓度随时间变化关系如图所示。
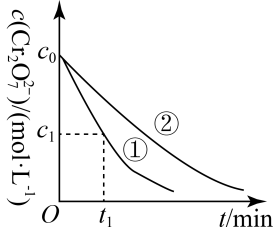
(1)写出草酸与重铬酸钾反应的离子方程式:______
(2)V1=______ ,V2=______ ,V3=______ ;
(3)实验①和②的结果表明_ ;实验①中O~t1时段反应速率v(Cr3+)=______ mol·L-1·min-1(用代数式表示)。
(4)该课题组对铁明矾[Al2Fe(SO4)4·24H2O]中起催化作用的成分提出如下假设。
请你完成假设二和假设三:
假设一:Fe2+起催化作用;
假设二:______ ;
假设三:______ ;
(5)请你设计实验验证上述假设一,完成下表中内容。(除了上述实验提供的试剂外,可供选择的试剂有K2SO4、FeSO4、K2SO4·Al2(SO4)3·24H2O、Al2(SO4)3等。溶液中的Cr2O 浓度可用仪器测定)
浓度可用仪器测定)
 转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在25℃下,控制光照强度、废水样品、初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成了以下实验设计表。
转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在25℃下,控制光照强度、废水样品、初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成了以下实验设计表。| 实验编号 | 初始pH | 废水样品体积/mL | 草酸溶液体积/mL | 蒸馏水体积/mL |
| ① | 4 | 60 | 10 | 30 |
| ② | 5 | 60 | V1 | 30 |
| ③ | 5 | V2 | 20 | V3 |
 浓度随时间变化关系如图所示。
浓度随时间变化关系如图所示。
(1)写出草酸与重铬酸钾反应的离子方程式:
(2)V1=
(3)实验①和②的结果表明
(4)该课题组对铁明矾[Al2Fe(SO4)4·24H2O]中起催化作用的成分提出如下假设。
请你完成假设二和假设三:
假设一:Fe2+起催化作用;
假设二:
假设三:
(5)请你设计实验验证上述假设一,完成下表中内容。(除了上述实验提供的试剂外,可供选择的试剂有K2SO4、FeSO4、K2SO4·Al2(SO4)3·24H2O、Al2(SO4)3等。溶液中的Cr2O
 浓度可用仪器测定)
浓度可用仪器测定)| 实验方案(不要求写具体操作过程) | 预期实验结果和结论 |
反应进行相同时间后,若溶液中c(Cr2O )实验①中的c(Cr2O )实验①中的c(Cr2O ),则假设一成立;若两溶液中的c(Cr2O ),则假设一成立;若两溶液中的c(Cr2O ),则假设一不成立。 ),则假设一不成立。 |
您最近半年使用:0次
8 . 随着经济全球化,我国已于2020年全面脱贫,家用汽车普及,有效处理汽车排放的尾气是需要进行研究的一项重要课题。利用催化技术可将尾气中的NO和CO转化成CO2和N2,为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究:
(1)资料查阅①不同的催化剂对同一反应的催化效率不同;
②使用相同的催化剂,当催化剂质量相等时,催化剂的比表面积对催化效率有影响。
(实验设计)课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验。完成以下实验设计表格
(图象分析与结论)利用气体传感器测定了三组实验中CO浓度随时间变化的曲线图,如图:
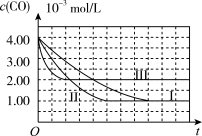
(2)计算第II组实验中,达平衡时NO的浓度为________ ;
(3)由曲线I、II可知,增大催化剂比表面积,汽车尾气转化速率____________________ (填“增大”、“减小”、“无影响”)。
(1)资料查阅①不同的催化剂对同一反应的催化效率不同;
②使用相同的催化剂,当催化剂质量相等时,催化剂的比表面积对催化效率有影响。
(实验设计)课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验。完成以下实验设计表格
| 实验编号 | 实验目的 | T /℃ | NO初始浓度 mol/L | CO初始浓度 mol/L | 同种催化剂的比表面积 m2/g |
| I | 为以下实验作参照 | 280 | 6.50×10-3 | 4.00×10-3 | 80 |
| II | ① | 280 | 6.50×10-3 | 4.00×10-3 | 120 |
| III | 探究温度对尾气转化速率的影响 | 360 | 6.50×10-3 | 4.00×10-3 | ② |

(2)计算第II组实验中,达平衡时NO的浓度为
(3)由曲线I、II可知,增大催化剂比表面积,汽车尾气转化速率
您最近半年使用:0次
解题方法
9 . 下列实验方案不能达到相应实验目的的是
| 实验目的 | 实验方案 | |
| A | 制备CuSO4 | 用稀硫酸、过氧化氢和铜粉反应 |
| B | 加快酸性KMnO4与H2C2O4溶液的反应速率 | 加入一粒黄豆大的MnSO4固体 |
| C | 除去NaCl固体表面的少量KC1杂质 | 用饱和NaCl溶液洗涤 |
| D | 探究浓度对反应速率的影响 | 向盛有同体积、不同浓度NaHSO3溶液的试管中同时加入同体积、同浓度NaClO溶液,观察现象 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
10 . [探究反应速率的影响因素]设计了如下的方案并记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器: 0.20 mol·L-1H2C2O4溶液、0.010 mol·L-1KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽 。
(1)上述实验①、②是探究 ____ 对化学反应速率的影响;若上述实验②、③是探究浓度对化学反应速率的影响,则 a 为_____ ;乙是实验需要测量的物理量,则表格中“乙”应填写_________ 。
[测定H2C2O4·xH2O 中 x 值] 已知:M(H2C2O4)=90 g·mol-1
①称取 1.260 g 纯草酸晶体,将其酸制成 100.00 mL 水溶液为待测液;
②取 25.00 mL 待测液放入锥形瓶中,再加入适的稀H2SO4;
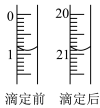
③用浓度为 0.05 00 mol·L-1的 KMnO4标准溶液进行滴定,所用 KMnO4溶液体积如右图。
(2)请写出与滴定有关反应的离子方程式_____________ 。
(3)本实验滴定达到终点的现象是_____ 。
(4)通过上述数据,求得 x=_______ 。以标准KMnO4 溶液滴定样品溶液的浓度,未用标准 KMnO4 溶液润洗滴定管,引起实验结果_________ (偏大、偏小或没有影响)。
| 物理量 | V(H2C2O4)/mL | V(蒸馏水)/mL | V(KMnO4)/mL | T/℃ | 乙 |
| ① | 2.0 | 0 | 4.0 | 50 | |
| ② | 2.0 | 0 | 4.0 | 25 | |
| ③ | 1.0 | a | 4.0 | 25 |
[测定H2C2O4·xH2O 中 x 值] 已知:M(H2C2O4)=90 g·mol-1
①称取 1.260 g 纯草酸晶体,将其酸制成 100.00 mL 水溶液为待测液;
②取 25.00 mL 待测液放入锥形瓶中,再加入适的稀H2SO4;
③用浓度为 0.05 00 mol·L-1的 KMnO4标准溶液进行滴定,所用 KMnO4溶液体积如右图。

(2)请写出与滴定有关反应的离子方程式
(3)本实验滴定达到终点的现象是
(4)通过上述数据,求得 x=
您最近半年使用:0次



