名校
解题方法
1 . 甲烷、水蒸气催化重整是工业制备氢气的方法之一,其反应为 。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用
。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用 表示]的变化关系如图所示。
表示]的变化关系如图所示。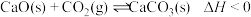 。
。
下列说法错误的是
 。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用
。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用 表示]的变化关系如图所示。
表示]的变化关系如图所示。
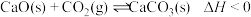 。
。下列说法错误的是
| A.该反应中正反应的活化能大于逆反应的活化能 |
B.向平衡体系中加入适量的 ,可提高氢气的产率 ,可提高氢气的产率 |
C.M点甲烷的平衡转化率为 |
D.在压强为p和600℃时,若向反应器中充入 和 和 ,平衡时氢气的体积分数小于 ,平衡时氢气的体积分数小于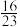 |
您最近半年使用:0次
名校
2 . 科学家研究出一种新的催化剂能有效处理汽车尾气,其反应的化学方程式为: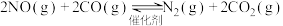
 ,若反应在恒容密闭容器中进行,由该反应相关图象作出的判断正确的是
,若反应在恒容密闭容器中进行,由该反应相关图象作出的判断正确的是
 ,若反应在恒容密闭容器中进行,由该反应相关图象作出的判断正确的是
,若反应在恒容密闭容器中进行,由该反应相关图象作出的判断正确的是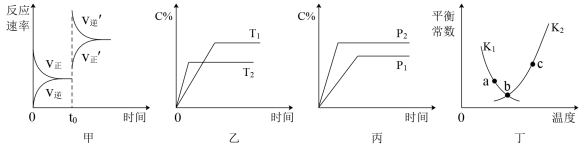
| A.甲图中改变的反应条件为升温 |
B.乙图中温度 ,纵坐标可代表NO的百分含量 ,纵坐标可代表NO的百分含量 |
C.丙图中压强 ,纵坐标可代表NO的体积分数 ,纵坐标可代表NO的体积分数 |
| D.丁图中a、b、c三点只有b点已经达到平衡状态 |
您最近半年使用:0次
名校
解题方法
3 . 稀土被称为新材料的宝库。稀土金属是元素周期表中第3族的钪、钇和15种镧系元素的总称。只需极少量,就能显著改变材料的性能,也被称为“神奇的调料”。
(1)中国化学家________所创立的“串级萃取理论”在稀土工业得到了普遍应用,引导了我国稀土分离科技和产业的全面革新,极大地提升了我国稀土产业的国际竞争力。
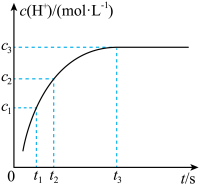
(2)镧系离子可用离子交换法分离,其反应可表示为: 。某温度下,
。某温度下, 随时间变化关系如图所示。下列说法正确的是________。
随时间变化关系如图所示。下列说法正确的是________。
(1)中国化学家________所创立的“串级萃取理论”在稀土工业得到了普遍应用,引导了我国稀土分离科技和产业的全面革新,极大地提升了我国稀土产业的国际竞争力。
| A.吴蕴初 | B.侯德榜 | C.屠呦呦 | D.徐光宪 |
(2)镧系离子可用离子交换法分离,其反应可表示为:
 。某温度下,
。某温度下, 随时间变化关系如图所示。下列说法正确的是________。
随时间变化关系如图所示。下列说法正确的是________。
A. 时的正反应速率大于 时的正反应速率大于 时的逆反应速率 时的逆反应速率 |
B. 时间段的平均反应速率为: 时间段的平均反应速率为: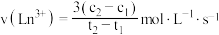 |
C. 时增大 时增大 ,该平衡向左移动,平衡常数减小 ,该平衡向左移动,平衡常数减小 |
D. 时离子交换反应停止 时离子交换反应停止 |
您最近半年使用:0次
名校
解题方法
4 . 对于可逆反应A(g)+2B(g) 2C(g) (正反应吸热),下列图像正确的是
2C(g) (正反应吸热),下列图像正确的是
 2C(g) (正反应吸热),下列图像正确的是
2C(g) (正反应吸热),下列图像正确的是A. | B. | C.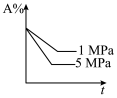 | D.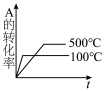 |
您最近半年使用:0次
2024-03-09更新
|
187次组卷
|
2卷引用:山西省吕梁市2023-2024学年高二上学期1月期末化学试题
5 . 某化学科研小组研究在其他条件不变时,改变某一条件对反应[可用 表示]化学平衡的影响,得到如图所示图像(图中
表示]化学平衡的影响,得到如图所示图像(图中 表示压强,
表示压强, 表示温度,
表示温度, 表示物质的量,
表示物质的量, 表示平衡转化率,
表示平衡转化率, 表示平衡体积分数):
表示平衡体积分数):
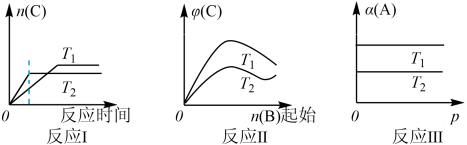
分析图像,回答下列问题:
(1)在反应I中,T1___________ (填“>”“<”或“=”)T2,该正反应为___________ (填“吸热”或“放热”)反应。
(2)在反应Ⅱ中,若此正反应为吸热反应,则T1___________ (填“>”“<”或“=”)T2。
(3)在反应Ⅲ中,a+b___________ c(填“>”“<”或“=”)。
 表示]化学平衡的影响,得到如图所示图像(图中
表示]化学平衡的影响,得到如图所示图像(图中 表示压强,
表示压强, 表示温度,
表示温度, 表示物质的量,
表示物质的量, 表示平衡转化率,
表示平衡转化率, 表示平衡体积分数):
表示平衡体积分数):
分析图像,回答下列问题:
(1)在反应I中,T1
(2)在反应Ⅱ中,若此正反应为吸热反应,则T1
(3)在反应Ⅲ中,a+b
您最近半年使用:0次
名校
6 . 二甲醚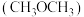 是含氢量高、廉价易得、无毒的优良制氢原料,二甲醚水蒸气重整制氢体系中发生如下反应:
是含氢量高、廉价易得、无毒的优良制氢原料,二甲醚水蒸气重整制氢体系中发生如下反应:
主反应: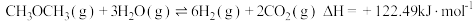
副反应: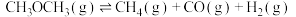
回答下列问题:
(1)上述两反应涉及的六种分子中,是非极性分子的是___________ (写出分子式)。CH4分子中的碳元素位于周期表的___________ 区。
(2)主反应在___________ (填“高温”或“低温”)下能自发进行。根据主反应,从平衡角度考虑能提高H2产率的措施有___________ (任写一种)。
(3)以水煤气作为原料制取H2可以减少副反应带来的损耗并提高H2的产量,如图是CO与水反应的历程图(附着在催化剂表面上的用·标识)。
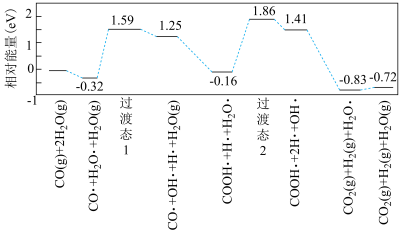
该反应历程决速步的反应方程式为___________ 。总反应的焓变___________ (填“<”或“>”)0。
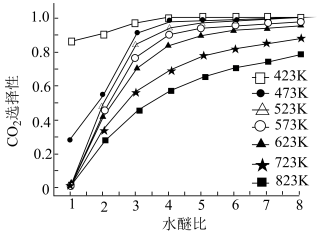
(4)如图是CO2选择性随水醚比变化的曲线,由图可知,工业上一般在___________ 条件下进行二甲醚制氢(考虑水醚比和温度两个角度)。
(5)向恒压为p的体系中充入物质的量之比为1:3的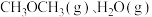 发生二甲醚水蒸气重整制氢反应,达到平衡时,二甲醚转化率为25%,且产物中
发生二甲醚水蒸气重整制氢反应,达到平衡时,二甲醚转化率为25%,且产物中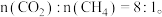
①以下说法不能判断该反应达到平衡状态的是___________ (填字母)。
A.混合气体中各物质分压保持不变 B.混合气体的密度保持不变
C.混合气体平均摩尔质量保持不变 D.消耗 时,有
时,有 生成
生成
②该温度下达到平衡时,H2O的转化率为___________ 。
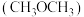 是含氢量高、廉价易得、无毒的优良制氢原料,二甲醚水蒸气重整制氢体系中发生如下反应:
是含氢量高、廉价易得、无毒的优良制氢原料,二甲醚水蒸气重整制氢体系中发生如下反应:主反应:
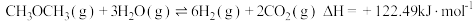
副反应:
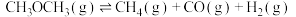
回答下列问题:
(1)上述两反应涉及的六种分子中,是非极性分子的是
(2)主反应在
(3)以水煤气作为原料制取H2可以减少副反应带来的损耗并提高H2的产量,如图是CO与水反应的历程图(附着在催化剂表面上的用·标识)。

该反应历程决速步的反应方程式为
(4)如图是CO2选择性随水醚比变化的曲线,由图可知,工业上一般在

(5)向恒压为p的体系中充入物质的量之比为1:3的
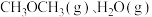 发生二甲醚水蒸气重整制氢反应,达到平衡时,二甲醚转化率为25%,且产物中
发生二甲醚水蒸气重整制氢反应,达到平衡时,二甲醚转化率为25%,且产物中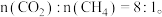
①以下说法不能判断该反应达到平衡状态的是
A.混合气体中各物质分压保持不变 B.混合气体的密度保持不变
C.混合气体平均摩尔质量保持不变 D.消耗
 时,有
时,有 生成
生成②该温度下达到平衡时,H2O的转化率为
您最近半年使用:0次
2024-02-29更新
|
50次组卷
|
2卷引用:河北正定中学本部2023-2024学年高二上学期期末考试化学试题
7 . 体积均为1L的两个恒容密闭容器I、Ⅱ中,均充入2mol CO(g)和2mol NO(g),发生反应: ,相对容器Ⅱ,容器I只改变一个外界条件,测得N2的物质的量与时间关系如图所示。下列叙述正确的是
,相对容器Ⅱ,容器I只改变一个外界条件,测得N2的物质的量与时间关系如图所示。下列叙述正确的是
 ,相对容器Ⅱ,容器I只改变一个外界条件,测得N2的物质的量与时间关系如图所示。下列叙述正确的是
,相对容器Ⅱ,容器I只改变一个外界条件,测得N2的物质的量与时间关系如图所示。下列叙述正确的是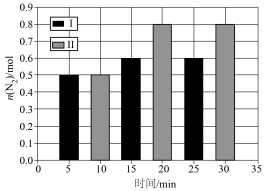
| A.该反应是吸热反应,容器I改变的条件可能是使用了催化剂 |
| B.相对容器Ⅱ,容器I改变的条件可能是升温或者加压 |
| C.容器Ⅱ中NO的平衡转化率为80% |
D.容器Ⅱ中0~10min内,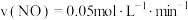 |
您最近半年使用:0次
名校
解题方法
8 . 一定温度下,密闭容器中发生反应:
 ,下列图示与对应的说法相符的是
,下列图示与对应的说法相符的是

 ,下列图示与对应的说法相符的是
,下列图示与对应的说法相符的是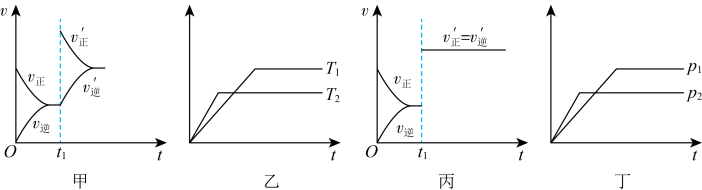
A.图甲中, 时,减小P的浓度 时,减小P的浓度 | B.图乙中,纵坐标表示生成物Q的物质的量 |
C.图丙中, 时,一定使用了催化剂 时,一定使用了催化剂 | D.图丁中,纵坐标表示反应物N的转化率 |
您最近半年使用:0次
名校
解题方法
9 . 近年来甲醇用途日益广泛,越来越引起商家的关注。工业上甲醇的合成途径多种多样。现在实验室中模拟甲醇合成反应,在2L密闭容器内,400℃时发生反应CO(g)+2H2(g) CH3OH(g),体系中n(CO)随时间的变化如表:
CH3OH(g),体系中n(CO)随时间的变化如表:
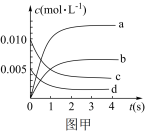
(1)图甲中表示CH3OH的变化的曲线是______ (填字母)。
(2)下列措施不能提高反应速率的有_______ (填字母,下同)。
a.升高温度 b.加入催化剂
c.减小压强 d.及时分离出CH3OH
(3)下列叙述能说明反应达到平衡状态的是_______ 。
a.CO和H2的浓度保持不变
b.v(H2)=2v(CO)
c.CO的物质的量分数保持不变
d.容器内气体密度保持不变
e.每生成1molCH3OH的同时有2molH-H断裂
(4)现有如下两个反应:A.NaOH+HCl=NaCl+H2O,B.Cu+2Ag+=2Ag+Cu2+。
①根据上述两反应的本质,能设计成原电池的是_______ (填字母)。
②将上述反应中能设计成原电池的反应设计成原电池。
I.写出负极的电极反应式________ ,反应类型为________ 。
II.画出装置图并标明电极材料与名称、电解质溶液、电子流向________ 。

 CH3OH(g),体系中n(CO)随时间的变化如表:
CH3OH(g),体系中n(CO)随时间的变化如表:| 时间/s | 0 | 1 | 2 | 3 | 5 |
| n(CO)/mol | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |
(1)图甲中表示CH3OH的变化的曲线是

(2)下列措施不能提高反应速率的有
a.升高温度 b.加入催化剂
c.减小压强 d.及时分离出CH3OH
(3)下列叙述能说明反应达到平衡状态的是
a.CO和H2的浓度保持不变
b.v(H2)=2v(CO)
c.CO的物质的量分数保持不变
d.容器内气体密度保持不变
e.每生成1molCH3OH的同时有2molH-H断裂
(4)现有如下两个反应:A.NaOH+HCl=NaCl+H2O,B.Cu+2Ag+=2Ag+Cu2+。
①根据上述两反应的本质,能设计成原电池的是
②将上述反应中能设计成原电池的反应设计成原电池。
I.写出负极的电极反应式
II.画出装置图并标明电极材料与名称、电解质溶液、电子流向

您最近半年使用:0次
名校
解题方法
10 . 尿素是一种很好用的保湿成分,它存在于肌肤的角质层当中,属于肌肤天然保湿因子NMF的主要成分。工业上以氨气和二氧化碳为原料合成尿素,反应分为如下两步:
反应①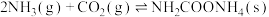
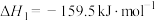
反应②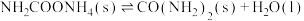

(1)下列反应与反应②的热效应相同的是___________。
(2)下图能表示上述两步反应能量变化的是___________。
(3)恒温恒容时,将2mol 和1mol
和1mol  充入2L反应器中合成尿素,经10min测得反应器内气体压强变为起始的80%(已知此时尿素为固态。水为液态),则从反应开始至10min时,
充入2L反应器中合成尿素,经10min测得反应器内气体压强变为起始的80%(已知此时尿素为固态。水为液态),则从反应开始至10min时, 的平均反应速率
的平均反应速率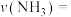
___________ (写出计算过程)。
(4)若将2mol 和1mol
和1mol  充入一容积可变的容器中进行,初始体积固定为V,10min后达到平衡时,
充入一容积可变的容器中进行,初始体积固定为V,10min后达到平衡时, 随时间变化如图所示:
随时间变化如图所示:
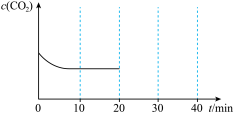
20min时压缩容器,使体积变为0.5V并保持不变,30min时达到新平衡,请在图中大致画出20min~40min内 随时间t变化的曲线
随时间t变化的曲线___________ 。
(5)实际生产中,为节约成本并提高反应②的生产效率,尿素合成工厂通常将反应②的发生场所设置在反应①的发生场所附近,请说明理由:___________ 。
反应①
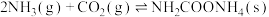
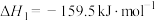
反应②
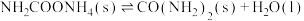

(1)下列反应与反应②的热效应相同的是___________。
| A.木炭与高温水蒸气反应 | B.镁条与稀盐酸反应 |
| C.小苏打与柠檬酸钠反应 | D.氢气与氯气反应 |
(2)下图能表示上述两步反应能量变化的是___________。
A.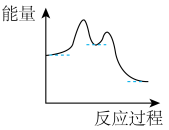 | B.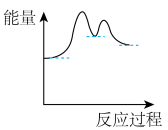 | C. | D.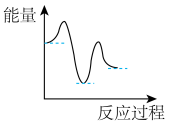 |
(3)恒温恒容时,将2mol
 和1mol
和1mol  充入2L反应器中合成尿素,经10min测得反应器内气体压强变为起始的80%(已知此时尿素为固态。水为液态),则从反应开始至10min时,
充入2L反应器中合成尿素,经10min测得反应器内气体压强变为起始的80%(已知此时尿素为固态。水为液态),则从反应开始至10min时, 的平均反应速率
的平均反应速率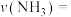
(4)若将2mol
 和1mol
和1mol  充入一容积可变的容器中进行,初始体积固定为V,10min后达到平衡时,
充入一容积可变的容器中进行,初始体积固定为V,10min后达到平衡时, 随时间变化如图所示:
随时间变化如图所示:
20min时压缩容器,使体积变为0.5V并保持不变,30min时达到新平衡,请在图中大致画出20min~40min内
 随时间t变化的曲线
随时间t变化的曲线(5)实际生产中,为节约成本并提高反应②的生产效率,尿素合成工厂通常将反应②的发生场所设置在反应①的发生场所附近,请说明理由:
您最近半年使用:0次



