名校
解题方法
1 . 一定温度下,密闭容器中发生反应:
 ,下列图示与对应的说法相符的是
,下列图示与对应的说法相符的是

 ,下列图示与对应的说法相符的是
,下列图示与对应的说法相符的是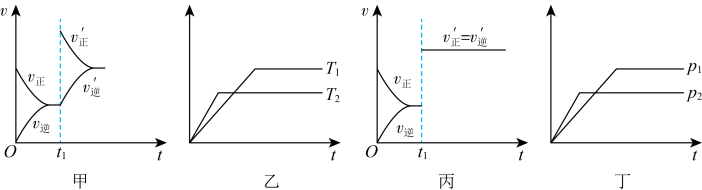
A.图甲中, 时,减小P的浓度 时,减小P的浓度 | B.图乙中,纵坐标表示生成物Q的物质的量 |
C.图丙中, 时,一定使用了催化剂 时,一定使用了催化剂 | D.图丁中,纵坐标表示反应物N的转化率 |
您最近一年使用:0次
2024-02-22更新
|
109次组卷
|
2卷引用:河北省沧州市八县联考2023-2024学年高二上学期1月期末化学试题
名校
解题方法
2 . 碳中和作为一种新型环保形式,目前已经被越来越多的大型活动和会议采用。回答下列有关问题:
(1)利用CO2合成二甲醚有两种工艺。
工艺1:涉及以下主要反应:
I.甲醇的合成:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H1=-49.0kJ/mol
Ⅱ.逆水汽变换:CO2(g)+H2(g)⇌CO(g)+H2O(g) △H2=+41.0kJ/mol
Ⅲ.甲醇脱水:2CH3OH(g)⇌CH3OCH3(g)+H2O(g) △H3=-23.5kJ/mol
工艺2:利用CO2直接加氢合成CH3OCH3和水蒸气(发应Ⅳ)
①据上述信息可知反应Ⅳ的热化学方程式为___________ 。反应I低温___________ 自发进行(填“能”或“不能”)。
②恒温恒容情况下,下列说法能判断反应Ⅳ达到平衡的是___________ 。
A.气体物质中碳元素与氧元素的质量比不变
B.容器内CH3OCH3浓度保持不变
C.容器内气体密度不变
D.容器内气体的平均摩尔质量不变
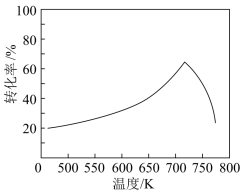
(2)对于合成甲醇的反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)由△H<0,一定条件下,单位时间内不同温度下测定的CO2转化率如图所示。温度高于710K时,随温度的升高CO2转化率降低的原因可能是___________ 。
(3)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示,两电极均为惰性电极。
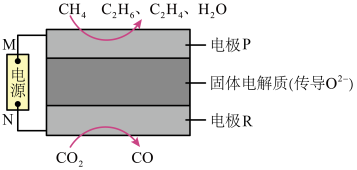
①电极M为电源的___________ 极;
②电极R上发生的电极反应为___________ 。
(1)利用CO2合成二甲醚有两种工艺。
工艺1:涉及以下主要反应:
I.甲醇的合成:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H1=-49.0kJ/mol
Ⅱ.逆水汽变换:CO2(g)+H2(g)⇌CO(g)+H2O(g) △H2=+41.0kJ/mol
Ⅲ.甲醇脱水:2CH3OH(g)⇌CH3OCH3(g)+H2O(g) △H3=-23.5kJ/mol
工艺2:利用CO2直接加氢合成CH3OCH3和水蒸气(发应Ⅳ)
①据上述信息可知反应Ⅳ的热化学方程式为
②恒温恒容情况下,下列说法能判断反应Ⅳ达到平衡的是
A.气体物质中碳元素与氧元素的质量比不变
B.容器内CH3OCH3浓度保持不变
C.容器内气体密度不变
D.容器内气体的平均摩尔质量不变
(2)对于合成甲醇的反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)由△H<0,一定条件下,单位时间内不同温度下测定的CO2转化率如图所示。温度高于710K时,随温度的升高CO2转化率降低的原因可能是

(3)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示,两电极均为惰性电极。

①电极M为电源的
②电极R上发生的电极反应为
您最近一年使用:0次
名校
3 . 根据相应的图像,下列相关说法正确的是
甲: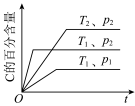 | 乙: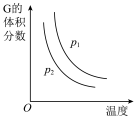 | 丙: | 丁: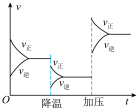 |
aA(g)+bB(g) cC(g) cC(g) | L(s)+aG(g)  bR(g) bR(g) | aA+bB cC cC | A+2B 2C+3D 2C+3D |
A.由图甲可知反应aA(g)+bB(g)  cC(g) : a+b>c 且正反应为吸热反应 cC(g) : a+b>c 且正反应为吸热反应 |
| B.反应达到平衡时外界条件对平衡影响关系如图乙所示,则正反应为吸热反应,且a>b |
| C.物质的含量和压强关系如图丙所示,可知E点v(逆)<v(正) |
| D.反应速率和反应条件变化关系如图丁所示,则该反应的正反应为放热反应,且A、B、C、D均为气体 |
您最近一年使用:0次
4 . 密闭容器中加入 ,一定条件下发生反应:
,一定条件下发生反应: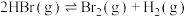 ,
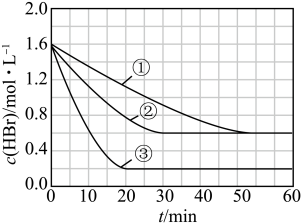
, 随反应时间的变化如曲线①所示,分别改变一个条件,得到曲线②和③,下列说法错误的是
随反应时间的变化如曲线①所示,分别改变一个条件,得到曲线②和③,下列说法错误的是
 ,一定条件下发生反应:
,一定条件下发生反应: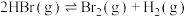 ,
, 随反应时间的变化如曲线①所示,分别改变一个条件,得到曲线②和③,下列说法错误的是
随反应时间的变化如曲线①所示,分别改变一个条件,得到曲线②和③,下列说法错误的是
| A.该反应正反应为吸热反应 |
B.曲线①,0~50min用 表示的平均反应速率为 表示的平均反应速率为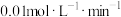 |
| C.曲线②,可能使用了催化剂或压缩容器体积 |
D.曲线③,达到平衡后,容器内各物质的浓度分别增加 ,平衡正向移动 ,平衡正向移动 |
您最近一年使用:0次
解题方法
5 . 研究 的转化可实现碳的循环利用。在反应器内
的转化可实现碳的循环利用。在反应器内 和
和 在催化剂作用下可发生如下反应:
在催化剂作用下可发生如下反应:
Ⅰ.

Ⅱ.

(1)反应I的历程如图1所示,其中吸附在催化剂表面上的物种用*标注。
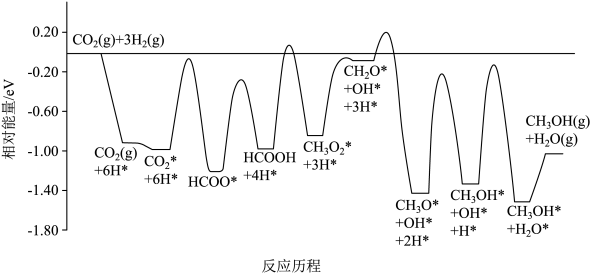
下列说法不正确的是 。
(2)若反应Ⅱ的正、逆反应速率分别表示为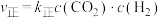 ,
,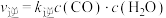 ,
, 、
、 分别为正、逆反应速率常数,c为物质的量浓度。
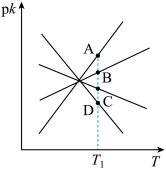
分别为正、逆反应速率常数,c为物质的量浓度。 ,如图2中有表示反应Ⅱ的正、逆反应速率常数随温度T变化的图像,若A、B、C、D点的纵坐标分别为
,如图2中有表示反应Ⅱ的正、逆反应速率常数随温度T变化的图像,若A、B、C、D点的纵坐标分别为 、
、 、
、 、
、 ,则温度
,则温度 时反应Ⅱ的化学平衡常数K=
时反应Ⅱ的化学平衡常数K=____________ 。
(3)一定条件下使 、
、 混合气体通过反应器,同时发生反应Ⅰ、Ⅱ,检测反应器出口气体的成分及其含量,计算
混合气体通过反应器,同时发生反应Ⅰ、Ⅱ,检测反应器出口气体的成分及其含量,计算 的转化率和
的转化率和 的选择性以评价催化剂的性能。
的选择性以评价催化剂的性能。
①220℃时,测得反应器出口气体中全部含碳物质的物质的量之比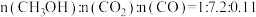 ,则该温度下
,则该温度下 转化率=
转化率=____________ 。(结果保留1位小数)
②其它条件相同时,反应温度对 的转化率和
的转化率和 的选择性的影响如图所示:
的选择性的影响如图所示:
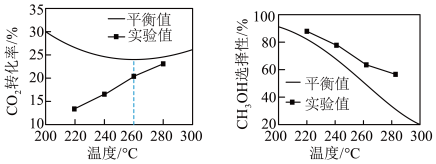
由图可知, 的转化率实验值低于其平衡值,而
的转化率实验值低于其平衡值,而 选择性的实验值却略高于其平衡值,请说明理由。
选择性的实验值却略高于其平衡值,请说明理由。__________ 。
(4)恒压下, 和
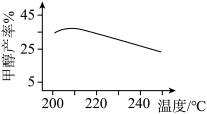
和 以物质的量比1:3投料合成甲醇(不考虑反应II),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出
以物质的量比1:3投料合成甲醇(不考虑反应II),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出 。请在图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线
。请在图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线_________ 。
 的转化可实现碳的循环利用。在反应器内
的转化可实现碳的循环利用。在反应器内 和
和 在催化剂作用下可发生如下反应:
在催化剂作用下可发生如下反应:Ⅰ.


Ⅱ.


(1)反应I的历程如图1所示,其中吸附在催化剂表面上的物种用*标注。

下列说法不正确的是 。
A.该反应的 ,能低温自发 ,能低温自发 |
B.该历程中最小能垒(活化能)步骤的化学方程式为 |
| C.催化剂可以降低反应活化能和反应热,但对反应物的转化率无影响 |
D.最后一步是 (g)、 (g)、 (g)从催化剂表面的解吸过程, (g)从催化剂表面的解吸过程, |
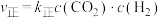 ,
,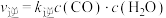 ,
, 、
、 分别为正、逆反应速率常数,c为物质的量浓度。
分别为正、逆反应速率常数,c为物质的量浓度。 ,如图2中有表示反应Ⅱ的正、逆反应速率常数随温度T变化的图像,若A、B、C、D点的纵坐标分别为
,如图2中有表示反应Ⅱ的正、逆反应速率常数随温度T变化的图像,若A、B、C、D点的纵坐标分别为 、
、 、
、 、
、 ,则温度
,则温度 时反应Ⅱ的化学平衡常数K=
时反应Ⅱ的化学平衡常数K=
(3)一定条件下使
 、
、 混合气体通过反应器,同时发生反应Ⅰ、Ⅱ,检测反应器出口气体的成分及其含量,计算
混合气体通过反应器,同时发生反应Ⅰ、Ⅱ,检测反应器出口气体的成分及其含量,计算 的转化率和
的转化率和 的选择性以评价催化剂的性能。
的选择性以评价催化剂的性能。
①220℃时,测得反应器出口气体中全部含碳物质的物质的量之比
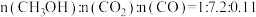 ,则该温度下
,则该温度下 转化率=
转化率=②其它条件相同时,反应温度对
 的转化率和
的转化率和 的选择性的影响如图所示:
的选择性的影响如图所示:
由图可知,
 的转化率实验值低于其平衡值,而
的转化率实验值低于其平衡值,而 选择性的实验值却略高于其平衡值,请说明理由。
选择性的实验值却略高于其平衡值,请说明理由。(4)恒压下,
 和
和 以物质的量比1:3投料合成甲醇(不考虑反应II),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出
以物质的量比1:3投料合成甲醇(不考虑反应II),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出 。请在图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线
。请在图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线
您最近一年使用:0次
解题方法
6 . 氨气的催化氧化是工业制取硝酸的重要步骤,假设只会发生以下两个竞争反应I、Ⅱ。
反应I:

反应Ⅱ:
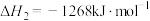
为分析某催化剂对该反应的选择性,将2mol 和3mol
和3mol 充入2L密闭容器中,在不同温度,相同时间下,测得有关物质的量关系如下图所示。下列说法不正确的是
充入2L密闭容器中,在不同温度,相同时间下,测得有关物质的量关系如下图所示。下列说法不正确的是

反应I:


反应Ⅱ:

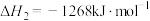
为分析某催化剂对该反应的选择性,将2mol
 和3mol
和3mol 充入2L密闭容器中,在不同温度,相同时间下,测得有关物质的量关系如下图所示。下列说法不正确的是
充入2L密闭容器中,在不同温度,相同时间下,测得有关物质的量关系如下图所示。下列说法不正确的是
A.根据图像推测, 、 、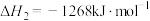 均小于0 均小于0 |
| B.该催化剂在低温时对反应Ⅱ的选择性更好 |
| C.对于反应I,NH3转化率大小顺序为:C>B>A |
| D.温度高于840℃时,NO的产率降低的原因可能是反应I的平衡常数变小 |
您最近一年使用:0次
名校
解题方法
7 . 甲烷、水蒸气催化重整是工业制备氢气的方法之一,其反应为 。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用
。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用 表示]的变化关系如图所示。
表示]的变化关系如图所示。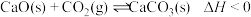 。
。
下列说法错误的是
 。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用
。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用 表示]的变化关系如图所示。
表示]的变化关系如图所示。
 。
。下列说法错误的是
| A.该反应中正反应的活化能大于逆反应的活化能 |
B.向平衡体系中加入适量的 ,可提高氢气的产率 ,可提高氢气的产率 |
C.M点甲烷的平衡转化率为 |
D.在压强为p和600℃时,若向反应器中充入 和 和 ,平衡时氢气的体积分数小于 ,平衡时氢气的体积分数小于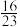 |
您最近一年使用:0次
解题方法
8 . 工业催化剂是一个催化反应工艺过程的核心,其选择性好坏、催化效率高低直接影响整个生产过程。在相同条件下研究催化剂Ⅰ、Ⅱ对反应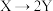 的影响,各物质浓度c随反应时间t的部分变化曲线如图,则下列说法错误的是
的影响,各物质浓度c随反应时间t的部分变化曲线如图,则下列说法错误的是
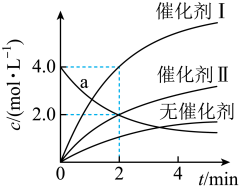
 的影响,各物质浓度c随反应时间t的部分变化曲线如图,则下列说法错误的是
的影响,各物质浓度c随反应时间t的部分变化曲线如图,则下列说法错误的是
| A.无催化剂时,反应不能进行 |
| B.与催化剂Ⅱ相比,催化剂Ⅰ使反应平衡时X的活化能更低 |
| C.a曲线表示使用催化剂Ⅰ时X的浓度随t的变化 |
| D.催化剂Ⅱ条件下,当X和Y物质的量之和不随时间变化时,反应达到平衡状态 |
您最近一年使用:0次
名校
9 . 二甲醚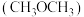 是含氢量高、廉价易得、无毒的优良制氢原料,二甲醚水蒸气重整制氢体系中发生如下反应:
是含氢量高、廉价易得、无毒的优良制氢原料,二甲醚水蒸气重整制氢体系中发生如下反应:
主反应: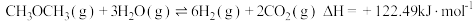
副反应: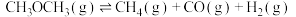
回答下列问题:
(1)上述两反应涉及的六种分子中,是非极性分子的是___________ (写出分子式)。CH4分子中的碳元素位于周期表的___________ 区。
(2)主反应在___________ (填“高温”或“低温”)下能自发进行。根据主反应,从平衡角度考虑能提高H2产率的措施有___________ (任写一种)。
(3)以水煤气作为原料制取H2可以减少副反应带来的损耗并提高H2的产量,如图是CO与水反应的历程图(附着在催化剂表面上的用·标识)。
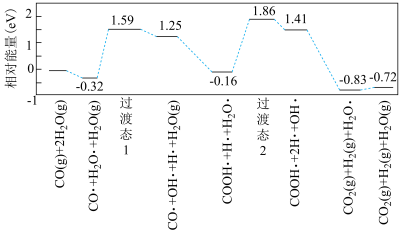
该反应历程决速步的反应方程式为___________ 。总反应的焓变___________ (填“<”或“>”)0。
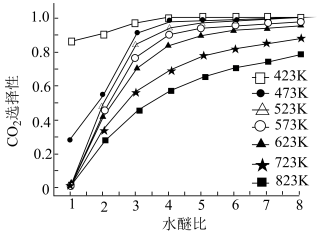
(4)如图是CO2选择性随水醚比变化的曲线,由图可知,工业上一般在___________ 条件下进行二甲醚制氢(考虑水醚比和温度两个角度)。
(5)向恒压为p的体系中充入物质的量之比为1:3的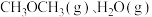 发生二甲醚水蒸气重整制氢反应,达到平衡时,二甲醚转化率为25%,且产物中
发生二甲醚水蒸气重整制氢反应,达到平衡时,二甲醚转化率为25%,且产物中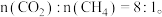
①以下说法不能判断该反应达到平衡状态的是___________ (填字母)。
A.混合气体中各物质分压保持不变 B.混合气体的密度保持不变
C.混合气体平均摩尔质量保持不变 D.消耗 时,有
时,有 生成
生成
②该温度下达到平衡时,H2O的转化率为___________ 。
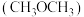 是含氢量高、廉价易得、无毒的优良制氢原料,二甲醚水蒸气重整制氢体系中发生如下反应:
是含氢量高、廉价易得、无毒的优良制氢原料,二甲醚水蒸气重整制氢体系中发生如下反应:主反应:
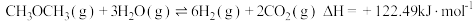
副反应:
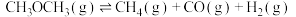
回答下列问题:
(1)上述两反应涉及的六种分子中,是非极性分子的是
(2)主反应在
(3)以水煤气作为原料制取H2可以减少副反应带来的损耗并提高H2的产量,如图是CO与水反应的历程图(附着在催化剂表面上的用·标识)。

该反应历程决速步的反应方程式为
(4)如图是CO2选择性随水醚比变化的曲线,由图可知,工业上一般在

(5)向恒压为p的体系中充入物质的量之比为1:3的
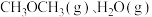 发生二甲醚水蒸气重整制氢反应,达到平衡时,二甲醚转化率为25%,且产物中
发生二甲醚水蒸气重整制氢反应,达到平衡时,二甲醚转化率为25%,且产物中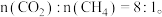
①以下说法不能判断该反应达到平衡状态的是
A.混合气体中各物质分压保持不变 B.混合气体的密度保持不变
C.混合气体平均摩尔质量保持不变 D.消耗
 时,有
时,有 生成
生成②该温度下达到平衡时,H2O的转化率为
您最近一年使用:0次
2024-02-29更新
|
59次组卷
|
2卷引用:河北正定中学本部2023-2024学年高二上学期期末考试化学试题
名校
解题方法
10 . 某密闭容器中充入等物质的量的A和B,一定温度下发生反应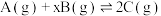 ,达到平衡后,在不同的时间段内反应物的浓度随时间的变化如甲图所示,正逆反应速率随时间的变化如乙图所示。下列说法错误的是
,达到平衡后,在不同的时间段内反应物的浓度随时间的变化如甲图所示,正逆反应速率随时间的变化如乙图所示。下列说法错误的是
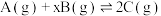 ,达到平衡后,在不同的时间段内反应物的浓度随时间的变化如甲图所示,正逆反应速率随时间的变化如乙图所示。下列说法错误的是
,达到平衡后,在不同的时间段内反应物的浓度随时间的变化如甲图所示,正逆反应速率随时间的变化如乙图所示。下列说法错误的是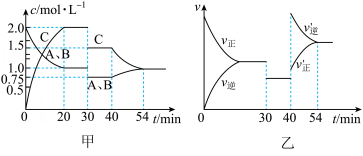
A.前20minB的平均反应速率为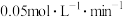 |
| B.30~40min间该反应使用了催化剂 |
C.化学方程式中的 ,正反应为放热反应 ,正反应为放热反应 |
| D.30min、40min时分别改变的条件是减小压强、升高温度 |
您最近一年使用:0次
2022-12-08更新
|
722次组卷
|
5卷引用:山东省烟台市2023届高三上学期期中学业水平诊断化学试卷
山东省烟台市2023届高三上学期期中学业水平诊断化学试卷山东省德州市第一中学2022-2023学年高二上学期期末线上考试化学试题山东省济宁市泗水县2023-2024学年高二上学期期中考试化学试题(已下线)题型18 化学反应原理综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)通关练08 聚焦反应热、速率及化学平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)



