研究 的转化可实现碳的循环利用。在反应器内
的转化可实现碳的循环利用。在反应器内 和
和 在催化剂作用下可发生如下反应:
在催化剂作用下可发生如下反应:
Ⅰ.

Ⅱ.

(1)反应I的历程如图1所示,其中吸附在催化剂表面上的物种用*标注。
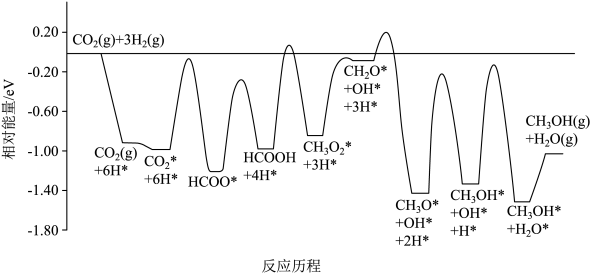
下列说法不正确的是 。
(2)若反应Ⅱ的正、逆反应速率分别表示为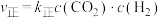 ,
,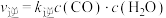 ,
, 、
、 分别为正、逆反应速率常数,c为物质的量浓度。
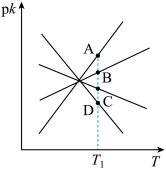
分别为正、逆反应速率常数,c为物质的量浓度。 ,如图2中有表示反应Ⅱ的正、逆反应速率常数随温度T变化的图像,若A、B、C、D点的纵坐标分别为
,如图2中有表示反应Ⅱ的正、逆反应速率常数随温度T变化的图像,若A、B、C、D点的纵坐标分别为 、
、 、
、 、
、 ,则温度
,则温度 时反应Ⅱ的化学平衡常数K=
时反应Ⅱ的化学平衡常数K=____________ 。
(3)一定条件下使 、
、 混合气体通过反应器,同时发生反应Ⅰ、Ⅱ,检测反应器出口气体的成分及其含量,计算
混合气体通过反应器,同时发生反应Ⅰ、Ⅱ,检测反应器出口气体的成分及其含量,计算 的转化率和
的转化率和 的选择性以评价催化剂的性能。
的选择性以评价催化剂的性能。
①220℃时,测得反应器出口气体中全部含碳物质的物质的量之比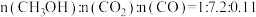 ,则该温度下
,则该温度下 转化率=
转化率=____________ 。(结果保留1位小数)
②其它条件相同时,反应温度对 的转化率和
的转化率和 的选择性的影响如图所示:
的选择性的影响如图所示:
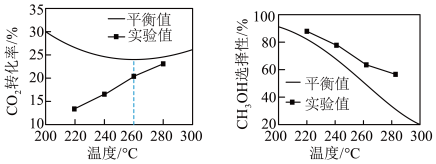
由图可知, 的转化率实验值低于其平衡值,而
的转化率实验值低于其平衡值,而 选择性的实验值却略高于其平衡值,请说明理由。
选择性的实验值却略高于其平衡值,请说明理由。__________ 。
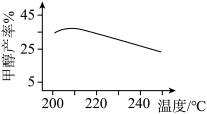
(4)恒压下, 和
和 以物质的量比1:3投料合成甲醇(不考虑反应II),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出
以物质的量比1:3投料合成甲醇(不考虑反应II),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出 。请在图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线
。请在图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线_________ 。
 的转化可实现碳的循环利用。在反应器内
的转化可实现碳的循环利用。在反应器内 和
和 在催化剂作用下可发生如下反应:
在催化剂作用下可发生如下反应:Ⅰ.


Ⅱ.


(1)反应I的历程如图1所示,其中吸附在催化剂表面上的物种用*标注。

下列说法不正确的是 。
A.该反应的 ,能低温自发 ,能低温自发 |
B.该历程中最小能垒(活化能)步骤的化学方程式为 |
| C.催化剂可以降低反应活化能和反应热,但对反应物的转化率无影响 |
D.最后一步是 (g)、 (g)、 (g)从催化剂表面的解吸过程, (g)从催化剂表面的解吸过程, |
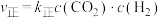 ,
,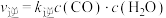 ,
, 、
、 分别为正、逆反应速率常数,c为物质的量浓度。
分别为正、逆反应速率常数,c为物质的量浓度。 ,如图2中有表示反应Ⅱ的正、逆反应速率常数随温度T变化的图像,若A、B、C、D点的纵坐标分别为
,如图2中有表示反应Ⅱ的正、逆反应速率常数随温度T变化的图像,若A、B、C、D点的纵坐标分别为 、
、 、
、 、
、 ,则温度
,则温度 时反应Ⅱ的化学平衡常数K=
时反应Ⅱ的化学平衡常数K=
(3)一定条件下使
 、
、 混合气体通过反应器,同时发生反应Ⅰ、Ⅱ,检测反应器出口气体的成分及其含量,计算
混合气体通过反应器,同时发生反应Ⅰ、Ⅱ,检测反应器出口气体的成分及其含量,计算 的转化率和
的转化率和 的选择性以评价催化剂的性能。
的选择性以评价催化剂的性能。
①220℃时,测得反应器出口气体中全部含碳物质的物质的量之比
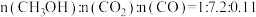 ,则该温度下
,则该温度下 转化率=
转化率=②其它条件相同时,反应温度对
 的转化率和
的转化率和 的选择性的影响如图所示:
的选择性的影响如图所示:
由图可知,
 的转化率实验值低于其平衡值,而
的转化率实验值低于其平衡值,而 选择性的实验值却略高于其平衡值,请说明理由。
选择性的实验值却略高于其平衡值,请说明理由。(4)恒压下,
 和
和 以物质的量比1:3投料合成甲醇(不考虑反应II),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出
以物质的量比1:3投料合成甲醇(不考虑反应II),在有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出 。请在图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线
。请在图中画出无分子筛膜时甲醇的平衡产率随温度的变化曲线
更新时间:2023-04-22 15:30:29
|
相似题推荐
解答题-原理综合题
|
困难
(0.15)
名校
解题方法
【推荐1】二甲醚是重要的有机合成原料:工业上常用合成气(主要成分为 、
、 )制备二甲醚,其主要反应如下:
)制备二甲醚,其主要反应如下:
反应ⅰ: ,
,
反应ⅱ: ,
,
反应ⅲ: ,
,
(1)已知 时,由稳定态单质生成
时,由稳定态单质生成 化合物的焓变称为该物质的标准摩尔生成焓
化合物的焓变称为该物质的标准摩尔生成焓 。几种物质的标准摩尔生成焓如下表所示,据此计算
。几种物质的标准摩尔生成焓如下表所示,据此计算
___________  。
。
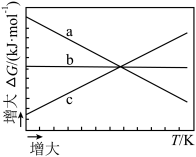
(2)已知 ,
, 随温度变化的三种趋势如下图中线条所示。能用来表示反应ⅰ的线条是
随温度变化的三种趋势如下图中线条所示。能用来表示反应ⅰ的线条是___________ (填线条字母)。
(3)在 催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。
催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。
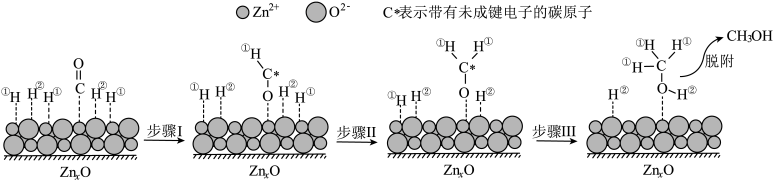
①根据元素电负性的变化规律,图中反应步骤Ⅲ可描述为___________ 。
②在合成甲醇过程中,需要不断分离出甲醇的原因为___________ (填选项字母)。
a.有利于平衡正向移动b.防止催化剂中毒c.提高正反应速率
(4)一定温度下,在体积为 的刚性容器中充入
的刚性容器中充入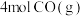 和
和 制备二甲醚,
制备二甲醚, 时达到平衡,平衡时
时达到平衡,平衡时 的转化率为80%,
的转化率为80%, ,且
,且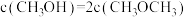 。
。
① 内,
内,
___________  。
。
②反应ⅲ的平衡常数
___________ (保留三位有效数字)。
(5)实际工业生产中,需要在260℃、压强恒为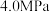 的反应釜中进行上述反应。初始时向反应釜中加入
的反应釜中进行上述反应。初始时向反应釜中加入 和
和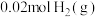 ,为确保反应的连续性,需向反应釜中以
,为确保反应的连续性,需向反应釜中以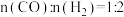 、进气流量
、进气流量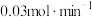 持续通入原料,同时控制出气流量。
持续通入原料,同时控制出气流量。
①需控制出气流量小于进气流量的原因为___________ 。
②已知出气流量为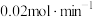 ,单位时间内
,单位时间内 的转化率为60%,则流出气体中
的转化率为60%,则流出气体中 的百分含量为
的百分含量为___________ 。
 、
、 )制备二甲醚,其主要反应如下:
)制备二甲醚,其主要反应如下:反应ⅰ:
 ,
,
反应ⅱ:
 ,
,
反应ⅲ:
 ,
,
(1)已知
 时,由稳定态单质生成
时,由稳定态单质生成 化合物的焓变称为该物质的标准摩尔生成焓
化合物的焓变称为该物质的标准摩尔生成焓 。几种物质的标准摩尔生成焓如下表所示,据此计算
。几种物质的标准摩尔生成焓如下表所示,据此计算
 。
。| 物质 |  |  |  |
 | 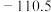 | 0.0 | 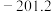 |
 ,
, 随温度变化的三种趋势如下图中线条所示。能用来表示反应ⅰ的线条是
随温度变化的三种趋势如下图中线条所示。能用来表示反应ⅰ的线条是
(3)在
 催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。
催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。
①根据元素电负性的变化规律,图中反应步骤Ⅲ可描述为
②在合成甲醇过程中,需要不断分离出甲醇的原因为
a.有利于平衡正向移动b.防止催化剂中毒c.提高正反应速率
(4)一定温度下,在体积为
 的刚性容器中充入
的刚性容器中充入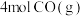 和
和 制备二甲醚,
制备二甲醚, 时达到平衡,平衡时
时达到平衡,平衡时 的转化率为80%,
的转化率为80%, ,且
,且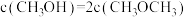 。
。①
 内,
内,
 。
。②反应ⅲ的平衡常数

(5)实际工业生产中,需要在260℃、压强恒为
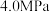 的反应釜中进行上述反应。初始时向反应釜中加入
的反应釜中进行上述反应。初始时向反应釜中加入 和
和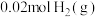 ,为确保反应的连续性,需向反应釜中以
,为确保反应的连续性,需向反应釜中以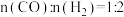 、进气流量
、进气流量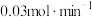 持续通入原料,同时控制出气流量。
持续通入原料,同时控制出气流量。①需控制出气流量小于进气流量的原因为
②已知出气流量为
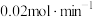 ,单位时间内
,单位时间内 的转化率为60%,则流出气体中
的转化率为60%,则流出气体中 的百分含量为
的百分含量为
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
名校
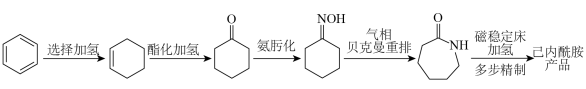
【推荐2】2023年12月具有完全知识产权、全球首套己内酰胺的绿色生产线正式在中国石化岳阳巴陵石化子公司投产。其生产流程如下:
(1)已知:①
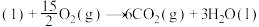
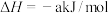
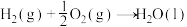

 的物质的量之比为1∶4,初始压强为5MPa的条件下,达平衡时,苯的转化率为20%,环己烷的选择性达90%,则反应②的
的物质的量之比为1∶4,初始压强为5MPa的条件下,达平衡时,苯的转化率为20%,环己烷的选择性达90%,则反应②的
___________ 。(填写计算式)
Ⅱ.苯选择加氢制环己烯是实现环己酮绿色合成新途径的关键,从热力学的角度来看极为不利,可选择更高效的催化剂,加快环己烯从催化剂的表面脱附,从而提高环己烯的选择性。采用的新型催化剂为:Ru-Zn纳米粒子@BZSS碱式复盐,通过调控BZSS滞水膜厚度进一步提高了环己烯选择性,使用该催化剂使苯的转化率达到70%以上,环己烯的选择性达到80%。已知:苯在水中的溶解度大于环己烯在水中的溶解度,新型负载型催化剂具有亲水性。
(3)请解释Ru-Zn纳米粒子@BZSS碱式复盐能提高环己烯选择性的原因(请从溶解性的角度解释):___________ 。
Ⅲ.中国石化环己酮氨肟化技术以微米级空心TS-1分子筛原粉为催化剂,并成功开发浆态床/膜分离组合新工艺,从而实现微米级催化剂的分离与连续循环使用。该环节中用蒽醌法生产过氧化氢的反应进程如下: 的分解温度为60℃,AQ的沸点377℃,AHQ的沸点390℃。
的分解温度为60℃,AQ的沸点377℃,AHQ的沸点390℃。
(4)有关该反应过程,说法不正确的是___________(填标号)。
(5)已知环己烯与羧酸发生加成反应的机理如下:
8S3SiIH催化的环烯烃与羧酸加成酯化反应结果
从表格中得出,环己烯与不同羧酸加成,其中与HCOOH反应的产率最高,最有可能的原因是___________ (从分子结构的角度解释)。而环己烯与环戊烯相比,在同样的催化剂条件下,相同温度下,环戊烯加成的产率更高的原因可能是___________ 。
(6)已知在标准状况下,AgCl的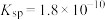 ,
, 的
的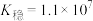 ,若把足量AgCl溶于10mol/L的氨水中,则形成的
,若把足量AgCl溶于10mol/L的氨水中,则形成的 的浓度为
的浓度为___________ mol/L(已知: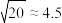 ,结果保留两位有效数字)。
,结果保留两位有效数字)。
(1)已知:①

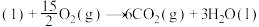
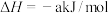
②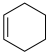
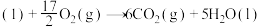
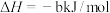
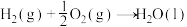

则:
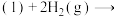

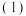

①
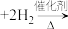
 、
、
②
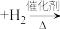
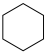 。
。
 的物质的量之比为1∶4,初始压强为5MPa的条件下,达平衡时,苯的转化率为20%,环己烷的选择性达90%,则反应②的
的物质的量之比为1∶4,初始压强为5MPa的条件下,达平衡时,苯的转化率为20%,环己烷的选择性达90%,则反应②的
Ⅱ.苯选择加氢制环己烯是实现环己酮绿色合成新途径的关键,从热力学的角度来看极为不利,可选择更高效的催化剂,加快环己烯从催化剂的表面脱附,从而提高环己烯的选择性。采用的新型催化剂为:Ru-Zn纳米粒子@BZSS碱式复盐,通过调控BZSS滞水膜厚度进一步提高了环己烯选择性,使用该催化剂使苯的转化率达到70%以上,环己烯的选择性达到80%。已知:苯在水中的溶解度大于环己烯在水中的溶解度,新型负载型催化剂具有亲水性。
(3)请解释Ru-Zn纳米粒子@BZSS碱式复盐能提高环己烯选择性的原因(请从溶解性的角度解释):
Ⅲ.中国石化环己酮氨肟化技术以微米级空心TS-1分子筛原粉为催化剂,并成功开发浆态床/膜分离组合新工艺,从而实现微米级催化剂的分离与连续循环使用。该环节中用蒽醌法生产过氧化氢的反应进程如下:
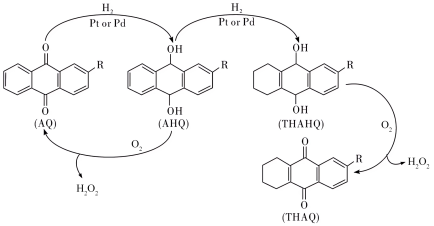
 的分解温度为60℃,AQ的沸点377℃,AHQ的沸点390℃。
的分解温度为60℃,AQ的沸点377℃,AHQ的沸点390℃。(4)有关该反应过程,说法不正确的是___________(填标号)。
A.从AQ到AHQ的反应中,发生变化的碳原子的杂化类型由 到 到 |
B.由THAHQ制备 的反应方程式为 的反应方程式为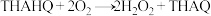 |
C.在AHQ的氧化过程中,生成的 和有机物AQ、AHQ的分离方法为蒸馏 和有机物AQ、AHQ的分离方法为蒸馏 |
| D.我国采用的浆态蒽醌氢化法,使用更高效的Pd基细颗粒催化剂,有利于提高催化的效率 |
(5)已知环己烯与羧酸发生加成反应的机理如下:

8S3SiIH催化的环烯烃与羧酸加成酯化反应结果
| 序号 | 羧酸 | 环烯烃 | 温度/℃ | 产物 | 产率/% |
| 1 | HCOOH |
| 95 |
| 90 |
| 2 |  |
| 110 |
| 82 |
| 3 |  |
| 120 |
| 62 |
| 4 | 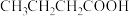 |
| 130 |
| 51 |
| 5 | HCOOH |
| 95 |
| 93 |
(6)已知在标准状况下,AgCl的
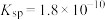 ,
, 的
的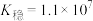 ,若把足量AgCl溶于10mol/L的氨水中,则形成的
,若把足量AgCl溶于10mol/L的氨水中,则形成的 的浓度为
的浓度为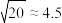 ,结果保留两位有效数字)。
,结果保留两位有效数字)。
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
【推荐3】近年来利用限域催化原理高选择性地将合成气直接制乙烯、丙烯等低碳烯烃工业,因具有流程短、能耗和煤耗低的优势,是目前煤制烯烃过程的一个研究热点。请回答下列问题:
(1)已知合成气制乙烯的热化学方程式为:2CO(g)+4H2(g) C2H4(g)+2H2O(g) ΔH = –231 kJ/mol
C2H4(g)+2H2O(g) ΔH = –231 kJ/mol
已知相关化学键的键能如下表所示,则表中的x=___________ 。
(2)新型Fe基复合催化剂高效抑制CO2生成,实现水煤气直接制取烯烃,原理如图所示。下列说法正确的是
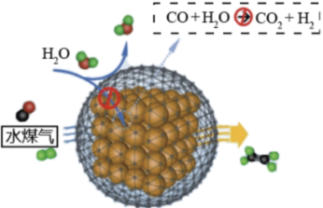
(3)在容积为1 L的密闭容器中以2∶1充入H2和 CO,在一定条件下发生反应:2CO(g)+4H2(g)  C2H4(g)+2H2O(g) ΔH = –231 kJ/mol,CO的平衡转化率与温度的关系如图所示。
C2H4(g)+2H2O(g) ΔH = –231 kJ/mol,CO的平衡转化率与温度的关系如图所示。
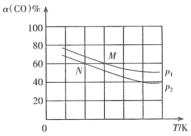
比较:P1___________ P2,M点的正反应速率___________ N点的逆反应速率。(填“>”“<”或“=”)
(4)某温度下,往体积为1 L的刚性容器中加入1 mol CO、2mol H2,在催化剂的作用下发生如下两个反应:
Ⅰ. 2CO(g)+4H2(g) C2H4(g)+2H2O(g);
C2H4(g)+2H2O(g);
Ⅱ. 3CO(g)+6H2(g) C3H6(g)+3H2O(g)
C3H6(g)+3H2O(g)
达到平衡时C2H4的体积分数为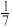 ,CO的转化率为80%,则C2H4的选择性为
,CO的转化率为80%,则C2H4的选择性为___________ 。(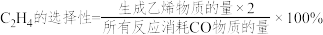 )。反应Ⅰ的平衡常数K=
)。反应Ⅰ的平衡常数K=___________ 。
(5)在常压、450℃、H2∶CO为2∶1的条件下,反应空速对CO转化率和乙烯选择性的影响如下图所示。已知:反应空速是指一定条件下,单位时间单位体积催化剂处理的气体量。

分析随着反应空速的增加,乙烯的选择性先升高后降低的原因是___________ 。
(6)在常压、H2:CO为2:1的条件下,经过相同反应时间(未达平衡)测得如下实验数据:
表中数据表明,在相同温度下不同的催化剂对CO转化为乙烯的选择性有显著的影响,其原因是______ 。
(1)已知合成气制乙烯的热化学方程式为:2CO(g)+4H2(g)
 C2H4(g)+2H2O(g) ΔH = –231 kJ/mol
C2H4(g)+2H2O(g) ΔH = –231 kJ/mol已知相关化学键的键能如下表所示,则表中的x=
| 化学键 | C≡O | H‒H | H‒O | C=C | C‒H |
| 键能/ KJ•mol-1 | x | 436 | 465 | 615 | 413 |

| A.该方法主要利用了催化剂改变反应活化能 |
| B.水煤气制取乙烯的反应中有极性键、非极性键的断裂和生成 |
| C.CO2分子和与乙烯分子空间构型相同 |
| D.与传统方法相比,该方法中反应的焓变小,产率高 |
 C2H4(g)+2H2O(g) ΔH = –231 kJ/mol,CO的平衡转化率与温度的关系如图所示。
C2H4(g)+2H2O(g) ΔH = –231 kJ/mol,CO的平衡转化率与温度的关系如图所示。
比较:P1
(4)某温度下,往体积为1 L的刚性容器中加入1 mol CO、2mol H2,在催化剂的作用下发生如下两个反应:
Ⅰ. 2CO(g)+4H2(g)
 C2H4(g)+2H2O(g);
C2H4(g)+2H2O(g);Ⅱ. 3CO(g)+6H2(g)
 C3H6(g)+3H2O(g)
C3H6(g)+3H2O(g)达到平衡时C2H4的体积分数为
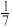 ,CO的转化率为80%,则C2H4的选择性为
,CO的转化率为80%,则C2H4的选择性为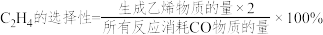 )。反应Ⅰ的平衡常数K=
)。反应Ⅰ的平衡常数K=(5)在常压、450℃、H2∶CO为2∶1的条件下,反应空速对CO转化率和乙烯选择性的影响如下图所示。已知:反应空速是指一定条件下,单位时间单位体积催化剂处理的气体量。

分析随着反应空速的增加,乙烯的选择性先升高后降低的原因是
(6)在常压、H2:CO为2:1的条件下,经过相同反应时间(未达平衡)测得如下实验数据:
| T(℃) | 催化剂 | CO转化率(%) | 乙烯选择性(%) |
| 450 | Fe-Mo-cat | 23.5 | 46.3 |
| 450 | Fe基复合催化剂 | 33.8 | 26.8 |
| 450 | 碳纳米管限域催化 | 43.5 | 58.2 |
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
名校
【推荐1】在推进碳达峰、碳中和的大背景下,可以通过多种手段实现 的减排和资源化利用。请回答下列问题:
的减排和资源化利用。请回答下列问题:
(1)科学家设想,二氧化碳加氢还原转化为推进剂甲烷,以实现星际旅行的愿望。其中涉及的主要反应如下:
反应Ⅰ:

反应Ⅱ:

①已知: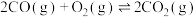
 ,则反应
,则反应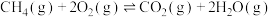 的
的
______ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
②反应Ⅰ的 与温度的关系如图1所示。已知反应Ⅰ的速率方程为
与温度的关系如图1所示。已知反应Ⅰ的速率方程为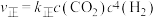 ,
, ,其中
,其中 、
、 为速率常数,只受温度影响。
为速率常数,只受温度影响。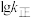 曲线的是
曲线的是______ (填“MH”或“NG”);反应Ⅰ的 (浓度平衡常数)与速率常数之间的关系为
(浓度平衡常数)与速率常数之间的关系为______ (用含 、
、 的代数式表示)。
的代数式表示)。
③向某恒压密闭容器中充入5 mol CO2、和20mol 、和在不同温度下同时发生上述反应Ⅰ和反应Ⅱ,平衡时两种含碳物质的物质的量
、和在不同温度下同时发生上述反应Ⅰ和反应Ⅱ,平衡时两种含碳物质的物质的量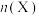 与温度T的关系如图2所示。
与温度T的关系如图2所示。______ (填含碳物质的分子式)的物质的量与温度的关系变化曲线;800K时,若平衡时容器内总压为p,图2中缺少的含碳物质平衡时为1.0 mol,则反应Ⅱ的压强平衡常数
_____ (结果保留两位有效数字, 为用分压表示的平衡常数,分压=总压×物质的量分数)。
为用分压表示的平衡常数,分压=总压×物质的量分数)。
(2)二氧化碳加氢制甲醇发生的主要化学反应如下:
①
 kJ⋅mol
kJ⋅mol
②
 kJ⋅mol
kJ⋅mol
控制压强为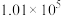 Pa、
Pa、 ,其他条件相同时,在密闭容器中发生上述反应①、②,反应温度对
,其他条件相同时,在密闭容器中发生上述反应①、②,反应温度对 的平衡转化率及
的平衡转化率及 的平衡选择性的影响如图3、4所示[
的平衡选择性的影响如图3、4所示[ 的选择性可表示为
的选择性可表示为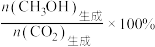 ]。
]。 的平衡转化率随温度升高而降低的原因是
的平衡转化率随温度升高而降低的原因是____________ 。
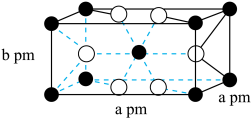
(3)金红石型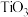 ,可用于
,可用于 催化氢化
催化氢化 ,其立方晶胞结构如图所示,设阿伏加德罗常数的值为
,其立方晶胞结构如图所示,设阿伏加德罗常数的值为 。
。______ 中心(填字母)。
A.三角形 B.四面体 C.六面体 D.八面体
②该晶体的密度为______ g·cm (用含a、b、
(用含a、b、 的代数式表示)。
的代数式表示)。
 的减排和资源化利用。请回答下列问题:
的减排和资源化利用。请回答下列问题:(1)科学家设想,二氧化碳加氢还原转化为推进剂甲烷,以实现星际旅行的愿望。其中涉及的主要反应如下:
反应Ⅰ:


反应Ⅱ:


①已知:
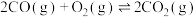
 ,则反应
,则反应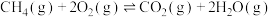 的
的
 、
、 、
、 的代数式表示)。
的代数式表示)。②反应Ⅰ的
 与温度的关系如图1所示。已知反应Ⅰ的速率方程为
与温度的关系如图1所示。已知反应Ⅰ的速率方程为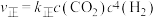 ,
, ,其中
,其中 、
、 为速率常数,只受温度影响。
为速率常数,只受温度影响。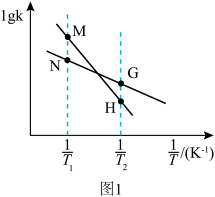
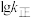 曲线的是
曲线的是 (浓度平衡常数)与速率常数之间的关系为
(浓度平衡常数)与速率常数之间的关系为 、
、 的代数式表示)。
的代数式表示)。③向某恒压密闭容器中充入5 mol CO2、和20mol
 、和在不同温度下同时发生上述反应Ⅰ和反应Ⅱ,平衡时两种含碳物质的物质的量
、和在不同温度下同时发生上述反应Ⅰ和反应Ⅱ,平衡时两种含碳物质的物质的量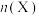 与温度T的关系如图2所示。
与温度T的关系如图2所示。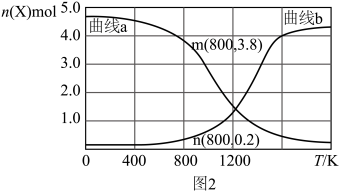

 为用分压表示的平衡常数,分压=总压×物质的量分数)。
为用分压表示的平衡常数,分压=总压×物质的量分数)。(2)二氧化碳加氢制甲醇发生的主要化学反应如下:
①

 kJ⋅mol
kJ⋅mol
②

 kJ⋅mol
kJ⋅mol
控制压强为
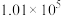 Pa、
Pa、 ,其他条件相同时,在密闭容器中发生上述反应①、②,反应温度对
,其他条件相同时,在密闭容器中发生上述反应①、②,反应温度对 的平衡转化率及
的平衡转化率及 的平衡选择性的影响如图3、4所示[
的平衡选择性的影响如图3、4所示[ 的选择性可表示为
的选择性可表示为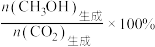 ]。
]。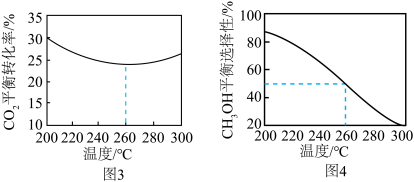
 的平衡转化率随温度升高而降低的原因是
的平衡转化率随温度升高而降低的原因是(3)金红石型
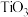 ,可用于
,可用于 催化氢化
催化氢化 ,其立方晶胞结构如图所示,设阿伏加德罗常数的值为
,其立方晶胞结构如图所示,设阿伏加德罗常数的值为 。
。
A.三角形 B.四面体 C.六面体 D.八面体
②该晶体的密度为
 (用含a、b、
(用含a、b、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
解题方法
【推荐2】 是高效光催化剂,可用四氯化钛(
是高效光催化剂,可用四氯化钛( )来制备
)来制备 。
。
已知:Ⅰ.
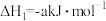
Ⅱ.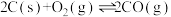
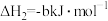
请回答下列问题:
(1)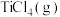 与
与 反应生成
反应生成 、
、 和氧气的热化学方程式为
和氧气的热化学方程式为_______ 。
(2)若反应Ⅰ的逆反应活化能表示为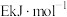 ,则E_______(填选项字母)。
,则E_______(填选项字母)。
(3)t℃时,向1L恒容密闭容器中充入0.1mol 和0.2mol
和0.2mol ,发生反应Ⅰ,经过4min达到平衡状态,平衡时测得容器中
,发生反应Ⅰ,经过4min达到平衡状态,平衡时测得容器中 的物质的量为0.02mol。
的物质的量为0.02mol。
①0~4min内 的反应速率
的反应速率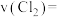
_______ 。
② 的平衡转化率
的平衡转化率
_______ 。
③下列措施即可加快反应速率,又能增大 平衡转化率的是
平衡转化率的是_______ (填选项字母)。
A.缩小容器容积 B.加入催化剂 C.分离出部分 D.增大
D.增大 浓度
浓度
④t℃时,向10L恒容密闭容器中充入4mol 和一定量
和一定量 的混合气体,发生反应Ⅰ,两种气体的平衡转化率(α)与起始的物质的量之比(
的混合气体,发生反应Ⅰ,两种气体的平衡转化率(α)与起始的物质的量之比( )的关系如图所示:
)的关系如图所示:
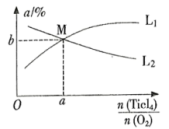
能表示 平衡转化率的曲线为
平衡转化率的曲线为_______ (填“ ”或“
”或“ ”);M点的坐标为
”);M点的坐标为_______ 。
(4)也可以利用四氯化钛( )水解制备
)水解制备 ,该反应的方程式为:
,该反应的方程式为:_______ 。
 是高效光催化剂,可用四氯化钛(
是高效光催化剂,可用四氯化钛( )来制备
)来制备 。
。已知:Ⅰ.

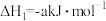
Ⅱ.
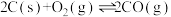
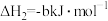
请回答下列问题:
(1)
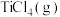 与
与 反应生成
反应生成 、
、 和氧气的热化学方程式为
和氧气的热化学方程式为(2)若反应Ⅰ的逆反应活化能表示为
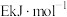 ,则E_______(填选项字母)。
,则E_______(填选项字母)。| A.大于a | B.小于a | C.等于a | D.无法确定 |
 和0.2mol
和0.2mol ,发生反应Ⅰ,经过4min达到平衡状态,平衡时测得容器中
,发生反应Ⅰ,经过4min达到平衡状态,平衡时测得容器中 的物质的量为0.02mol。
的物质的量为0.02mol。①0~4min内
 的反应速率
的反应速率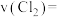
②
 的平衡转化率
的平衡转化率
③下列措施即可加快反应速率,又能增大
 平衡转化率的是
平衡转化率的是A.缩小容器容积 B.加入催化剂 C.分离出部分
 D.增大
D.增大 浓度
浓度④t℃时,向10L恒容密闭容器中充入4mol
 和一定量
和一定量 的混合气体,发生反应Ⅰ,两种气体的平衡转化率(α)与起始的物质的量之比(
的混合气体,发生反应Ⅰ,两种气体的平衡转化率(α)与起始的物质的量之比( )的关系如图所示:
)的关系如图所示:
能表示
 平衡转化率的曲线为
平衡转化率的曲线为 ”或“
”或“ ”);M点的坐标为
”);M点的坐标为(4)也可以利用四氯化钛(
 )水解制备
)水解制备 ,该反应的方程式为:
,该反应的方程式为:
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
名校
解题方法
【推荐3】氮及其化合物在工农业生产和生命活动中起着重要的作用,但同时,氮的氧化物 、
、 等又是环境污染的主要物质,研究其转化规律一直是科学热点问题。根据所学知识回答下列问题:
等又是环境污染的主要物质,研究其转化规律一直是科学热点问题。根据所学知识回答下列问题:
(1)甲烷可以催化还原氮氧化物消除氮氧化物污染,已知反应:
I.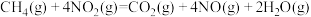

II.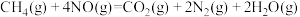

III.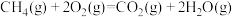

则 的
的
________ 。
(2)已知反应Ⅰ在任意温度下均能自发进行,则该反应为________ (填“吸热”或“放热”)反应。
(3) 是乙二胺四乙酸根离子,与
是乙二胺四乙酸根离子,与 形成的络合物
形成的络合物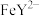 可用于吸收烟气中的
可用于吸收烟气中的 。其吸收原理:
。其吸收原理: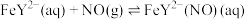
 。将含
。将含 的烟气以一定的流速通入起始温度为50℃的
的烟气以一定的流速通入起始温度为50℃的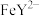 溶液中。
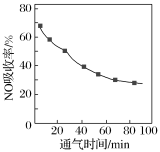
溶液中。 吸收率随通入烟气的时间的变化如图所示。时间越长,
吸收率随通入烟气的时间的变化如图所示。时间越长, 吸收率越低的原因是
吸收率越低的原因是___________ 。
(4)在一定条件下, 可直接催化分解:
可直接催化分解: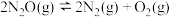 ,同时伴有副反应
,同时伴有副反应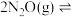
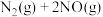 发生。
发生。
①在温度为 时,将含
时,将含 的混合气体(
的混合气体( 体积分数为40%)以
体积分数为40%)以 的流速通过催化剂,测得
的流速通过催化剂,测得 的转化率为40%,则平均反应速率
的转化率为40%,则平均反应速率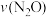 为
为________ 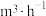 。欲提高
。欲提高 的转化率,可采取的措施为
的转化率,可采取的措施为_______________ (任写一条)。
② 和
和 时,在恒压密闭容器中进行模拟实验。各组分(
时,在恒压密闭容器中进行模拟实验。各组分( 含量极少,可忽略)的相关信息如表:
含量极少,可忽略)的相关信息如表:
其中
______ , 的平衡转化率为
的平衡转化率为______ (保留三位有效数字);该温度下,反应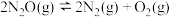 的压强平衡常数
的压强平衡常数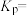
______  (用分压表示,
(用分压表示,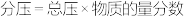 )。
)。
 、
、 等又是环境污染的主要物质,研究其转化规律一直是科学热点问题。根据所学知识回答下列问题:
等又是环境污染的主要物质,研究其转化规律一直是科学热点问题。根据所学知识回答下列问题:(1)甲烷可以催化还原氮氧化物消除氮氧化物污染,已知反应:
I.
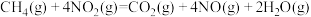

II.
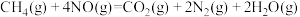

III.
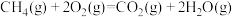

则
 的
的
(2)已知反应Ⅰ在任意温度下均能自发进行,则该反应为
(3)
 是乙二胺四乙酸根离子,与
是乙二胺四乙酸根离子,与 形成的络合物
形成的络合物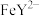 可用于吸收烟气中的
可用于吸收烟气中的 。其吸收原理:
。其吸收原理: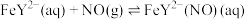
 。将含
。将含 的烟气以一定的流速通入起始温度为50℃的
的烟气以一定的流速通入起始温度为50℃的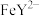 溶液中。
溶液中。 吸收率随通入烟气的时间的变化如图所示。时间越长,
吸收率随通入烟气的时间的变化如图所示。时间越长, 吸收率越低的原因是
吸收率越低的原因是
(4)在一定条件下,
 可直接催化分解:
可直接催化分解: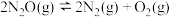 ,同时伴有副反应
,同时伴有副反应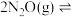
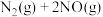 发生。
发生。①在温度为
 时,将含
时,将含 的混合气体(
的混合气体( 体积分数为40%)以
体积分数为40%)以 的流速通过催化剂,测得
的流速通过催化剂,测得 的转化率为40%,则平均反应速率
的转化率为40%,则平均反应速率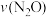 为
为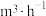 。欲提高
。欲提高 的转化率,可采取的措施为
的转化率,可采取的措施为②
 和
和 时,在恒压密闭容器中进行模拟实验。各组分(
时,在恒压密闭容器中进行模拟实验。各组分( 含量极少,可忽略)的相关信息如表:
含量极少,可忽略)的相关信息如表:物质 |
|
|
|
|
|
|
n(投料)/mol | 19 | 34 | 6.5 | 25 | 0 | 0 |
n(平衡)/mol | 50 | x | 20 | 25 | 2 | 2 |

 的平衡转化率为
的平衡转化率为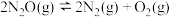 的压强平衡常数
的压强平衡常数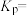
 (用分压表示,
(用分压表示,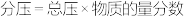 )。
)。
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
解题方法
【推荐1】液氨是一种良好的储氢物质。
已知:① 2NH3(g) N2 (g) + 3H2(g) ΔH =+92.4 kJ·mol-1
N2 (g) + 3H2(g) ΔH =+92.4 kJ·mol-1
② 液氨中2NH3(l) NH2- + NH4+
NH2- + NH4+
(1)氨气自发分解的反应条件是________ (填“低温”或“高温”)。
(2)图1为某温度下等质量的不同金属分别催化等浓度氨气分解生成氢气的初始速率。反应的活化能最大 的是__________ (填催化剂的化学式)。
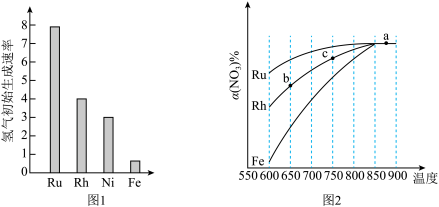
(3)其他条件相同,反应①在不同催化剂作用下反应相同时间后,氨气的转化率随反应温度的变化如图2所示。
①a点所代表的状态________ (填“是”或“不是”)平衡状态。
②c点氨气的转化率高于b点,原因是___________________________________________ 。
③请在图2中再添加一条Ni催化分解氨气过程的总趋势曲线。____________
④假设Ru催化下,温度为750℃时,氨气的初始浓度为c0,平衡转化率为40%,则该温度下此反应的 平衡常数K =_________________ 。
(4)用Pt电极对液氨进行电解也可产生H2和N2。阴极的电极反应式是____________________ 。
已知:① 2NH3(g)
 N2 (g) + 3H2(g) ΔH =+92.4 kJ·mol-1
N2 (g) + 3H2(g) ΔH =+92.4 kJ·mol-1② 液氨中2NH3(l)
 NH2- + NH4+
NH2- + NH4+(1)氨气自发分解的反应条件是
(2)图1为某温度下等质量的不同金属分别催化等浓度氨气分解生成氢气的初始速率。反应的活化能最大 的是

(3)其他条件相同,反应①在不同催化剂作用下反应相同时间后,氨气的转化率随反应温度的变化如图2所示。
①a点所代表的状态
②c点氨气的转化率高于b点,原因是
③请在图2中再添加一条Ni催化分解氨气过程的总趋势曲线。
④假设Ru催化下,温度为750℃时,氨气的初始浓度为c0,平衡转化率为40%,则该温度下此反应的 平衡常数K =
(4)用Pt电极对液氨进行电解也可产生H2和N2。阴极的电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
名校
解题方法
【推荐2】R是一种亲氯有机物,属于非电解质,易溶于水,在含Cl-的溶液中能发生如下反应。
反应I: R(aq)+Cl-(aq) RCl-(aq)
RCl-(aq)
反应II:RCl-(aq)+Cl-(aq) RCl
RCl (aq)
(aq)
回答下列问题:
(1)R的分子结构可表示为M-COOH,M为有机分子部分结构。补充完整方程式__________
R+CH3CH2OH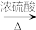 H2O +___________。
H2O +___________。
(2)常温下,向NaCl溶液中加入R,15s末测得c(RC1-)=0.07mol/L,c(RCl )=0.04mol/L。
)=0.04mol/L。
①0~15s内,Cl-的平均消耗速率v(C1-)=___________ 。
②待反应充分进行,达到平衡状态时溶液的体积为V0,加蒸馏水稀释至溶液体积为V,达到新平衡时,Cl-的物质的量浓度为c平(Cl-),RCl 的物质的量浓度为c平(RCl
的物质的量浓度为c平(RCl )。写出反应I平衡常数的表达式KI=
)。写出反应I平衡常数的表达式KI=___________ ,稀释过程中平衡常数KI的值___________ (填“变大”、“变小”或“不变”),请在答题卡坐标内 画出 随1g
随1g 的变化趋势曲线
的变化趋势曲线___________ 。
(3)室温下,向Cl-初始浓度c0(Cl-)=amol/L的NaCl溶液中加入不同量的R,用数据传感器测得平衡时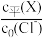 (X表示Cl-、RCl-,RCl
(X表示Cl-、RCl-,RCl 随
随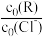 变化的数据,记录如表所示(b和d代表数字,忽略溶液体积变化):
变化的数据,记录如表所示(b和d代表数字,忽略溶液体积变化):
①从表格中数据可看出关系式: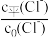 +
+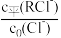 +2×
+2×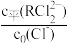 =1,则d=
=1,则d=___________ ;此关系式也可从理论上推导,下列理论依据中,可推导该关系式的有___________ (填选项序号)。
A.能量守恒定律 B.电荷守恒定律 C.质量守恒定律
D.氧化还原反应遵循还原剂失去的电子总数和氧化剂得到的电子总数相等的规律
②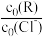 =0.50时,R的转化率为
=0.50时,R的转化率为___________ 。
反应I: R(aq)+Cl-(aq)
 RCl-(aq)
RCl-(aq)反应II:RCl-(aq)+Cl-(aq)
 RCl
RCl (aq)
(aq)回答下列问题:
(1)R的分子结构可表示为M-COOH,M为有机分子部分结构。补充完整方程式
R+CH3CH2OH
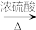 H2O +___________。
H2O +___________。(2)常温下,向NaCl溶液中加入R,15s末测得c(RC1-)=0.07mol/L,c(RCl
 )=0.04mol/L。
)=0.04mol/L。①0~15s内,Cl-的平均消耗速率v(C1-)=
②待反应充分进行,达到平衡状态时溶液的体积为V0,加蒸馏水稀释至溶液体积为V,达到新平衡时,Cl-的物质的量浓度为c平(Cl-),RCl
 的物质的量浓度为c平(RCl
的物质的量浓度为c平(RCl )。写出反应I平衡常数的表达式KI=
)。写出反应I平衡常数的表达式KI= 随1g
随1g 的变化趋势曲线
的变化趋势曲线(3)室温下,向Cl-初始浓度c0(Cl-)=amol/L的NaCl溶液中加入不同量的R,用数据传感器测得平衡时
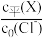 (X表示Cl-、RCl-,RCl
(X表示Cl-、RCl-,RCl 随
随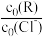 变化的数据,记录如表所示(b和d代表数字,忽略溶液体积变化):
变化的数据,记录如表所示(b和d代表数字,忽略溶液体积变化):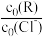 | 0 | 0.25 | 0.50 | 0.75 | 1.00 | |
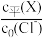 | Cl- | 1.00 | 0.79 | 0.64 | 0.54 | 0.46 |
| RCl- | 0 | 0.09 | 0.16 | 0.22 | 0.28 | |
| RCl22- | 0 | 0.06 | b | d | 0.13 | |
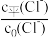 +
+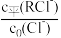 +2×
+2×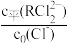 =1,则d=
=1,则d=A.能量守恒定律 B.电荷守恒定律 C.质量守恒定律
D.氧化还原反应遵循还原剂失去的电子总数和氧化剂得到的电子总数相等的规律
②
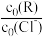 =0.50时,R的转化率为
=0.50时,R的转化率为
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
名校
解题方法
【推荐3】 催化重整
催化重整 技术可得到富含CO的化工原料。回答下列问题:
技术可得到富含CO的化工原料。回答下列问题:
(1) 催化重整
催化重整 的催化转化如图所示:
的催化转化如图所示:
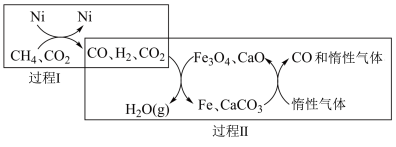
①已知相关反应的能量变化如图所示:
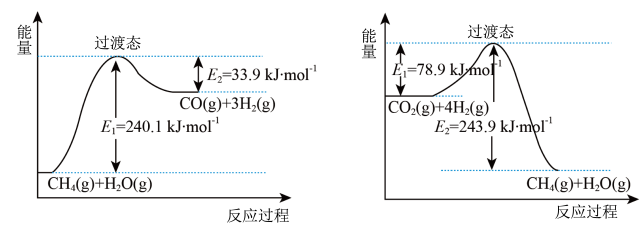
过程Ⅰ的热化学方程式为_______ 。
②关于上述过程Ⅰ、Ⅱ的说法不正确的是_______ (填序号)。
a.过程Ⅱ实现了含碳物质与含氢物质的分离
b.整个催化重整过程,消耗 理论上生成2molCO
理论上生成2molCO
c.过程Ⅰ中,Ni降低了反应的活化能
d. 、CaO为中间产物
、CaO为中间产物
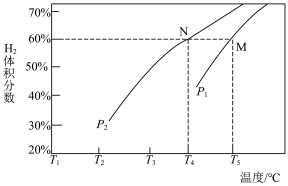
③在体积为3L的密闭容器中,加入甲烷和水蒸气各4mol,在一定条件下反应生成 、CO,测得平衡时
、CO,测得平衡时 的体积分数与温度、压强的关系如图所示。温度为
的体积分数与温度、压强的关系如图所示。温度为 ℃、压强为
℃、压强为 时,N点表示的体系状态
时,N点表示的体系状态
_______  (填“>”、“=”或“<”);M点表示的体系状态
(填“>”、“=”或“<”);M点表示的体系状态 的平衡转化率为
的平衡转化率为_______ %(结果保留一位小数)。
(2)在一刚性密闭容器中, 和
和 的分压分别为20kPa、30kPa,加入
的分压分别为20kPa、30kPa,加入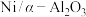 催化剂并加热至1123K使其发生反应
催化剂并加热至1123K使其发生反应 。
。
①研究表明CO的生成速率 ,某时刻测得
,某时刻测得 ,则
,则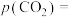
_______ kPa,
_______  。
。
②达到平衡后测得体系压强是起始时的1.6倍,则该反应的平衡常数为:
_______  (用各物质的分压代替物质的量浓度计算)。
(用各物质的分压代替物质的量浓度计算)。
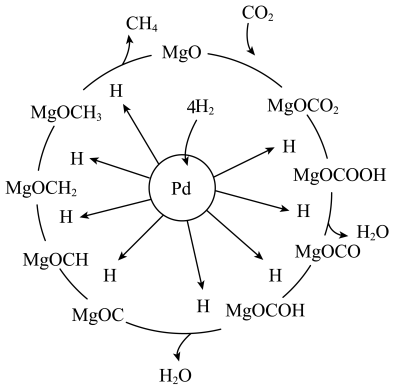
(3)一定条件下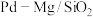 催化剂可使
催化剂可使 “甲烷化”从而变废为宝,其反应机理如图所示,该反应的化学方程式为
“甲烷化”从而变废为宝,其反应机理如图所示,该反应的化学方程式为_______ ,反应过程中碳元素的化合价为-3价的中间体是_______ 。
 催化重整
催化重整 技术可得到富含CO的化工原料。回答下列问题:
技术可得到富含CO的化工原料。回答下列问题:(1)
 催化重整
催化重整 的催化转化如图所示:
的催化转化如图所示:
①已知相关反应的能量变化如图所示:

过程Ⅰ的热化学方程式为
②关于上述过程Ⅰ、Ⅱ的说法不正确的是
a.过程Ⅱ实现了含碳物质与含氢物质的分离
b.整个催化重整过程,消耗
 理论上生成2molCO
理论上生成2molCOc.过程Ⅰ中,Ni降低了反应的活化能
d.
 、CaO为中间产物
、CaO为中间产物③在体积为3L的密闭容器中,加入甲烷和水蒸气各4mol,在一定条件下反应生成
 、CO,测得平衡时
、CO,测得平衡时 的体积分数与温度、压强的关系如图所示。温度为
的体积分数与温度、压强的关系如图所示。温度为 ℃、压强为
℃、压强为 时,N点表示的体系状态
时,N点表示的体系状态
 (填“>”、“=”或“<”);M点表示的体系状态
(填“>”、“=”或“<”);M点表示的体系状态 的平衡转化率为
的平衡转化率为
(2)在一刚性密闭容器中,
 和
和 的分压分别为20kPa、30kPa,加入
的分压分别为20kPa、30kPa,加入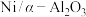 催化剂并加热至1123K使其发生反应
催化剂并加热至1123K使其发生反应 。
。①研究表明CO的生成速率
 ,某时刻测得
,某时刻测得 ,则
,则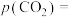

 。
。②达到平衡后测得体系压强是起始时的1.6倍,则该反应的平衡常数为:

 (用各物质的分压代替物质的量浓度计算)。
(用各物质的分压代替物质的量浓度计算)。(3)一定条件下
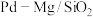 催化剂可使
催化剂可使 “甲烷化”从而变废为宝,其反应机理如图所示,该反应的化学方程式为
“甲烷化”从而变废为宝,其反应机理如图所示,该反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
名校
解题方法
【推荐1】全球大气 浓度升高对人类生产、生活产生了影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
浓度升高对人类生产、生活产生了影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
(1)已知25℃时,大气中的 溶于水存在以下过程:
溶于水存在以下过程:
①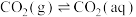
②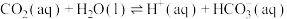

过程①的
_______ 0(填“>”“<”或“=”)。溶液中 的浓度与其在大气中的分压(分压=总压×物质的量分数)成正比,比例系数为
的浓度与其在大气中的分压(分压=总压×物质的量分数)成正比,比例系数为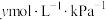 。当大气压强为
。当大气压强为 ,大气中
,大气中 的物质的量分数为x时,溶液中
的物质的量分数为x时,溶液中 的浓度为
的浓度为_______  (忽略
(忽略 和水的电离)。
和水的电离)。
(2)焦炭与水蒸气可在高温下反应制 。
。
反应Ⅰ:
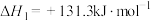

反应Ⅱ: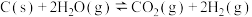
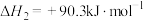

反应Ⅲ:
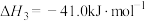

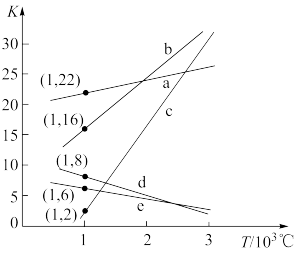
①上述反应的化学平衡常数随温度变化的关系如图所示,表示 、
、 、
、 的曲线分别是c、
的曲线分别是c、_______ 、_______ 。
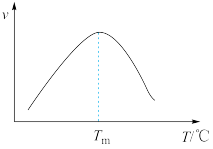
②研究表明,反应Ⅲ的速率方程为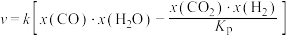 ,x表示相应气体的物质的量分数,Kp为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。在气体物质的量分数和催化剂一定的情况下,反应速率随温度的变化如图所示。根据速率方程分析T>Tm时,v逐渐下降的原因是
,x表示相应气体的物质的量分数,Kp为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。在气体物质的量分数和催化剂一定的情况下,反应速率随温度的变化如图所示。根据速率方程分析T>Tm时,v逐渐下降的原因是_______ 。
(3)甲烷干法重整制 同时存在如下反应:
同时存在如下反应:
主反应:

副反应:

温度为T℃,压强为 的恒压密闭容器中,通入2mol
的恒压密闭容器中,通入2mol 和1mol
和1mol 发生上述反应。平衡时
发生上述反应。平衡时 的分压为
的分压为 ,甲烷的转化率为40%。
,甲烷的转化率为40%。
①下列说法正确的是_______ (填标号)
A. 和
和 不变,说明反应达到平衡状态
不变,说明反应达到平衡状态
B.相同条件下,主反应的速率大于副反应,说明主反应的活化能小
C.选用合适的催化剂可以提高主反应的选择性,增大甲烷的平衡转化率
D.平衡后,若增大压强,主反应平衡逆向移动,副反应平衡不移动
②平衡时混合气体的总物质的量为_______ mol,主反应的平衡常数
_______ (用含 和
和 的计算式表示)。
的计算式表示)。
 浓度升高对人类生产、生活产生了影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
浓度升高对人类生产、生活产生了影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:(1)已知25℃时,大气中的
 溶于水存在以下过程:
溶于水存在以下过程:①
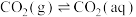
②
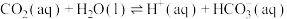

过程①的

 的浓度与其在大气中的分压(分压=总压×物质的量分数)成正比,比例系数为
的浓度与其在大气中的分压(分压=总压×物质的量分数)成正比,比例系数为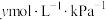 。当大气压强为
。当大气压强为 ,大气中
,大气中 的物质的量分数为x时,溶液中
的物质的量分数为x时,溶液中 的浓度为
的浓度为 (忽略
(忽略 和水的电离)。
和水的电离)。(2)焦炭与水蒸气可在高温下反应制
 。
。反应Ⅰ:

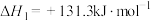

反应Ⅱ:
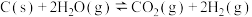
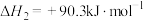

反应Ⅲ:

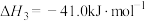

①上述反应的化学平衡常数随温度变化的关系如图所示,表示
 、
、 、
、 的曲线分别是c、
的曲线分别是c、
②研究表明,反应Ⅲ的速率方程为
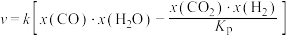 ,x表示相应气体的物质的量分数,Kp为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。在气体物质的量分数和催化剂一定的情况下,反应速率随温度的变化如图所示。根据速率方程分析T>Tm时,v逐渐下降的原因是
,x表示相应气体的物质的量分数,Kp为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。在气体物质的量分数和催化剂一定的情况下,反应速率随温度的变化如图所示。根据速率方程分析T>Tm时,v逐渐下降的原因是
(3)甲烷干法重整制
 同时存在如下反应:
同时存在如下反应:主反应:


副反应:


温度为T℃,压强为
 的恒压密闭容器中,通入2mol
的恒压密闭容器中,通入2mol 和1mol
和1mol 发生上述反应。平衡时
发生上述反应。平衡时 的分压为
的分压为 ,甲烷的转化率为40%。
,甲烷的转化率为40%。①下列说法正确的是
A.
 和
和 不变,说明反应达到平衡状态
不变,说明反应达到平衡状态B.相同条件下,主反应的速率大于副反应,说明主反应的活化能小
C.选用合适的催化剂可以提高主反应的选择性,增大甲烷的平衡转化率
D.平衡后,若增大压强,主反应平衡逆向移动,副反应平衡不移动
②平衡时混合气体的总物质的量为

 和
和 的计算式表示)。
的计算式表示)。
您最近一年使用:0次
解答题-原理综合题
|
困难
(0.15)
解题方法
【推荐2】NOx、CO 都是常见的空气污染物,研究它们的处理方法对环境保护有重要的意义。
(1)用催化剂将NO和CO转化为N2和CO2是处理尾气的重要方式之一。在298K,101kPa时,相关反应如下:
I:2NO(g)+2CO(g) 2CO2(g)+N2(g) △H1= -751 kJ·mol-1,△S=-197.5J·mol -1K-1
2CO2(g)+N2(g) △H1= -751 kJ·mol-1,△S=-197.5J·mol -1K-1
Ⅱ:4NO(g) N2O(g)+O2(g)
N2O(g)+O2(g)
Ⅲ:2CO(g)+O2(g) 2CO2(g)
2CO2(g)
请回答:
①反应I在298K时能否自发进行_______ (填“能”或者“否”)。
②目前汽车排气管内部装有三元催化器,尾气中反应物或生成物浓度随温度变化如图2、图3 所示。

请选择使用三元催化剂的最佳温度______________ ,并说明理由___________________________ 。
③为探究温度对催化剂催化效果的影响,将固定比例 NO、CO 混合气体,以一定流速通过三元催化剂排气管,相同时间内测量尾气中 NO 的含量,得到脱氮率随温度变化如图所示,已知图中 BC 段为平衡状态,且平衡脱氮率为 m-n×10 -4T2,100℃≤T≤1000℃,m、n 为常数。下列说法不正确的是_______ 。
A.平衡脱氮率 m-n×10 -4T2表达式中:m=0.69,n=2.5×10-3
B.CD 段处于平衡状态,因反应 I 正向放热,升温平衡逆向移动,故脱氮率降低
C.D 点平衡脱氮率为 44%
D.BA 段因温度下降,催化剂活性降低,故平衡脱氮率下降

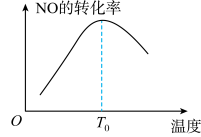
(2)工业上也可用 CH4在催化剂作用下还原 NO 消除污染,其反应为CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(g) △H<0。相同时间测得 NO 的转化率随反应温度变化的情况如图所示。请在图中画出其他条件不变,增大压强(催化剂未失活)情况下,NO 的转化率随温度变化的图像
2N2(g)+CO2(g)+2H2O(g) △H<0。相同时间测得 NO 的转化率随反应温度变化的情况如图所示。请在图中画出其他条件不变,增大压强(催化剂未失活)情况下,NO 的转化率随温度变化的图像_______ 。
(3)一种焦炭催化 CO 还原 NO 反应的历程如下,请补充完整相关基元反应(“*”表示吸附态):
A.NO NO*
NO*
B.2NO* ON-NO*
ON-NO*
C.___________
D.ON-NO-CO* ON-N*+CO2
ON-N*+CO2
E.___________
(1)用催化剂将NO和CO转化为N2和CO2是处理尾气的重要方式之一。在298K,101kPa时,相关反应如下:
I:2NO(g)+2CO(g)
 2CO2(g)+N2(g) △H1= -751 kJ·mol-1,△S=-197.5J·mol -1K-1
2CO2(g)+N2(g) △H1= -751 kJ·mol-1,△S=-197.5J·mol -1K-1Ⅱ:4NO(g)
 N2O(g)+O2(g)
N2O(g)+O2(g) Ⅲ:2CO(g)+O2(g)
 2CO2(g)
2CO2(g) 请回答:
①反应I在298K时能否自发进行
②目前汽车排气管内部装有三元催化器,尾气中反应物或生成物浓度随温度变化如图2、图3 所示。

请选择使用三元催化剂的最佳温度
③为探究温度对催化剂催化效果的影响,将固定比例 NO、CO 混合气体,以一定流速通过三元催化剂排气管,相同时间内测量尾气中 NO 的含量,得到脱氮率随温度变化如图所示,已知图中 BC 段为平衡状态,且平衡脱氮率为 m-n×10 -4T2,100℃≤T≤1000℃,m、n 为常数。下列说法不正确的是
A.平衡脱氮率 m-n×10 -4T2表达式中:m=0.69,n=2.5×10-3
B.CD 段处于平衡状态,因反应 I 正向放热,升温平衡逆向移动,故脱氮率降低
C.D 点平衡脱氮率为 44%
D.BA 段因温度下降,催化剂活性降低,故平衡脱氮率下降

(2)工业上也可用 CH4在催化剂作用下还原 NO 消除污染,其反应为CH4(g)+4NO(g)
 2N2(g)+CO2(g)+2H2O(g) △H<0。相同时间测得 NO 的转化率随反应温度变化的情况如图所示。请在图中画出其他条件不变,增大压强(催化剂未失活)情况下,NO 的转化率随温度变化的图像
2N2(g)+CO2(g)+2H2O(g) △H<0。相同时间测得 NO 的转化率随反应温度变化的情况如图所示。请在图中画出其他条件不变,增大压强(催化剂未失活)情况下,NO 的转化率随温度变化的图像
(3)一种焦炭催化 CO 还原 NO 反应的历程如下,请补充完整相关基元反应(“*”表示吸附态):
A.NO
 NO*
NO* B.2NO*
 ON-NO*
ON-NO* C.
D.ON-NO-CO*
 ON-N*+CO2
ON-N*+CO2E.
您最近一年使用:0次
【推荐3】3D打印对钛粉要求很高,熔盐电解精炼是制取钛粉的有效途径。精炼时一般采用按一定比例组成的NaCl-KCl熔盐,其中含有一定浓度的低价氯化钛( ,x=2、3)。回答下列问题:
,x=2、3)。回答下列问题:
(1)精炼制海绵钛时,废旧钛网作电解池的___________ 极。
(2) 的一种制备原理为
的一种制备原理为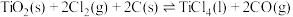
 。一定温度下,恒容密闭容器中发生该反应至平衡后,继续通入一定量的
。一定温度下,恒容密闭容器中发生该反应至平衡后,继续通入一定量的 ,则
,则 的平衡转化率将
的平衡转化率将______ (填“增大”“减小”或“不变”,下同), 的浓度将
的浓度将___________ 。
(3)采用海绵钛(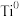 ,固态)与
,固态)与 制取低价钛离子(
制取低价钛离子( 、
、 )的电解质熔盐时,熔盐中存下如下4个反应:
)的电解质熔盐时,熔盐中存下如下4个反应:
i.

ii.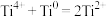

iii.

iv.∙∙∙∙∙∙
反应iv的离子方程式为___________ ;上述4个反应的平衡常数与温度的关系如图,由此可知
___________ (填“>”“<”或“=”)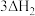 。
。

(4)向下图装置中加入海绵钛,从石英管中缓慢加入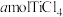 ,恒温条件下进行反应。
,恒温条件下进行反应。
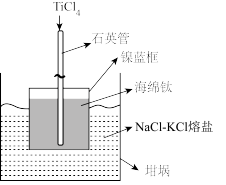
①平衡时,测得消耗海绵钛及 的物质的量分别为bmol、cmol。熔盐中低价钛离子的平均价态为
的物质的量分别为bmol、cmol。熔盐中低价钛离子的平均价态为___________ 。
②反应iii以物质的量分数表示的平衡常数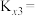
___________ 。
 ,x=2、3)。回答下列问题:
,x=2、3)。回答下列问题:(1)精炼制海绵钛时,废旧钛网作电解池的
(2)
 的一种制备原理为
的一种制备原理为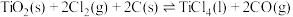
 。一定温度下,恒容密闭容器中发生该反应至平衡后,继续通入一定量的
。一定温度下,恒容密闭容器中发生该反应至平衡后,继续通入一定量的 ,则
,则 的平衡转化率将
的平衡转化率将 的浓度将
的浓度将(3)采用海绵钛(
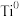 ,固态)与
,固态)与 制取低价钛离子(
制取低价钛离子( 、
、 )的电解质熔盐时,熔盐中存下如下4个反应:
)的电解质熔盐时,熔盐中存下如下4个反应:i.


ii.
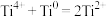

iii.


iv.∙∙∙∙∙∙

反应iv的离子方程式为

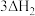 。
。
(4)向下图装置中加入海绵钛,从石英管中缓慢加入
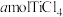 ,恒温条件下进行反应。
,恒温条件下进行反应。
①平衡时,测得消耗海绵钛及
 的物质的量分别为bmol、cmol。熔盐中低价钛离子的平均价态为
的物质的量分别为bmol、cmol。熔盐中低价钛离子的平均价态为②反应iii以物质的量分数表示的平衡常数
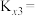
您最近一年使用:0次