18-19高一·浙江·期中
1 . 工业上,通常将乙苯蒸气和水蒸气以物质的量之比为1:9混合,控制一定的反应温度,并保持体系总压为常压的条件下进行反应制苯乙烯: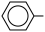 CH2CH3(g)
CH2CH3(g)
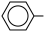 CH=CH2(g)+H2(g)在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)如图所示,下列说法
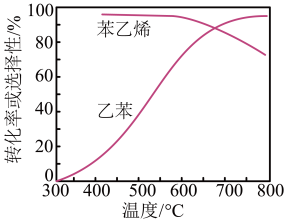
CH=CH2(g)+H2(g)在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)如图所示,下列说法不正确 的是( )
 CH2CH3(g)
CH2CH3(g)
 CH=CH2(g)+H2(g)在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)如图所示,下列说法
CH=CH2(g)+H2(g)在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)如图所示,下列说法
| A.随着反应的温度不断升高,乙苯的转化率和苯乙烯的选择性均迅速地升高 |
| B.工业上控制反应温度600℃,因为该温度下乙苯转化率和苯乙烯选择性均较高 |
| C.工业上在乙苯蒸气中掺入水蒸气,相当于减小原反应物的浓度 |
| D.当温度偏低时,虽然苯乙烯选择性较大,但乙苯转化率低,反应速率较慢 |
您最近一年使用:0次
名校
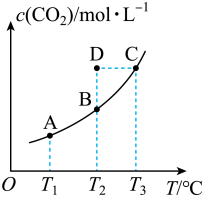
2 . 在恒容密闭容器中存在下列平衡:CO(g)+H2O(g) CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是( )
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是( )
 CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是( )
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是( )
A.反应CO(g)+H2O(g) CO2(g)+H2(g)的ΔH<0 CO2(g)+H2(g)的ΔH<0 |
| B.在T2时,若反应处于状态D,则一定有v正<v逆 |
| C.平衡状态A与C相比,平衡状态A的c(CO)大 |
| D.使用合适的催化剂能提高CO的转化率 |
您最近一年使用:0次
2020-10-14更新
|
153次组卷
|
2卷引用:福建省莆田市第二中学2021届高三10月月考化学试题
2018高三上·全国·专题练习
名校
解题方法
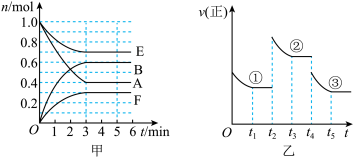
3 . 某温度时,在体积为2L的密闭容器中,气态物质A、B、E、F的物质的量n随时间t的变化情况如图甲所示,在一定条件下反应达到平衡状态,反应进程中正反应速率随时间的变化情况如图乙所示,在 、
、 时刻分别只改变一个条件
时刻分别只改变一个条件 温度、压强或某反应物的量
温度、压强或某反应物的量 。下列说法错误的是
。下列说法错误的是
 、
、 时刻分别只改变一个条件
时刻分别只改变一个条件 温度、压强或某反应物的量
温度、压强或某反应物的量 。下列说法错误的是
。下列说法错误的是 
A.此温度下,该反应的化学方程式为 |
B.若平衡状态 和 和 对应的温度相同,则 对应的温度相同,则 和 和 对应的平衡常数K一定相同 对应的平衡常数K一定相同 |
C. 时刻改变的条件是增大压强 时刻改变的条件是增大压强 |
D. 时刻改变的条件是降低温度 时刻改变的条件是降低温度 |
您最近一年使用:0次
2020-01-25更新
|
280次组卷
|
14卷引用:2018年9月26日《每日一题》一轮复习化学反应速率和化学平衡图象
(已下线)2018年9月26日《每日一题》一轮复习化学反应速率和化学平衡图象四川省成都市外国语学校2019届高三上学期第一次月考化学试题(已下线)2019年4月13日《每日一题》三轮复习—— 周末培优(已下线)2019年9月25日 《每日一题》2020年高考一轮复习-化学反应速率和化学平衡图象河北省衡水中学2020届高三上学期第四次调研考试化学试题2020届高三化学二轮冲刺新题专练——化学反应速率的图像分析(提升练)2020届高三化学二轮冲刺新题专练——化学反应速率的图像分析(已下线)专题讲座(五)反应速率、平衡图像题解题策略(练) — 2022年高考化学一轮复习讲练测(新教材新高考)上海交通大学附属中学2021-2022高二上学期开学摸底测试化学试题宁夏银川一中2021-2022学年高二上学期期中考试化学试题宁夏石嘴山市第三中学2021-2022学年高二下学期第一次月考化学试题山东省东营市第一中学2021-2022学年高二上学期期中考试化学试题2020届高三化学二轮冲刺新题专练——化学平衡移动及其影响因素(已下线)第七章 化学反应速率与化学平衡 第44练 化学反应速率、平衡的常规图像
4 . 某密闭容器中发生如下反应:2X(g)+Y(g)⇌2Z(g) △H<0,图是表示该反应速率(v)随时间(t)变化的关系图。t2、t3、t5时刻外界条件均有改变(但都没有改变各物质的用量)。下列说法中正确的是( )


| A.t2时是使用了正催化剂 |
| B.t5时增大了压强 |
| C.t3时降低了温度 |
| D.t4时该反应的平衡常数大于t6时反应的平衡常数 |
您最近一年使用:0次
2021-01-04更新
|
234次组卷
|
2卷引用:海南省北京师范大学万宁附属中学2019-2020学年高一下学期期末考试化学试题
解题方法
5 . 如图表示可逆反应A(g)+3B(g)⇌2C(g) △H<0达平衡后,t1时改变某一反应条件,反应速率随时间变化的情况,根据曲线判断下列说法中正确的是( )
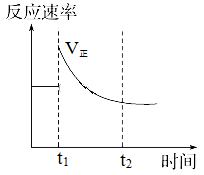

| A.t1时降低了温度,平衡向正反应方向移动 |
| B.t1时增大了压强,平衡向正反应方向移动 |
| C.t1时可能使用了催化剂 |
| D.t1时增大了A的浓度,同时减小了C的浓度,平衡向正反应方向移动 |
您最近一年使用:0次
2019-12-28更新
|
308次组卷
|
4卷引用:内蒙古通辽市科左后旗甘旗卡第二高级中学2020届高三12月月考化学试题
内蒙古通辽市科左后旗甘旗卡第二高级中学2020届高三12月月考化学试题(已下线)单科化学-2021年秋季高三开学摸底考试卷02(课标全国专用)四川省成都高新实验中学2021-2022学年高三上学期入学考试化学试题黑龙江省齐齐哈尔普高十校2022-2023学年高三上学期期末考试化学试题
名校
6 . 向一体积不变的密闭容器中加入2 mol A、0.6 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知t3-t4阶段为使用催化剂;图一中t0-t1阶段c(B)未画出。
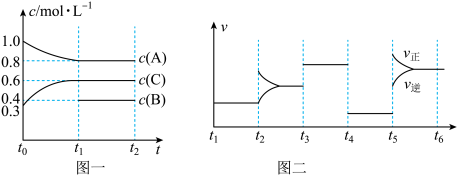
下列说法不正确的是

下列说法不正确的是
A.此温度下该反应的化学方程式为2A(g)+B(s) 3C(g) 3C(g) |
| B.t4-t5阶段改变的条件为减小压强 |
| C.B的起始物质的量为1.0 mol |
| D.在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为a+2c/3=2.4和b+c/3=1.2 |
您最近一年使用:0次
2019-09-30更新
|
224次组卷
|
2卷引用:甘肃省张掖市山丹县第一中学2019-2020学年上学期9月月考--高二化学
名校
解题方法
7 . 在一定温度下的密闭容器中发生反应:2X(g)+Y(g) 2Z(g),平衡后的某一时刻(t1)改变了外界条件,其反应速率随时间的变化图像如图所示,则下列说法符合该图像的是( )
2Z(g),平衡后的某一时刻(t1)改变了外界条件,其反应速率随时间的变化图像如图所示,则下列说法符合该图像的是( )
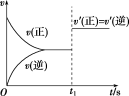
 2Z(g),平衡后的某一时刻(t1)改变了外界条件,其反应速率随时间的变化图像如图所示,则下列说法符合该图像的是( )
2Z(g),平衡后的某一时刻(t1)改变了外界条件,其反应速率随时间的变化图像如图所示,则下列说法符合该图像的是( )
| A.t1时刻,增大了X的浓度 |
| B.t1时刻,升高了体系温度 |
| C.t1时刻,缩小了容器体积 |
| D.t1时刻,使用了催化剂 |
您最近一年使用:0次
2019-12-19更新
|
108次组卷
|
2卷引用:四川省广安市岳池县顾县中学2019—2020学年第一学期高二上学期期中测试化学(选修四)试题
名校
解题方法
8 . 在容积不变的密闭容器中,发生可逆反应A(g)+2B(g) 3C(g)+D(s)ΔH<0,当其他条件不变时改变某一条件,对此反应的影响可用如图像表示。下列说法错误的是
3C(g)+D(s)ΔH<0,当其他条件不变时改变某一条件,对此反应的影响可用如图像表示。下列说法错误的是
 3C(g)+D(s)ΔH<0,当其他条件不变时改变某一条件,对此反应的影响可用如图像表示。下列说法错误的是
3C(g)+D(s)ΔH<0,当其他条件不变时改变某一条件,对此反应的影响可用如图像表示。下列说法错误的是
| A.图Ⅰ表示t1时刻升高温度对反应速率的影响 |
| B.图Ⅰ不能表示t1时刻增大C物质的浓度对反应速率的影响 |
| C.图Ⅱ一定表示的是在t1时刻使用了催化剂对反应速率的影响 |
| D.图Ⅲ乙的温度比甲的温度高 |
您最近一年使用:0次
2020-12-16更新
|
639次组卷
|
6卷引用:安徽省合肥市第七中学2020-2021学年高二上学期第一次段考化学试卷
安徽省合肥市第七中学2020-2021学年高二上学期第一次段考化学试卷浙江省诸暨市2018-2019学年高一下学期期末考试化学试题 (已下线)专题24 化学平衡图像题的突破-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)湖北省黄冈市麻城市第二中学2021-2022学年高二上学期期中考试化学试题(已下线)题型12 化学平衡图表分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)湖南省益阳市桃江县第四中学2023-2024学年高二上学期第一次月考化学试卷
名校
解题方法
9 . 在恒容条件下发生反应A(g)+3B(g)⇌2C(g)(ΔH<0),改变其他反应条件,在I,II阶段体系中各物质的浓度随时间变化的曲线如图所示。下列说法中正确的是


| A.第I阶段用C表示的平衡前的反应速率v(C)=0.1mol/(L·s) |
| B.由第一次平衡到第二次平衡,可能采取的措施是从反应体系中移出产物C |
| C.第I阶段的平衡常数KI与第II阶段平衡常数KII的大小关系是:KI<KII |
| D.第I阶段中B的平衡转化率αII(B)=0.019 |
您最近一年使用:0次
2019高三·全国·专题练习
10 . 向某密闭容器中加入0.3 mol A、0.1 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如甲图所示[t0~t1阶段c(B)未画出]。乙图为t2时刻后改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知,t3~t4阶段使用催化剂。下列说法中不正确的是( )
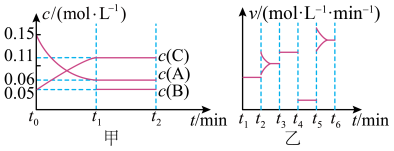

| A.若t1=15 min,则用C的浓度变化表示在t0~t1时间段的平均反应速率为0.004 mol·L-1·min-1 |
| B.t4~t5阶段改变的条件一定是减小压强 |
| C.B的起始物质的量为0.02 mol |
| D.t5~t6阶段,容器内A的物质的量减少了0.03 mol,而此过程中容器与外界的热交换总量为a kJ,则该反应的热化学方程式为3A(g) ⇌B(g)+2C(g) ΔH=+100a kJ·mol-1 |
您最近一年使用:0次



