1 . 异丁醇催化脱水制备异丁烯主要涉及以下2个反应。研究一定压强下不同含水量的异丁醇在恒压反应器中的脱水反应,得到了异丁烯的平衡产率随温度的变化结果如图。

①
②
下列说法不正确的是

①

②

下列说法不正确的是
| A.其他条件不变时,在催化剂的活性温度内,升高温度有利于异丁烯的制备 |
B.高于190℃时,温度对异丁烯的平衡产率影响不大的原因是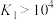 、 、 |
C.190℃时,增大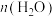 ∶n(异丁醇),不利于反应②的进行 ∶n(异丁醇),不利于反应②的进行 |
D.若只有异丁烯、水和二聚异丁烯生成,则初始物质浓度 与流出物质浓度c之间存在: 与流出物质浓度c之间存在: (异丁醇)=c(异丁烯)+2c(二聚异丁烯) (异丁醇)=c(异丁烯)+2c(二聚异丁烯) |
您最近一年使用:0次
解题方法
2 . 工业上可通过甲醇羰基化法制取甲酸甲酯( ):
):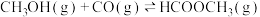 ,在容积固定的密闭容器中,投入等物质的量
,在容积固定的密闭容器中,投入等物质的量 和CO,测得相同时间内CO的转化率随温度变化曲线如图所示。下列说法不正确的是
和CO,测得相同时间内CO的转化率随温度变化曲线如图所示。下列说法不正确的是

 ):
):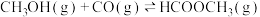 ,在容积固定的密闭容器中,投入等物质的量
,在容积固定的密闭容器中,投入等物质的量 和CO,测得相同时间内CO的转化率随温度变化曲线如图所示。下列说法不正确的是
和CO,测得相同时间内CO的转化率随温度变化曲线如图所示。下列说法不正确的是
| A.增大甲醇蒸气的浓度,CO的转化率增大 |
| B.平衡常数K(75℃)>K(85℃) |
C.b点反应速率 |
| D.生产时反应温度控制在80~85℃为宜 |
您最近一年使用:0次
名校
3 . 向1L的密闭容器中加入1molX、0.3molZ和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间的变化如图甲所示。图乙为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是
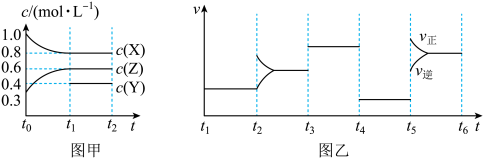

| A.Y的起始物质的量为0.5mol |
B.该反应的化学方程式为2X(g)+Y(g) 3Z(g) ΔH<0 3Z(g) ΔH<0 |
| C.若t0=0,t1=10s,则t0~t1阶段的平均反应速率为v(Z)=0.03mol·L-1·s-1 |
| D.反应物X的转化率t6点比t3点高 |
您最近一年使用:0次
2021-10-05更新
|
1056次组卷
|
21卷引用:2017届天津市五区县高三上学期期末考试化学试卷
2017届天津市五区县高三上学期期末考试化学试卷2017届天津市红桥区高三上学期期末考试(下学期开学考试)化学试卷安徽省江淮名校2017-2018学年高二期中考试化学试题天津市五区县2017届高三上学期期末考试化学试卷安徽省肥东高级中学2017-2018学年高二下学期第二学段考试化学试题广东省揭西县河婆中学2018-2019学年高二上学期期中考试化学试题贵州省铜仁第一中学2020届高三上学期第二次月考化学试题湖北省宜昌市葛洲坝中学2019-2020学年高二上学期期中考试化学试题安徽省枞阳县浮山中学2019-2020学年高二上学期期中考试化学试题云南普洱市景东县第一中学2019-2020学年高二下学期期中考试化学试题河南省南阳市2018-2019学年高二下学期期终质量评估化学试题内蒙古自治区呼和浩特市第二中学2019-2020学年高二上学期月考化学试题重庆第二外国语学校2020-2021学年度高三下学期高三5月诊断考试化学试题(已下线)考向21 化学反应速率及影响因素-备战2022年高考化学一轮复习考点微专题江西省吉安市第一中学2021-2022学年度高二上学期开学考试化学试题河南省新蔡县第一高级中学2021-2022学年高二上学期9月月考化学试题黑龙江省双鸭山市第一中学2021-2022学年高二上学期期中考试化学试题四川师范大学附属中学2022-2023学年高二上学期期中考试化学试题甘肃省徽县第一中学2021-2022学年高二上学期11月月考化学试题广东省广州市铁一中学2023-2024学年高二上学期10月月考化学试题湖南省长沙市雅礼中学2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
4 . I.含硫化合物及含碳化合物是实验室和工业上的常用化学品。请回答:
(1)实验室可用铜与浓硫酸反应制备少量 :
: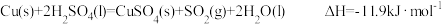 。判断该反应的自发性并说明理由
。判断该反应的自发性并说明理由_______ 。
(2)接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
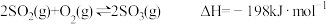
①该反应450℃时的平衡常数_____ 500℃时的平衡常数(填“大于”、“小于”或“等于”)。
②下列描述中能表明该反应已达平衡状态的是________
A.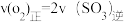
B.容器中气体的平均分子量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
③在一个固定容积为5L的密闭容器中充入0.20 mol 和0.10mol
和0.10mol ,半分钟后达到平衡,测得容器中含
,半分钟后达到平衡,测得容器中含 0.18mol;若继续通入0.20mol
0.18mol;若继续通入0.20mol 和0.10mol
和0.10mol ,则平衡
,则平衡______ 移动(填“向正反应方向”、“向逆反应方向” 或“不”)。
(3)工业上主要采用接触法由含硫矿石制备硫酸。下列说法正确的是_______。
Ⅱ.工业上,常采用氧化还原方法处理尾气中的CO。沥青混凝土可作为反应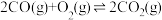 的催化剂。图中表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土(
的催化剂。图中表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土( 型、
型、 型)催化时,CO的转化率与温度的关系。
型)催化时,CO的转化率与温度的关系。
(4)在a、b、c、d四点中,未达到平衡状态的是_______ (填序号)。
(5)下列关于图示的说法正确的是_______(填序号)。
(1)实验室可用铜与浓硫酸反应制备少量
 :
: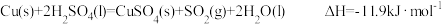 。判断该反应的自发性并说明理由
。判断该反应的自发性并说明理由(2)接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
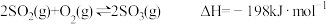
①该反应450℃时的平衡常数
②下列描述中能表明该反应已达平衡状态的是
A.
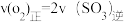
B.容器中气体的平均分子量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
③在一个固定容积为5L的密闭容器中充入0.20 mol
 和0.10mol
和0.10mol ,半分钟后达到平衡,测得容器中含
,半分钟后达到平衡,测得容器中含 0.18mol;若继续通入0.20mol
0.18mol;若继续通入0.20mol 和0.10mol
和0.10mol ,则平衡
,则平衡(3)工业上主要采用接触法由含硫矿石制备硫酸。下列说法正确的是_______。
A.须采用高温高压的反应条件使 氧化为 氧化为 |
| B.进入接触室之前的气流无需净化处理 |
| C.通入过量的空气可以提高含硫矿石和SO2的转化率 |
| D.在吸收塔中宜采用水或稀硫酸吸收SO3以提高吸收速率 |
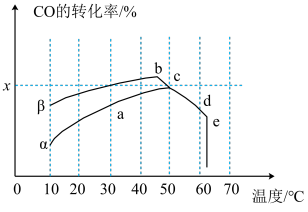
Ⅱ.工业上,常采用氧化还原方法处理尾气中的CO。沥青混凝土可作为反应
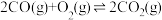 的催化剂。图中表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土(
的催化剂。图中表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土( 型、
型、 型)催化时,CO的转化率与温度的关系。
型)催化时,CO的转化率与温度的关系。
(4)在a、b、c、d四点中,未达到平衡状态的是
(5)下列关于图示的说法正确的是_______(填序号)。
| A.e点转化率出现突变的原因可能是温度升高后催化剂失去活性 |
| B.b点时CO与O2分子之间发生有效碰撞的几率在整个实验过程中最高 |
C.在均未达到平衡状态时,同温下 型沥青混凝土中CO转化速率比 型沥青混凝土中CO转化速率比 型的要大 型的要大 |
D.CO转化反应的平衡常数 |
您最近一年使用:0次
5 . 某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g) ΔH<0。图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
2Z(g) ΔH<0。图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
 2Z(g) ΔH<0。图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
2Z(g) ΔH<0。图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是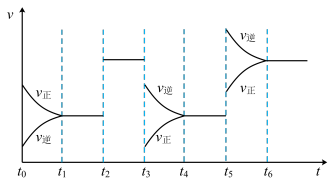
| A.t2时加入了催化剂 | B.t3时降低了温度 |
| C.t5时增大了压强 | D.t3~t4时间内转化率最低 |
您最近一年使用:0次
名校
6 . 乙酸甲酯转化为乙醇的反应原理为CH3COOCH3(g)+2H2(g)⇌C2H5OH(g)+CH3OH(g) ΔH<0。该反应中反应速率随时间变化的关系如图所示,t1、t3、t4时刻分别改变某一外界条件。下列说法错误的是
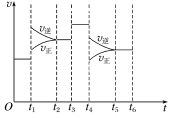

| A.t1时升高温度 |
| B.t3时加入催化剂 |
| C.t4时增大反应容器的容积,使体系压强减小 |
| D.在反应保持化学平衡的时间段中,C2H5OH的体积分数最小的时间段是t2~t3 |
您最近一年使用:0次
2022-10-13更新
|
513次组卷
|
7卷引用:北京市陈经纶中学2022-2023学年高二10月月考化学试题
解题方法
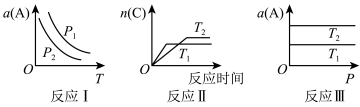
7 . 在其他条件不变时,只改变某一条件,化学反应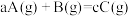 的平衡的变化图象如图,图中p表示压强,T表示温度,n表示物质的量,a表示平衡转化率,据此分析下列说法不正确的是
的平衡的变化图象如图,图中p表示压强,T表示温度,n表示物质的量,a表示平衡转化率,据此分析下列说法不正确的是
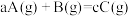 的平衡的变化图象如图,图中p表示压强,T表示温度,n表示物质的量,a表示平衡转化率,据此分析下列说法不正确的是
的平衡的变化图象如图,图中p表示压强,T表示温度,n表示物质的量,a表示平衡转化率,据此分析下列说法不正确的是
| A.由图象Ⅰ,说明正反应为放热反应 |
B.在图象Ⅰ中,若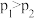 ,则此反应的 ,则此反应的 |
C.由图象Ⅱ,说明温度 |
D.由图象Ⅲ,说明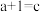 |
您最近一年使用:0次
名校
8 . 根据相应的图象,判断下列相关说法正确的是


| A.密闭容器中反应达到平衡,t0时改变某一条件有如图甲变化所示,则改变的条件只能是加入催化剂 |
| B.反应达到平衡时外界条件对平衡影响关系如图乙所示,则正反应为放热反应,且a>b |
| C.如图丙所示,在恒容的密闭容器中,反应达到平衡后,改变NO的物质的量,平衡常数的变化趋势如图丙 |
| D.反应速率和反应条件变化关系如图丁所示,则该反应的正反应为放热反应,且A、B、C、D均为气体 |
您最近一年使用:0次
2021高二·全国·专题练习
名校
解题方法
9 . 向绝热恒容密闭容器中通入1 mol SO2和1 mol NO2,发生反应SO2(g)+NO2(g) SO3(g)+NO(g),正反应速率随时间变化如图所示。下列有关说法不正确的是
SO3(g)+NO(g),正反应速率随时间变化如图所示。下列有关说法不正确的是

 SO3(g)+NO(g),正反应速率随时间变化如图所示。下列有关说法不正确的是
SO3(g)+NO(g),正反应速率随时间变化如图所示。下列有关说法不正确的是
| A.生成物的总能量低于反应物的总能量 |
| B.c点容器内气体颜色不再改变 |
| C.当Δt1=Δt2时,SO2的转化率:a~b段小于b~c段 |
| D.c~d段,反应物浓度减小是影响正反应速率下降的主要因素 |
您最近一年使用:0次
2021-08-21更新
|
592次组卷
|
6卷引用:专题2.2.3 影响化学平衡的因素(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)
(已下线)专题2.2.3 影响化学平衡的因素(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)福建省武平县第一中学2021-2022学年高二上学期第一次月考化学试题湖北省武汉市蔡甸区汉阳一中2021-2022学年高二上学期9月月考化学试题山西省运城市芮城中学2021-2022学年高二上学期阶段性月考化学试题福建省龙岩第一中学2021-2022学年高二上学期期中考试化学试题广东省东莞市东莞中学松山湖学校2023-2024学年高二上学期期中考试化学试题
名校
10 . 某密闭容器中充入等物质的量的A和B,一定温度下发生反应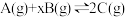 ,达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
,达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
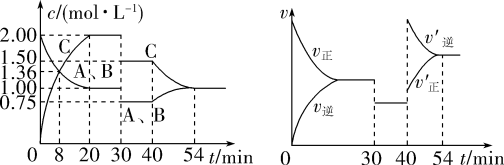
下列说法中不正确 的是
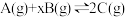 ,达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
,达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
下列说法中
| A.30min~40min间该反应使用了催化剂 |
| B.反应方程式中的x=1 |
| C.正反应为放热反应 |
| D.前8minA的平均反应速率为0.08mol·L-1·min-1 |
您最近一年使用:0次



