29. 实验室中有一瓶未知浓度的醋酸,为了补齐这瓶试剂的标签,某学生用0.1000 mol•L
-1的KOH标准溶液滴定对此进行滴定,其操作分解为如下几步:
A.移取20 mL待测醋酸注入洁净的锥形瓶,并加入2~3滴______(指示剂)
B.用标准溶液润洗滴定管2~3次
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准KOH溶液注入碱式滴定管至“0”刻度以上1~2cm
E.调节液面至“0”或“0”以下某一刻度,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度
G.用蒸馏水洗涤滴定管2~3次
就此实验完成填空:
(1)请补齐步骤中缺失的部分,并对操作步骤进行正确的排序(用序号字母填写)
_____。
G→____→____→____→____→A→F
_____。
(2)在滴定过程中,左手控制碱式滴定管,右手摇动锥形瓶,眼睛应该注视
______。
(3)排出碱式滴定管中的气泡应采用操作
_____(填“甲”、“乙”或“丙”),然后轻轻挤压玻璃球使尖嘴部分充满碱液。

(4)判断到达滴定终点的现象是
______。
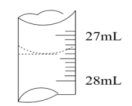
(5)若甲学生在实验过程中,记录滴定前滴定管内液面读数为2.50mL,滴定后液面如图,则此时消耗标准溶液的体积为
______。
(6)乙学生做了三组平行实验,数据记录如表:选取下述合理数据,计算出待测溶液的物质的量浓度为
______。(保留四位有效数字)
| 实验序号 | 待测醋酸溶液的体积/mL | 0.1000 mol•L-1的KOH溶液的体积/mL |
| 滴定前刻度 | 滴定后刻度 |
| 1 | 25.00 |  | 26.29 |
| 2 | 25.00 | 1.00 | 31.00 |
| 3 | 25.00 | 1.00 | 27.31 |
(7)下列操作中可能使所测醋酸溶液浓度偏大的是
______。
| A.碱式滴定管未用标准溶液润洗,直接装入标准溶液 |
| B.碱式滴定管滴定前有气泡,滴定后气泡消失 |
| C.滴定前盛放醋酸溶液的锥形瓶用蒸馏水洗净后未干燥 |
| D.读取氢氧化钾体积开始时仰视读数,滴定结束后俯视读数 |