海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
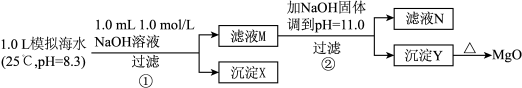
注:溶液中某种离子的浓度小于1.0×10-5mol/L,可认为该离子不存在。实验过程中,假设溶液体积不变。
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;Ksp[Ca(OH)2]=4.68×10-6;Ksp[Mg(OH)2]=5.61×10-12。请回答下列问题:
(1)沉淀物X为______ 。
(2)滤液N中Ca2+浓度为______ 。
(3)加NaOH固体调整pH=12.5是否可行______ (填“是”“否”);原因是______ 。

| 模拟海水中的离子浓度/(mol/L) | Na+ | Mg2+ | Ca2+ | Cl- | HCO |
| 0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;Ksp[Ca(OH)2]=4.68×10-6;Ksp[Mg(OH)2]=5.61×10-12。请回答下列问题:
(1)沉淀物X为
(2)滤液N中Ca2+浓度为
(3)加NaOH固体调整pH=12.5是否可行
更新时间:2023-01-25 17:59:21
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】铅及其化合物有着优异的性能和广泛的应用。工业上利用铅浮渣(主要成分是PbO、Pb,还含有少量的Ag、CaO)制备硫酸铅。制备流程图如下
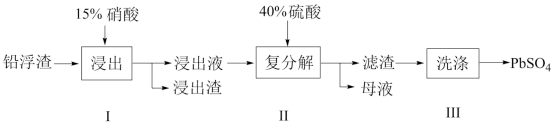
已知:Ksp(PbSO4)=1.6×10-8 Ksp(CaSO4)=4.9×10-5
(1)步骤I有NO产生浸出液中含量最多的金属阳离子为Pb2+,写出Pb参加反应的化学方程式___________________________ ,为防止Ag被溶解进入溶液,步骤I操作时应注意_______________________ 。
(2)粗PbSO4产品含有的杂质是____________ ;要得到纯净的PbSO4,需要用试剂进行多次洗涤,再用蒸馏水洗涤。最好选用的试剂是_________________ 。
A.稀硫酸 B.稀盐酸 C.硝酸铅溶液 D.酒精
(3)母液可循环利用的物质是HNO3,若母液中残留的 过多,循环利用时可能出现的问题是
过多,循环利用时可能出现的问题是______________________________ 。
(4)若将步骤Ⅱ中的Pb2+完全沉淀,则溶液中的c( )至少为
)至少为___________ mol/L。
(5)(CH3COO)2Pb是皮毛行业可溶于水的染色助剂,可用PbSO4与CH3COONH4反应制备,写出该反应的离子方程式_______________________ 。
(6)铅蓄电池是电压稳定、使用方便的二次电池。PbSO4在其中扮演了重要角色,写出铅蓄电池充电时阳极的电极反应_______________________ 。

已知:Ksp(PbSO4)=1.6×10-8 Ksp(CaSO4)=4.9×10-5
(1)步骤I有NO产生浸出液中含量最多的金属阳离子为Pb2+,写出Pb参加反应的化学方程式
(2)粗PbSO4产品含有的杂质是
A.稀硫酸 B.稀盐酸 C.硝酸铅溶液 D.酒精
(3)母液可循环利用的物质是HNO3,若母液中残留的
 过多,循环利用时可能出现的问题是
过多,循环利用时可能出现的问题是(4)若将步骤Ⅱ中的Pb2+完全沉淀,则溶液中的c(
 )至少为
)至少为(5)(CH3COO)2Pb是皮毛行业可溶于水的染色助剂,可用PbSO4与CH3COONH4反应制备,写出该反应的离子方程式
(6)铅蓄电池是电压稳定、使用方便的二次电池。PbSO4在其中扮演了重要角色,写出铅蓄电池充电时阳极的电极反应
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】 和
和 都是锂离子电池的电极材料,可利用钛铁矿(主要成分为
都是锂离子电池的电极材料,可利用钛铁矿(主要成分为 ,还含有少量MgO、
,还含有少量MgO、 等杂质)来制备。工艺流程如下;
等杂质)来制备。工艺流程如下;
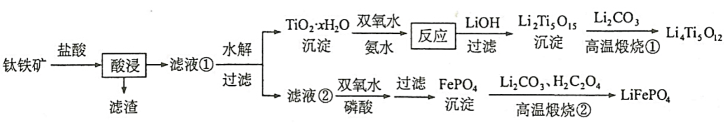
回答下列问题:
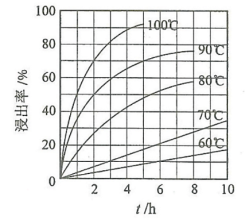
(1)“酸浸”实验中,铁的浸出率结果如图所示。由图可知,当铁的浸出率为80%时,所采用的实验条件为______ 。
(2)“酸浸”后,钛主要以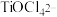 形式存在,写出相应反应的离子方程式
形式存在,写出相应反应的离子方程式______ 。
(3) 沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
分析40℃时 转化率最高的原因
转化率最高的原因______ 。
(4)若“滤液②”中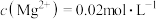 ,加入双氧水和磷酸(设溶液体积增加1倍),使
,加入双氧水和磷酸(设溶液体积增加1倍),使 恰好沉淀完全即溶液中
恰好沉淀完全即溶液中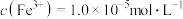 ,此时是否有
,此时是否有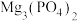 沉淀生成?
沉淀生成?______ (列式计算说明理由)[已知 、
、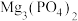 的
的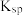 分别为
分别为 、
、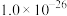 ].
].
(5)写出“高温煅烧②”中由 制备
制备 的化学方程式
的化学方程式______ 。
(6)一种钛酸锂二次电池原理如图,放电时 由N极层状材料中脱出经由电解质嵌入M极层状材料中,充电时N极电极反应方程式为
由N极层状材料中脱出经由电解质嵌入M极层状材料中,充电时N极电极反应方程式为______ ,放电时M极每增重7g,负载中转移电子数为______ 。
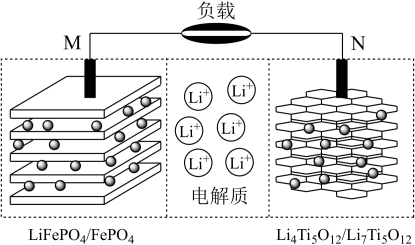
 和
和 都是锂离子电池的电极材料,可利用钛铁矿(主要成分为
都是锂离子电池的电极材料,可利用钛铁矿(主要成分为 ,还含有少量MgO、
,还含有少量MgO、 等杂质)来制备。工艺流程如下;
等杂质)来制备。工艺流程如下;
回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如图所示。由图可知,当铁的浸出率为80%时,所采用的实验条件为

(2)“酸浸”后,钛主要以
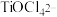 形式存在,写出相应反应的离子方程式
形式存在,写出相应反应的离子方程式(3)
 沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
沉淀与双氧水、氨水反应40min所得实验结果如下表所示:| 温度/℃ | 30 | 35 | 40 | 45 | 50 |
 转化率/% 转化率/% | 92 | 95 | 97 | 93 | 88 |
 转化率最高的原因
转化率最高的原因(4)若“滤液②”中
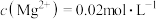 ,加入双氧水和磷酸(设溶液体积增加1倍),使
,加入双氧水和磷酸(设溶液体积增加1倍),使 恰好沉淀完全即溶液中
恰好沉淀完全即溶液中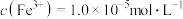 ,此时是否有
,此时是否有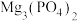 沉淀生成?
沉淀生成? 、
、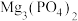 的
的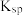 分别为
分别为 、
、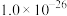 ].
].(5)写出“高温煅烧②”中由
 制备
制备 的化学方程式
的化学方程式(6)一种钛酸锂二次电池原理如图,放电时
 由N极层状材料中脱出经由电解质嵌入M极层状材料中,充电时N极电极反应方程式为
由N极层状材料中脱出经由电解质嵌入M极层状材料中,充电时N极电极反应方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示。请回答下列问题:
(1)A点表示Ag2SO4是_______ (填“饱和”或“不饱和”)溶液。B点对应的Ksp_______ (填“>”“<”或“=”)C点对应的Ksp。

(2)现将足量的Ag2SO4分别放入下面三种溶液中:
a.40mL0.01mol·L-1K2SO4溶液 B.10mL蒸馏水 C.10mL0.02mol·L-1H2SO4溶液
则Ag2SO4的溶解程度由大到小的排列顺序为_______ (填字母)。
(3)在25℃下,向浓度均为0.1mol/L的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成_______ 沉淀(填化学式),生成该沉淀的离子方程式为_______ 。[已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20]
(4)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,(Br-):(Cl-)=_______ 。[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
(1)A点表示Ag2SO4是

(2)现将足量的Ag2SO4分别放入下面三种溶液中:
a.40mL0.01mol·L-1K2SO4溶液 B.10mL蒸馏水 C.10mL0.02mol·L-1H2SO4溶液
则Ag2SO4的溶解程度由大到小的排列顺序为
(3)在25℃下,向浓度均为0.1mol/L的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成
(4)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,(Br-):(Cl-)=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】钼酸钠晶体(Na2MoO4·2H2O)是一种金属腐蚀抑制剂。下图是利用钼精矿(主要成分是MoS2,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。

回答下列问题:
(1)Na2MoO4·2H2O中钼元素的化合价是___________ ;在焙烧炉中,空气从炉底进入,矿石经粉碎后从炉项进入,这样处理的目的是___________ 。
(2)“焙烧”时MoS2转化为MoO3,写出该反应的化学方程式:___________ ,反应中氧化产物是___________ (填化学式)。
(3)“浸取”时含钼化合物发生反应的离子方程式为___________ ;“结晶”前需向滤液中加入Ba(OH)2固体以除去 。若滤液中c(MoO
。若滤液中c(MoO )=0.40mol/L,c(
)=0.40mol/L,c( )=0.10mol/L,当BaMoO4开始沉淀时,
)=0.10mol/L,当BaMoO4开始沉淀时, 的去除率是
的去除率是___________ %[已知:Ksp(ВaCO3)=1×10-9、Ksp(BaMoO4)=4.0×10-8]。
(4)“分析纯”的钼酸钠常用钼酸铵[(NH4)2MoO4]和氢氧化钠反应来制取,若将该反应产生的气体与流程中所产生的气体一起通入水中,得到正盐的化学式为___________ 。

回答下列问题:
(1)Na2MoO4·2H2O中钼元素的化合价是
(2)“焙烧”时MoS2转化为MoO3,写出该反应的化学方程式:
(3)“浸取”时含钼化合物发生反应的离子方程式为
 。若滤液中c(MoO
。若滤液中c(MoO )=0.40mol/L,c(
)=0.40mol/L,c( )=0.10mol/L,当BaMoO4开始沉淀时,
)=0.10mol/L,当BaMoO4开始沉淀时, 的去除率是
的去除率是(4)“分析纯”的钼酸钠常用钼酸铵[(NH4)2MoO4]和氢氧化钠反应来制取,若将该反应产生的气体与流程中所产生的气体一起通入水中,得到正盐的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】SCR催化剂是工业上广泛应用的燃煤烟气脱硝催化剂,其主要成分为WO3、TiO2、V2O5,以及少量SiO2、CaO、Al2O3、Fe2O3等。一种从废SCR催化剂中回收钨的工艺如下:

回答下列问题
(1)“酸浸还原”中V2O5转化成可溶于水的VOC2O4,VOC2O4中V的化合价是___________ ,该反应的化学方程式为___________ 。可用浓盐酸代替草酸,但缺点是___________ 。
(2)“碱浸”时WO3转化为WO 的离子方程式为
的离子方程式为___________ 。
(3)“试剂a”可选用___________ (选填“盐酸”、“氢氧化钠”或“氨水”)。“滤渣”的主要成分是___________ 。
(4)常温下Ksp[Ca(OH)2]=5.5×10-6,Ksp(CaWO4)=8.7×10-9。“沉钨”过程中不断加入石灰乳,当测得“滤液”中pH=13时,c(WO )为
)为___________ mol·L-l(保留2位有效数字)
(5)“熔融电解”过程中阴极反应为WO +6e-=W+4O2-。电解过程中石墨阳极有损耗并有气体产生,用反应方程式解释该现象
+6e-=W+4O2-。电解过程中石墨阳极有损耗并有气体产生,用反应方程式解释该现象___________ 。

回答下列问题
(1)“酸浸还原”中V2O5转化成可溶于水的VOC2O4,VOC2O4中V的化合价是
(2)“碱浸”时WO3转化为WO
 的离子方程式为
的离子方程式为(3)“试剂a”可选用
(4)常温下Ksp[Ca(OH)2]=5.5×10-6,Ksp(CaWO4)=8.7×10-9。“沉钨”过程中不断加入石灰乳,当测得“滤液”中pH=13时,c(WO
 )为
)为(5)“熔融电解”过程中阴极反应为WO
 +6e-=W+4O2-。电解过程中石墨阳极有损耗并有气体产生,用反应方程式解释该现象
+6e-=W+4O2-。电解过程中石墨阳极有损耗并有气体产生,用反应方程式解释该现象
您最近一年使用:0次
【推荐3】氧化锌是一种常用添加剂,广泛应用于塑料、合成橡胶、电池等产品的制造。一种利用氧化锌烟灰制备活性氧化锌的工艺流程如下:
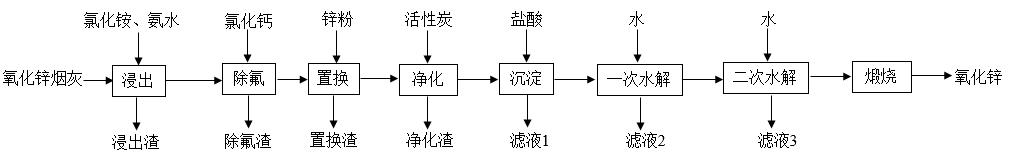
已知:I.氧化锌烟灰的主要化学组成如下:
Ⅱ.浸出”时,大部分锌元素以Zn(NH3)42+形式进入溶液,同时部分Pb、Cu、F元素也进入溶液中。
(1)氨的电子式______________________ 。
(2)“浸出”时,氧化锌发生反应的离子方程式为_________________________________ ;“浸出”时温度不宜过高,其原因为____________________________________________ 。
(3)若“浸出”后,所得溶液中c(F-)=0.02mol/L,向其中加入等体积的氯化钙溶液(忽略溶液体积变化),使F-沉淀完全即溶液中c(F-)<10-5mol/L,则所加氯化钙溶液的浓度度最小为___________ 。已知:Ksp(CaF2)=3.45×10-11
(4)“置换”时,所得置换渣中除了含Zn外,还含有___________ ;“净化”时,利用活性炭___________ 性,除去溶液中残留的有机物。
(5)“沉淀”时,可得到滤渣Zn(NH3)2Cl2。所加盐酸过量时,会导致沉淀部分溶解甚至消失,其化学方程式为____________________________________________ 。
(6)“一次水解”时,产物为Zn(OH)xCly。取10.64g该水解产物,经二次水解、煅烧后,可得活性氧化锌8.1g(假设各步均转化完全)。则一次水解产物的化学式为___________ 。

已知:I.氧化锌烟灰的主要化学组成如下:
| 元素组成 | Zn | Pb | Cu | Cl | F |
| 质量分数% | 59.78 | 9.07 | 0.30 | 2.24 | 1.80 |
Ⅱ.浸出”时,大部分锌元素以Zn(NH3)42+形式进入溶液,同时部分Pb、Cu、F元素也进入溶液中。
(1)氨的电子式
(2)“浸出”时,氧化锌发生反应的离子方程式为
(3)若“浸出”后,所得溶液中c(F-)=0.02mol/L,向其中加入等体积的氯化钙溶液(忽略溶液体积变化),使F-沉淀完全即溶液中c(F-)<10-5mol/L,则所加氯化钙溶液的浓度度最小为
(4)“置换”时,所得置换渣中除了含Zn外,还含有
(5)“沉淀”时,可得到滤渣Zn(NH3)2Cl2。所加盐酸过量时,会导致沉淀部分溶解甚至消失,其化学方程式为
(6)“一次水解”时,产物为Zn(OH)xCly。取10.64g该水解产物,经二次水解、煅烧后,可得活性氧化锌8.1g(假设各步均转化完全)。则一次水解产物的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】ClO2作为一种广谱型的消毒剂,将逐渐用来替代Cl2成为自来水的消毒剂。已知ClO2是一种易溶于水而难溶于有机溶剂的气体,实验室制备ClO2的原理是用亚氯酸钠固体与氯气反应:2NaClO2+Cl2=2ClO2+2NaCl。下图是实验室中制取纯净、干燥的氯气并用它制取和收集一定量纯净的ClO2的装置(某些夹持装置和垫持用品省略)。其中E中盛有CCl4液体(用于除去ClO2中未反应的Cl2)
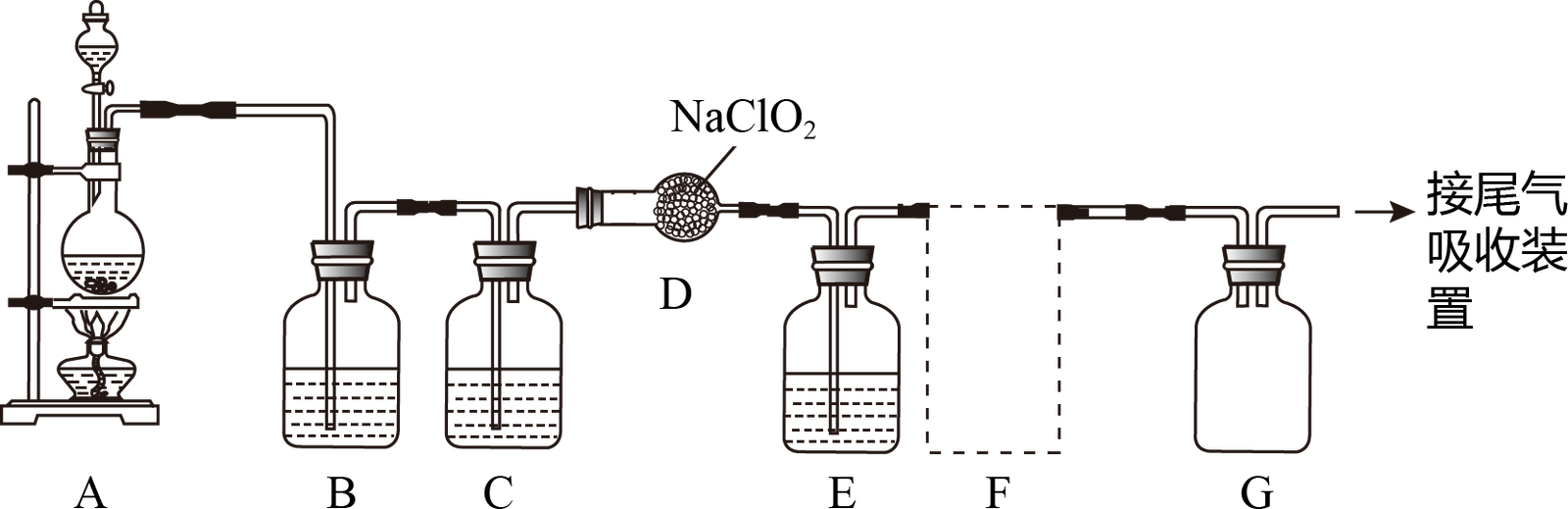
(1)NaClO2中氯元素的化合价是_______
(2)装置A中烧瓶内发生反应的化学方程式 为_______ ;
(3)B装置中所盛试剂是_______ ;C装置所盛试剂的作用是_______ ;
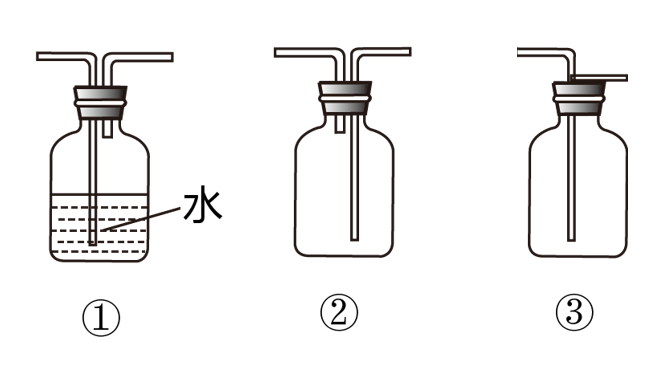
(4)F为ClO2的收集装置,下列装置中最合适的ClO2收集装置是_______ (选填:①或②或③)

(1)NaClO2中氯元素的化合价是
(2)装置A中烧瓶内发生反应的
(3)B装置中所盛试剂是
(4)F为ClO2的收集装置,下列装置中最合适的ClO2收集装置是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氧化钪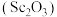 可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含
可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含 、
、 等离子)为原料制备氧化钪
等离子)为原料制备氧化钪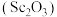 的一种流程如下图。
的一种流程如下图。
(1)基态钪原子的价层电子排布式为___________ 。
(2)“萃取”时,钛白工业废酸中加入 可降低钛的萃取率,可能是生成了难萃取的
可降低钛的萃取率,可能是生成了难萃取的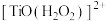 ,其中
,其中 的作用是
的作用是___________ (填标号)。
A.作氧化剂 B.作还原剂 C.提供配体
(3)“洗涤”时,洗涤剂是用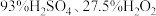 和
和 三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将A试剂沿烧杯内壁缓慢注入B试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入C试剂中,并不断搅拌,则A、C分别对应上述试剂中的
三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将A试剂沿烧杯内壁缓慢注入B试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入C试剂中,并不断搅拌,则A、C分别对应上述试剂中的___________ 、___________ 。
(4)萃取剂萃取 的原理为
的原理为 (
(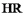 代表萃取剂)。在“反萃取”中,加入
代表萃取剂)。在“反萃取”中,加入 溶液后生成
溶液后生成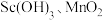 等物质,其中生成含
等物质,其中生成含 化合物的化学方程式为
化合物的化学方程式为___________ 。 时,经“反萃取”后所得滤液的
时,经“反萃取”后所得滤液的 ,则残留的
,则残留的 浓度为
浓度为___________  (已知:
(已知: 时,
时, 。
。
(5)“沉钪”时用到草酸。已知草酸的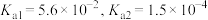 ,则在
,则在 时,
时, 的草酸溶液中
的草酸溶液中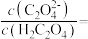
___________ 。
(6)在空气中焙烧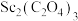 的化学方程式为
的化学方程式为___________ 。
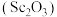 可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含
可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含 、
、 等离子)为原料制备氧化钪
等离子)为原料制备氧化钪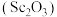 的一种流程如下图。
的一种流程如下图。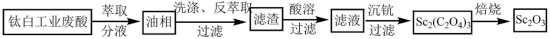
(1)基态钪原子的价层电子排布式为
(2)“萃取”时,钛白工业废酸中加入
 可降低钛的萃取率,可能是生成了难萃取的
可降低钛的萃取率,可能是生成了难萃取的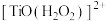 ,其中
,其中 的作用是
的作用是A.作氧化剂 B.作还原剂 C.提供配体
(3)“洗涤”时,洗涤剂是用
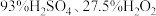 和
和 三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将A试剂沿烧杯内壁缓慢注入B试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入C试剂中,并不断搅拌,则A、C分别对应上述试剂中的
三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将A试剂沿烧杯内壁缓慢注入B试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入C试剂中,并不断搅拌,则A、C分别对应上述试剂中的(4)萃取剂萃取
 的原理为
的原理为 (
(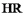 代表萃取剂)。在“反萃取”中,加入
代表萃取剂)。在“反萃取”中,加入 溶液后生成
溶液后生成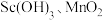 等物质,其中生成含
等物质,其中生成含 化合物的化学方程式为
化合物的化学方程式为 时,经“反萃取”后所得滤液的
时,经“反萃取”后所得滤液的 ,则残留的
,则残留的 浓度为
浓度为 (已知:
(已知: 时,
时, 。
。(5)“沉钪”时用到草酸。已知草酸的
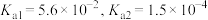 ,则在
,则在 时,
时, 的草酸溶液中
的草酸溶液中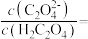
(6)在空气中焙烧
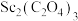 的化学方程式为
的化学方程式为
您最近一年使用:0次
【推荐3】从高碳钼精矿(主要含有MoS2、NiS、CaCO3和石墨)中提取镍和钼的化合物,其主要工艺流程如图所示:
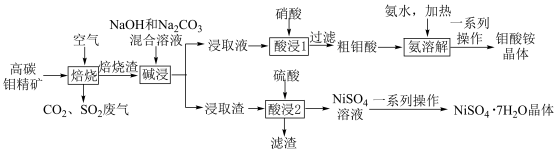
已知:焙烧渣的主要成分为MoO3、CaMoO4、NiMoO4、CaSO4。回答下列问题:
(1)Mo与Cr同族,原子序数为42,则基态Mo原子的价电子排布式为___________ 。
(2)“焙烧”过程中 转化为
转化为 的化学方程式为
的化学方程式为___________ 。
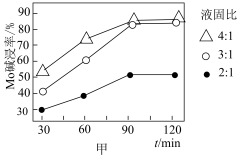
(3)“碱浸”过程中,液固比(NaOH和 混合溶液的体积与焙烧渣的质量比)与碱浸率之间的关系如图甲所示,则“碱浸”时应选用的最佳液固比为
混合溶液的体积与焙烧渣的质量比)与碱浸率之间的关系如图甲所示,则“碱浸”时应选用的最佳液固比为___________ 。
(4)已知常温下相关物质的Ksp如下表,则浸取渣的主要成分是___________ (填化学式)。
(5)“氨溶解”过程中需要控制温度在70℃左右,温度不宜过高的原因是___________ 。
(6)取一定量的NiSO4·7H2O样品进行热重分析,样品在受热过程中的固体残留率随温度变化的曲线如图乙所示。
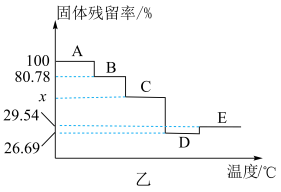
①已知C时失掉全部结晶水,则C时的固体残留率为___________ %(保留两位小数),E时残留固体的化学式为___________ 。
②镍可以形成多种氧化物,其中一种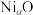 晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0.88,且晶体中的Ni分别为
晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0.88,且晶体中的Ni分别为 、
、 ,则晶体中
,则晶体中 与
与 的最简整数比为
的最简整数比为___________ ,晶胞参数为428pm,则晶体密度为___________  (
( 表示阿伏加德罗常数的值,列出计算式即可)。
表示阿伏加德罗常数的值,列出计算式即可)。

已知:焙烧渣的主要成分为MoO3、CaMoO4、NiMoO4、CaSO4。回答下列问题:
(1)Mo与Cr同族,原子序数为42,则基态Mo原子的价电子排布式为
(2)“焙烧”过程中
 转化为
转化为 的化学方程式为
的化学方程式为(3)“碱浸”过程中,液固比(NaOH和
 混合溶液的体积与焙烧渣的质量比)与碱浸率之间的关系如图甲所示,则“碱浸”时应选用的最佳液固比为
混合溶液的体积与焙烧渣的质量比)与碱浸率之间的关系如图甲所示,则“碱浸”时应选用的最佳液固比为
(4)已知常温下相关物质的Ksp如下表,则浸取渣的主要成分是
| 物质 | 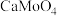 |  |  |  |
 | 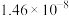 | 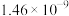 | 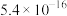 |  |
(5)“氨溶解”过程中需要控制温度在70℃左右,温度不宜过高的原因是
(6)取一定量的NiSO4·7H2O样品进行热重分析,样品在受热过程中的固体残留率随温度变化的曲线如图乙所示。

①已知C时失掉全部结晶水,则C时的固体残留率为
②镍可以形成多种氧化物,其中一种
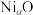 晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0.88,且晶体中的Ni分别为
晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0.88,且晶体中的Ni分别为 、
、 ,则晶体中
,则晶体中 与
与 的最简整数比为
的最简整数比为 (
( 表示阿伏加德罗常数的值,列出计算式即可)。
表示阿伏加德罗常数的值,列出计算式即可)。
您最近一年使用:0次



