1 . 铜及其化合物广泛应用于工农业生产及生活中。
(1)用铜作阳极,钛片作阴极,电解一定浓度的NaCl和NaOH的混合溶液可得到 ,阳极及溶液中物质的有关转化如图所示,阳极的电极反应为
,阳极及溶液中物质的有关转化如图所示,阳极的电极反应为___________ ,每生成14.4g  转移电子的物质的量为
转移电子的物质的量为___________ mol。 ,CuCl水解的反应为
,CuCl水解的反应为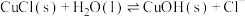
 。该反应的平衡常数K与此温度下
。该反应的平衡常数K与此温度下 、
、 (CuOH)、
(CuOH)、 (CuCl)的关系为
(CuCl)的关系为___________ 。
(3)不同电压下,Cu/ /CuO复合电极在0.1
/CuO复合电极在0.1 的
的 溶液中的光电催化还原
溶液中的光电催化还原 生成甲醇的装置如图2所示,不同电压下产物甲醇的产量随时间的变化如图3所示。
生成甲醇的装置如图2所示,不同电压下产物甲醇的产量随时间的变化如图3所示。 /CuO)复合电极是
/CuO)复合电极是___________ (填“阴极”或“阳极”),光电催化还原 生成甲醇的最佳电压是
生成甲醇的最佳电压是___________ 。
(1)用铜作阳极,钛片作阴极,电解一定浓度的NaCl和NaOH的混合溶液可得到
 ,阳极及溶液中物质的有关转化如图所示,阳极的电极反应为
,阳极及溶液中物质的有关转化如图所示,阳极的电极反应为 转移电子的物质的量为
转移电子的物质的量为
 ,CuCl水解的反应为
,CuCl水解的反应为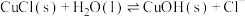
 。该反应的平衡常数K与此温度下
。该反应的平衡常数K与此温度下 、
、 (CuOH)、
(CuOH)、 (CuCl)的关系为
(CuCl)的关系为(3)不同电压下,Cu/
 /CuO复合电极在0.1
/CuO复合电极在0.1 的
的 溶液中的光电催化还原
溶液中的光电催化还原 生成甲醇的装置如图2所示,不同电压下产物甲醇的产量随时间的变化如图3所示。
生成甲醇的装置如图2所示,不同电压下产物甲醇的产量随时间的变化如图3所示。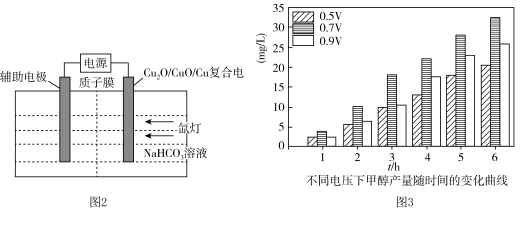
 /CuO)复合电极是
/CuO)复合电极是 生成甲醇的最佳电压是
生成甲醇的最佳电压是
您最近半年使用:0次
2 . 室温下,用含少量 的
的 溶液制备
溶液制备 的过程如图所示。已知:
的过程如图所示。已知: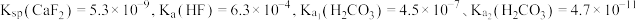 。下列说法正确的是
。下列说法正确的是

 的
的 溶液制备
溶液制备 的过程如图所示。已知:
的过程如图所示。已知: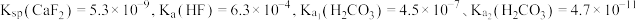 。下列说法正确的是
。下列说法正确的是
A.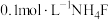 溶液中: 溶液中: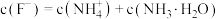 |
B.“除钙”得到的上层清液中: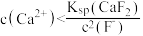 |
C. 的氨水 的氨水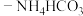 溶液: 溶液: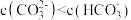 |
D.“沉铁”反应的离子方程式: |
您最近半年使用:0次
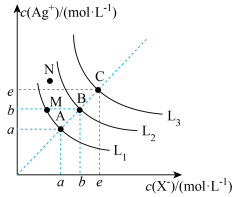
3 . 25℃时,卤化银(AgX,X=Cl、Br、I)在水中的沉淀溶解平衡曲线如图所示,AgCl、AgBr、AgI的 数据见下表(已知
数据见下表(已知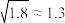 、
、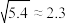 、
、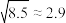 )。下列说法错误的是
)。下列说法错误的是
 数据见下表(已知
数据见下表(已知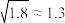 、
、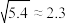 、
、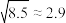 )。下列说法错误的是
)。下列说法错误的是| 化学式 |  |  |  |
| 溶度积 |  |  | 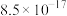 |

| A.N点为AgBr的饱和溶液 |
| B.L1、L2、L3分别为AgI、AgBr、AgCl的沉淀溶解平衡曲线 |
C.向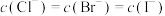 的混合溶液中滴入AgNO3溶液时,先生成AgI沉淀 的混合溶液中滴入AgNO3溶液时,先生成AgI沉淀 |
D.M点为AgX的饱和溶液,此时M点对应的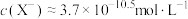 |
您最近半年使用:0次
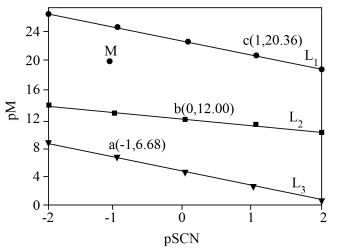
4 . 常温下,向含 、
、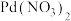 和
和 的溶液中滴加KSCN溶液,浊液中
的溶液中滴加KSCN溶液,浊液中 [
[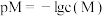 ,
,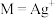 、
、 或
或 ]与
]与 的关系如图所示。已知:常温下,
的关系如图所示。已知:常温下,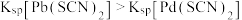 ,平衡常数K大于
,平衡常数K大于 时认为该反应能完全进行。
时认为该反应能完全进行。
下列叙述错误的是
 、
、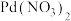 和
和 的溶液中滴加KSCN溶液,浊液中
的溶液中滴加KSCN溶液,浊液中 [
[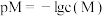 ,
,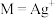 、
、 或
或 ]与
]与 的关系如图所示。已知:常温下,
的关系如图所示。已知:常温下,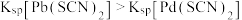 ,平衡常数K大于
,平衡常数K大于 时认为该反应能完全进行。
时认为该反应能完全进行。
下列叙述错误的是
A.直线 代表pPd与pSCN的关系 代表pPd与pSCN的关系 |
B.饱和AgSCN溶液中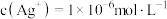 |
C.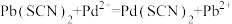 不可逆 不可逆 |
D.M点溶液可析出AgSCN和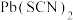 |
您最近半年使用:0次
2024-03-10更新
|
237次组卷
|
2卷引用:河南省创新发展联盟2023-2024学年高三下学期2月月考理综试题-高中化学
名校
解题方法
5 . 石灰水是实验室中常用的一种化学试剂,其在室温下的溶度积Ksp[Ca(OH)2]=4.7×10-6,在不同温度下的溶解度变化如图所示。下列有关饱和澄清石灰水的说法错误的是


A.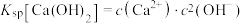 | B.加入少量 粉末,溶液变浑浊 粉末,溶液变浑浊 |
C.在空气中敞口久置只析出 | D.水浴加热,溶液变浑浊 |
您最近半年使用:0次
6 . 常温下,几种物质的溶度积常数见下表:
(1)写出 的溶度积常数表达式
的溶度积常数表达式___________ 。
(2)某酸性 溶液中含少到的
溶液中含少到的 ,为制得纯净的
,为制得纯净的 溶液,宜加入
溶液,宜加入___________ 调至溶液 ,使
,使 转化为
转化为 沉淀,此时溶液中的
沉淀,此时溶液中的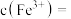
___________ 。
(3)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成 写出反应的离子方程式:
写出反应的离子方程式:___________ 。
(4)某工业废水中含有 等重金属离子,最适宜向此工业废水中加入过量的
等重金属离子,最适宜向此工业废水中加入过量的___________ (填字母)除去它们。
A.NaOH B. C.Na2S
C.Na2S
| 物质 |  |  |  |  |  |
 | 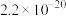 |  |  | 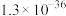 | 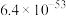 |
 的溶度积常数表达式
的溶度积常数表达式(2)某酸性
 溶液中含少到的
溶液中含少到的 ,为制得纯净的
,为制得纯净的 溶液,宜加入
溶液,宜加入 ,使
,使 转化为
转化为 沉淀,此时溶液中的
沉淀,此时溶液中的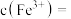
(3)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成
 写出反应的离子方程式:
写出反应的离子方程式:(4)某工业废水中含有
 等重金属离子,最适宜向此工业废水中加入过量的
等重金属离子,最适宜向此工业废水中加入过量的A.NaOH B.
 C.Na2S
C.Na2S
您最近半年使用:0次
7 . I.请写出下列基态粒子的简化电子排布式:
(1)S:___________ 。
(2)Cr:___________ 。
II.
(3)在一定温度下,Mg(OH)2在水中的沉淀溶解平衡可用离子方程式表示为___________ ,该平衡的Ksp可表示为___________ 。
(1)S:
(2)Cr:
II.
(3)在一定温度下,Mg(OH)2在水中的沉淀溶解平衡可用离子方程式表示为
您最近半年使用:0次
8 . 已知 的吸光度(A)与溶液中的
的吸光度(A)与溶液中的 成正比,其标准曲线如图所示。常温时,测得
成正比,其标准曲线如图所示。常温时,测得 饱和溶液
饱和溶液 的吸光度A=0.217,下列说法不正确的是
的吸光度A=0.217,下列说法不正确的是

 的吸光度(A)与溶液中的
的吸光度(A)与溶液中的 成正比,其标准曲线如图所示。常温时,测得
成正比,其标准曲线如图所示。常温时,测得 饱和溶液
饱和溶液 的吸光度A=0.217,下列说法不正确的是
的吸光度A=0.217,下列说法不正确的是
A.向 悬浊液中加入少量水, 悬浊液中加入少量水, 不变 不变 |
B. 饱和溶液中 饱和溶液中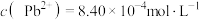 |
C. 的溶度积常数 的溶度积常数 的数量级为 的数量级为 |
D.测得40℃时 饱和溶液 饱和溶液 的吸光度A=0.343,说明 的吸光度A=0.343,说明 的溶解为吸热过程 的溶解为吸热过程 |
您最近半年使用:0次
9 . 常温下,分别向体积均为10mL、浓度均为0.1mol/L的FeCl2和MnCl2溶液中滴加0.1mol/L的K2S溶液,滴加过程中溶液-1gc(Fe2+)和-1gc(Mn2+)与滴入K2S溶液体积(V)的关系如图所示。[已知:Ksp(MnS)>Ksp(FeS),lg3≈0.5,忽略溶液混合时温度和体积的变化],下列说法正确的是
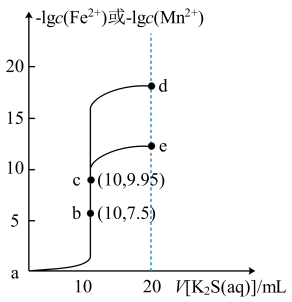

| A.a-b-e为MnCl2溶液的滴定曲线 |
| B.加入过量难溶的FeS可除去FeCl2溶液中混有的Mn2+ |
| C.e点纵坐标约为12.5 |
| D.溶液的pH:c>d>a |
您最近半年使用:0次
2024-01-13更新
|
101次组卷
|
2卷引用:湖南省长沙市麓山国际实验学校2023-2024学年高二上学期第三次月考化学试题
2023高三·全国·专题练习
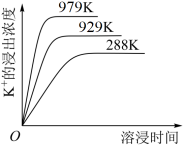
10 . 已知难溶性物质K2SO4·MgSO4·2CaSO4在水中存在如下平衡:K2SO4·MgSO4·2CaSO4(s)⇌2Ca2++2K++Mg2++4 。不同温度下,K+的浸出浓度与溶浸时间的关系如图所示,则下列说法错误的是
。不同温度下,K+的浸出浓度与溶浸时间的关系如图所示,则下列说法错误的是
 。不同温度下,K+的浸出浓度与溶浸时间的关系如图所示,则下列说法错误的是
。不同温度下,K+的浸出浓度与溶浸时间的关系如图所示,则下列说法错误的是
| A.向该体系中加入饱和NaOH溶液,溶解平衡向右移动 |
| B.向该体系中加入饱和碳酸钠溶液,溶解平衡向左移动 |
| C.升高温度,化学反应速率增大,溶解平衡向右移动 |
D.该平衡的Ksp=c2(Ca2+)·c2(K+)·c(Mg2+)·c4( ) ) |
您最近半年使用:0次



