1 . 一块铜板被等分成两块,Cu(a)和Cu(b);锤打Cu(a),Cu(b)不动。再由Cu(a)、Cu(b)及CuSO4溶液组成电池:Cu(a)|CuSO4(cmol·L-1)|Cu(b),测得电动势E>0,因为Cu(a)的
| A.△S>0,△H=0 | B.△S>0,△H<0 |
| C.△S<0,△H=0 | D.△S<0,△H<0 |
您最近半年使用:0次
解题方法
2 . 研究化学反应进行的方向对于反应设计等具有重要意义,下列说法正确的是
A. <0、 <0、 >0的反应在温度低时不能自发进行 >0的反应在温度低时不能自发进行 |
| B.在其他外界条件不变的情况下,汽车排气管中使用催化剂可以改变产生尾气的反应方向 |
| C.冰在室温下自动熔化成水是一个熵增的过程 |
D.一定温度下,反应MgCl2(1) Mg(1)+Cl2(g)的 Mg(1)+Cl2(g)的 <0、 <0、 >0 >0 |
您最近半年使用:0次
解题方法
3 . 已知体系自由能变化ΔG=ΔH-TΔS。已知两个反应的ΔG与温度的关系如图所示,下列说法不正确的是
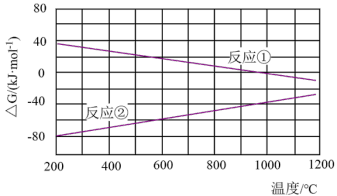
已知:ΔH和ΔS随温度变化很小

已知:ΔH和ΔS随温度变化很小
| A.反应②的ΔS<0 | B.反应①在1200℃时能自发进行 |
| C.在一定温度范围内,反应①②均能自发 | D.反应②的ΔH>0 |
您最近半年使用:0次
解题方法
4 . 下列对熵的理解错误的是
| A.等质量的同种物质气态时熵值最大,固态时熵值最小 |
| B.体系越有序,熵值越小;越混乱,熵值越大 |
| C.从焓判据来看,△H<0有利于反应的自发进行 |
| D.25℃、 1.01×105Pa时,2N2O5(g)=4NO2(g)+O2(g)是熵减反应 |
您最近半年使用:0次
5 . 合成氨厂的CO2可用于合成重要化工原料CH3OH,主要反应为:3H2(g)+CO2(g) CH3OH(g)+H2O(g),向两个容积固定为2L的密闭容器中分别充入比例相同,但总量不同的H2和CO2气体,H2的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
CH3OH(g)+H2O(g),向两个容积固定为2L的密闭容器中分别充入比例相同,但总量不同的H2和CO2气体,H2的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
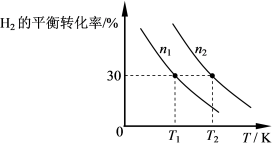
(1)若T1时,向容器中充入n1mol气体(3molH2和1molCO2),反应至5min时达到平衡,则0~5min内CO2的平均反应速率v(CO2)=______ 。
(2)由上图可判断该反应是______ (选填“吸热”或“放热”)反应,在______ (填“较高”或“较低”)温度下有利于该反应自发进行。
(3)判断图中n1、n2相对大小,并说明理由。______
 CH3OH(g)+H2O(g),向两个容积固定为2L的密闭容器中分别充入比例相同,但总量不同的H2和CO2气体,H2的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
CH3OH(g)+H2O(g),向两个容积固定为2L的密闭容器中分别充入比例相同,但总量不同的H2和CO2气体,H2的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。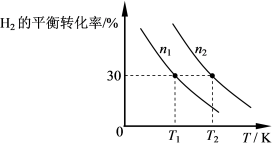
(1)若T1时,向容器中充入n1mol气体(3molH2和1molCO2),反应至5min时达到平衡,则0~5min内CO2的平均反应速率v(CO2)=
(2)由上图可判断该反应是
(3)判断图中n1、n2相对大小,并说明理由。
您最近半年使用:0次
解题方法
6 . 下列词语描述中,属于△H<0、△S>0的化学变化的是
| A.春风化雨 | B.滴水成冰 | C.蜡炬成灰 | D.聚沙成塔 |
您最近半年使用:0次
解题方法
7 . 自发进行的化学反应大多数是_____ 反应,也有些是_____ 反应。(填“吸热”或“放热”)
您最近半年使用:0次
名校
解题方法
8 .  升华的过程中,其焓变和熵变正确的是
升华的过程中,其焓变和熵变正确的是
 升华的过程中,其焓变和熵变正确的是
升华的过程中,其焓变和熵变正确的是A. , , | B. , , |
C. , , | D. , , |
您最近半年使用:0次
9 . 以下过程在常温下都可以自发进行,可利用焓判据来解释的是
| A.2N2O5(g)=4N2O4(g)+O2(g) ΔH=+56.7kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1 |
| C.硝酸铵自发地溶于水 |
| D.湿衣服经过晾晒变干 |
您最近半年使用:0次
2024-01-28更新
|
35次组卷
|
2卷引用:四川省成都市成华区某校2023-2024学年高二上学期12月月考化学试题
名校
解题方法
10 . 下列关于焓判据和熵判据的说法中,不正确的是
| A.放热的自发过程可能是熵减小的过程,吸热的自发过程一定为熵增加的过程 |
| B.4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s) ΔH=-444.3kJ·mol-1,ΔS=-280.1J·mol-1·K-1。此反应在常温常压下能自发进行 |
| C.碳酸钙分解为吸热反应,该反应室温下不能自发进行,但在高温下则能自发进行 |
| D.吉布斯自由能大于0的反应一定不能发生 |
您最近半年使用:0次
2024-01-17更新
|
162次组卷
|
2卷引用:广东省深圳市宝安中学(集团)2023-2024学年高二上学期期中考试 化学试卷



