室温下,下列溶液中粒子浓度关系正确的是
| A.Na2S溶液:c(Na+)> c(HS-)>c(OH-) > c(H2S) |
B.Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O )+2c(H2C2O4) )+2c(H2C2O4) |
C.pH=5的NaHSO3溶液: c(Na+)>c(H2SO3)>c(SO )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
| D.CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) |
更新时间:2021-11-13 16:18:06
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列溶液呈酸性的是
| A.Na2CO3 | B.NaHCO3 | C.NaHSO4 | D.NaCl |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】常温下,下列关于电解质溶液的正确判断是
A.在pH=12的溶液中,Al3+、Cl-、CO 、Na+可以大量共存 、Na+可以大量共存 |
B.在pH=0的溶液中,Na+、NO 、SO 、SO 、K+可以大量共存 、K+可以大量共存 |
C.由水电离出的氢离子浓度为1.0×10-12mol•L-1溶液中,K+、Cl-、HCO 、Na+可以大量共存 、Na+可以大量共存 |
| D.由0.1mol•L-1一元酸HA溶液的pH=3,可推知NaA溶液存在A-+H2O⇌HA+OH- |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列关于电解质溶液的叙述不正确的是
A.常温下, 的 的 溶液和 溶液和 的 的 溶液中, 溶液中, 相等 相等 |
B.中和 、体积均相同的盐酸和醋酸溶液,后者消耗 、体积均相同的盐酸和醋酸溶液,后者消耗 的物质的量较大 的物质的量较大 |
C.将 的醋酸溶液稀释后,溶液中所有离子的浓度均降低 的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
D.同浓度的 与 与 稀溶液中均存在: 稀溶液中均存在: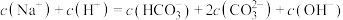 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】设 为阿伏加德罗常数,下列说法不正确的是
为阿伏加德罗常数,下列说法不正确的是
 为阿伏加德罗常数,下列说法不正确的是
为阿伏加德罗常数,下列说法不正确的是A.0.05 液态 液态 中含有0.05 中含有0.05 个阳离子 个阳离子 |
B.0.1  溶液中含有 溶液中含有 微粒数小于0.1 微粒数小于0.1 |
C.0.5  溶于水,溶液中的 溶于水,溶液中的 、 、 、 、 、 、 微粒总数和为0.5 微粒总数和为0.5 |
D.将1  溶于稀氨水中使溶液呈中性,溶液中 溶于稀氨水中使溶液呈中性,溶液中 数目为 数目为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列有关电解质溶液的说法不正确的是
A.向0.1 的氨水中加入少量水,溶液中 的氨水中加入少量水,溶液中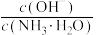 增大 增大 |
B.将 溶液从20℃升温至30℃,溶液中 溶液从20℃升温至30℃,溶液中 增大 增大 |
C.向氢氧化钠溶液中加入醋酸溶液至中性,溶液中 |
D.向 的饱和溶液中加入 的饱和溶液中加入 固体,溶液中的 固体,溶液中的 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】在常温下,下列有关4种溶液的叙述错误的是
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| A.分别加水稀释 10倍,四种溶液的pH:①>②>④>③ |
B.将溶液①④等体积混合,所得溶液中离子浓度的大小关系:c(Cl- )>c( )>c(OH- )>c(H+ ) )>c(OH- )>c(H+ ) |
| C.在溶液①②中分别加入适量的氯化铵晶体后,两种溶液的pH均减小 |
| D.将a L溶液④与b L溶液②混合后(忽略混合后的体积变化),若所得溶液的pH=4,则a:b=11 :9 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】室温下,通过下列实验探究NaHSO3、Na2SO3溶液的性质。
实验1:用pH试纸测量0.1mol·L-1NaHSO3溶液的pH,测得pH约为5
实验2:0.1mol·L-1NaHSO3溶液中加入等体积0.1mol·L-1NaOH溶液,没有明显现象
实验3:0.1mol·L-1Na2SO3溶液中滴加新制饱和氯水,氯水颜色褪去
实验4:将0.1mol·L-1Na2SO3溶液与0.1mol·L-1CaCl2溶液等体积混合,产白色沉淀
下列说法正确的是
实验1:用pH试纸测量0.1mol·L-1NaHSO3溶液的pH,测得pH约为5
实验2:0.1mol·L-1NaHSO3溶液中加入等体积0.1mol·L-1NaOH溶液,没有明显现象
实验3:0.1mol·L-1Na2SO3溶液中滴加新制饱和氯水,氯水颜色褪去
实验4:将0.1mol·L-1Na2SO3溶液与0.1mol·L-1CaCl2溶液等体积混合,产白色沉淀
下列说法正确的是
A.由实验1可得出: >Ka2(H2SO3) >Ka2(H2SO3) |
B.实验2所得的溶液中c(HSO )>c(SO )>c(SO ) ) |
C.实验3中发生反应的离子方程式为H2O+Cl2+SO =SO =SO +2H++2Cl- +2H++2Cl- |
D.实验4中两溶液混合时有:c(Ca2+)·c(SO )<Ksp(CaSO3) )<Ksp(CaSO3) |
您最近一年使用:0次





