1 . 钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:正极_________ , 负极_________ 。
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用如图所示的方案,其中焊接在闸门上的固体材料R可以采用_________。
(3)如图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的_________ 极。
①若溶液的pH=7,则该溶液中c( )
)_________ c(Cl-)。
②若溶液的pH>7,则该溶液中c( )
)_________ c(Cl-)。
③若c( )<c (Cl-),则溶液的pH
)<c (Cl-),则溶液的pH_________ 7。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:正极
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用如图所示的方案,其中焊接在闸门上的固体材料R可以采用_________。
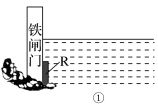
| A.铜 | B.钠 | C.锌 | D.石墨 |
(3)如图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的

①若溶液的pH=7,则该溶液中c(
 )
)②若溶液的pH>7,则该溶液中c(
 )
)③若c(
 )<c (Cl-),则溶液的pH
)<c (Cl-),则溶液的pH
您最近半年使用:0次
名校
解题方法
2 . 常温下,用一定浓度的NaOH溶液滴定某浓度的磷酸溶液,所得溶液的pH与lgX的关系如图所示,X表示 、
、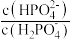 或
或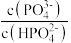 ,下列说法错误的是
,下列说法错误的是
 、
、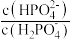 或
或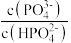 ,下列说法错误的是
,下列说法错误的是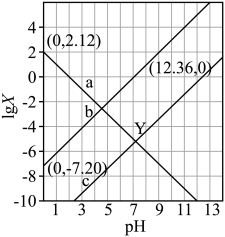
A.b中X为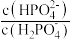 |
| B.Y点溶液的pH=7.24 |
C.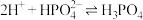 的平衡常数为 的平衡常数为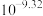 |
D.等浓度的Na3PO4与NaH2PO4溶液按体积比1:3混合后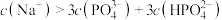 |
您最近半年使用:0次
今日更新
|
164次组卷
|
2卷引用:东北三省四城市联考暨沈阳市高三下学期质量监测(二)化学试题
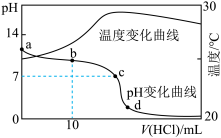
3 . 常温下,往20.00mL1.000mol·L-1氨水中滴入等浓度盐酸,溶液pH和温度随加入盐酸体积的变化曲线如图:___________ Kw(d)(填“>”、“<”或“=”)。
(2)若a点的pH=11,则常温下Kb(NH3·H2O)=___________ 。
(3)当盐酸滴入10mL时得到b点溶液,此时b点溶液中物料守恒___________ ,c(NH3·H2O)___________ c( )(填“>”、“<”或“=”)
)(填“>”、“<”或“=”)
(4)c点溶液的电荷守恒___________ ,此时c点溶液中c( )
)___________ c(Cl-)(填“>”、“<”或“=”)。
(5)a、b、c三点中,水电离出的H+浓度从大到小顺序是___________ ,且此时a点溶液pH=11中水电离出的H+浓度为___________ 。
(2)若a点的pH=11,则常温下Kb(NH3·H2O)=
(3)当盐酸滴入10mL时得到b点溶液,此时b点溶液中物料守恒
 )(填“>”、“<”或“=”)
)(填“>”、“<”或“=”)(4)c点溶液的电荷守恒
 )
)(5)a、b、c三点中,水电离出的H+浓度从大到小顺序是
您最近半年使用:0次
名校
解题方法
4 . 下列有关说法正确的是
A.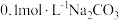 与 与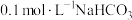 溶液等体积混合: 溶液等体积混合: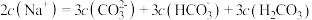 |
B.用相同浓度的 溶液分别滴定等体积 溶液分别滴定等体积 均为3的盐酸和甲酸至终点,消耗 均为3的盐酸和甲酸至终点,消耗 溶液的体积相等 溶液的体积相等 |
C.将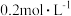 的 的 与 与 的 的 溶液等体积混合后 溶液等体积混合后 ,则: ,则: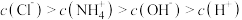 |
D.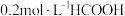 与 与 等体积混合后的溶液中: 等体积混合后的溶液中: |
您最近半年使用:0次
名校
解题方法
5 . 用0.100mol·L-1NaOH溶液滴定等浓度的20mL柠檬酸溶液,滴定曲线如下图所示:_____ 、______ 。
(2)图中50~60mL之间,反应的离子方程式为_______ 。
(3)滴定终点的指示剂选用_______试液。
(4)在上述滴定过程中,各微粒浓度大小关系正确的是_______。
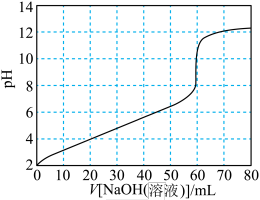
(2)图中50~60mL之间,反应的离子方程式为
(3)滴定终点的指示剂选用_______试液。
| A.无色酚酞 | B.甲基橙 | C.紫色石蕊 | D.品红 |
(4)在上述滴定过程中,各微粒浓度大小关系正确的是_______。
A. 时, 时,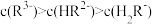 |
B. 时, 时,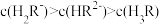 |
C. 时, 时,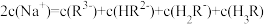 |
D. 时, 时,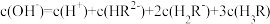 |
您最近半年使用:0次
解题方法
6 . 常温下,乳酸(用HL表示)的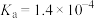 ,乳酸和氢氧化钠溶液反应生成乳酸钠(用NaL表示)。下列说法正确的是
,乳酸和氢氧化钠溶液反应生成乳酸钠(用NaL表示)。下列说法正确的是
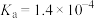 ,乳酸和氢氧化钠溶液反应生成乳酸钠(用NaL表示)。下列说法正确的是
,乳酸和氢氧化钠溶液反应生成乳酸钠(用NaL表示)。下列说法正确的是| A.NaL水溶液呈中性 |
B.0.01 HL溶液的pH=2 HL溶液的pH=2 |
C.0.01 HL溶液中, HL溶液中,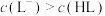 |
D.0.01 NaL溶液中, NaL溶液中, |
您最近半年使用:0次
7 .  为锂离子电池的正极材料的前体,用于制革、处理锅炉水及在食品工业、发酵工业中作缓冲剂。利用以氟磷灰石[主要成分为
为锂离子电池的正极材料的前体,用于制革、处理锅炉水及在食品工业、发酵工业中作缓冲剂。利用以氟磷灰石[主要成分为 ]按下列流程进行制备:
]按下列流程进行制备: 时
时 电离平衡常数
电离平衡常数 ,碳酸电离平衡常数
,碳酸电离平衡常数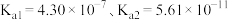 。下列说法正确的是
。下列说法正确的是
 为锂离子电池的正极材料的前体,用于制革、处理锅炉水及在食品工业、发酵工业中作缓冲剂。利用以氟磷灰石[主要成分为
为锂离子电池的正极材料的前体,用于制革、处理锅炉水及在食品工业、发酵工业中作缓冲剂。利用以氟磷灰石[主要成分为 ]按下列流程进行制备:
]按下列流程进行制备:
 时
时 电离平衡常数
电离平衡常数 ,碳酸电离平衡常数
,碳酸电离平衡常数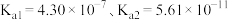 。下列说法正确的是
。下列说法正确的是A. 滴入足量 滴入足量 溶液中反应: 溶液中反应: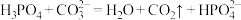 |
B.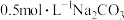 溶液中存在: 溶液中存在: |
C. 溶液中: 溶液中: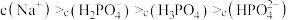 |
D.产生 沉淀的上层清液中, 沉淀的上层清液中, |
您最近半年使用:0次
名校
8 . 25℃时, 水溶液中
水溶液中 、
、 、
、 的分布分数
的分布分数 与pH的关系如下图。例如
与pH的关系如下图。例如 。向0.5L浓度为0.1mol/L的氨水中通入
。向0.5L浓度为0.1mol/L的氨水中通入 气体。已知该温度下,
气体。已知该温度下, 的
的 ,下列说法正确的是
,下列说法正确的是
 水溶液中
水溶液中 、
、 、
、 的分布分数
的分布分数 与pH的关系如下图。例如
与pH的关系如下图。例如 。向0.5L浓度为0.1mol/L的氨水中通入
。向0.5L浓度为0.1mol/L的氨水中通入 气体。已知该温度下,
气体。已知该温度下, 的
的 ,下列说法正确的是
,下列说法正确的是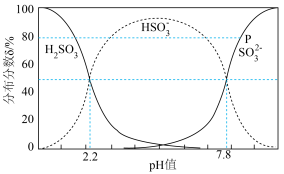
A.通入0.05mol 时, 时,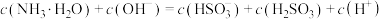 |
B.当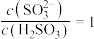 时, 时,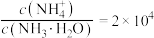 |
C.当 时, 时,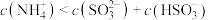 |
D. 的 的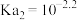 |
您最近半年使用:0次
解题方法
9 . 碳酸氢钠广泛应用于化工、医药、食品和纺织等领域。
(1)实验室用碳酸氢钠固体配制 溶液,需要的仪器有药匙、胶头滴管、量筒、
溶液,需要的仪器有药匙、胶头滴管、量筒、_____ (从下图中选择,写出仪器名称)。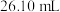 碳酸氢钠溶液于锥形瓶中,滴入2滴甲基橙作指示剂,用浓度为
碳酸氢钠溶液于锥形瓶中,滴入2滴甲基橙作指示剂,用浓度为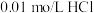 溶液滴定未知浓度的碳酸氢钠溶液。
溶液滴定未知浓度的碳酸氢钠溶液。
①滴定终点的现象是_____ 。
②重复4次的实验数据如下表(待测液的体积均为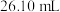 )。
)。
标准 溶液体积的平均值为
溶液体积的平均值为_____  ,用该数据可计算出碳酸氢钠溶液的浓度。
,用该数据可计算出碳酸氢钠溶液的浓度。
(3) 时,向
时,向 溶液中滴加
溶液中滴加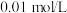 的盐酸,溶液的
的盐酸,溶液的 随加入的盐酸的体积变化如图所示。下列说法正确的是_____(填标号)。
随加入的盐酸的体积变化如图所示。下列说法正确的是_____(填标号)。
(4)某化学小组探究外界因素对 水解程度的影响。甲同学设计实验方案如下
水解程度的影响。甲同学设计实验方案如下
(表中溶液浓度均为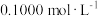 ):
):
i.实验1和2探究加水稀释对 水解程度的影响;
水解程度的影响;
ii.实验1和3探究加入 对
对 水解程度的影响;
水解程度的影响;
iii.实验1和4探究温度对 水解程度的影响。
水解程度的影响。
①根据甲同学的实验方案,补充数据:
_____  。加水稀释
。加水稀释 的水解程度
的水解程度_____ (填“增大”或“减小”)。
②已知 水解为吸热反应,甲同学预测
水解为吸热反应,甲同学预测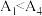 ,但实验结果为
,但实验结果为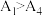 。实验结果与预测不一致的原因可能是
。实验结果与预测不一致的原因可能是_____ 。
(1)实验室用碳酸氢钠固体配制
 溶液,需要的仪器有药匙、胶头滴管、量筒、
溶液,需要的仪器有药匙、胶头滴管、量筒、
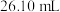 碳酸氢钠溶液于锥形瓶中,滴入2滴甲基橙作指示剂,用浓度为
碳酸氢钠溶液于锥形瓶中,滴入2滴甲基橙作指示剂,用浓度为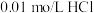 溶液滴定未知浓度的碳酸氢钠溶液。
溶液滴定未知浓度的碳酸氢钠溶液。①滴定终点的现象是
②重复4次的实验数据如下表(待测液的体积均为
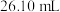 )。
)。| 实验次数 | 1 | 2 | 3 | 4 |
 溶液体积/ 溶液体积/ | 26.10 | 28.20 | 26.12 | 26.08 |
 溶液体积的平均值为
溶液体积的平均值为 ,用该数据可计算出碳酸氢钠溶液的浓度。
,用该数据可计算出碳酸氢钠溶液的浓度。(3)
 时,向
时,向 溶液中滴加
溶液中滴加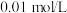 的盐酸,溶液的
的盐酸,溶液的 随加入的盐酸的体积变化如图所示。下列说法正确的是_____(填标号)。
随加入的盐酸的体积变化如图所示。下列说法正确的是_____(填标号)。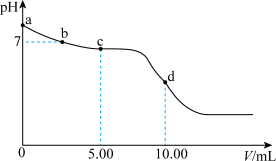
A.若a点坐标为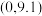 ,则 ,则 水解常数的数量级为 水解常数的数量级为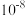 |
B.b点, |
C.c点,溶液中的 主要来自 主要来自 的电离 的电离 |
D.d点,溶液中微粒浓度存在关系: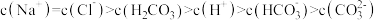 |
(4)某化学小组探究外界因素对
 水解程度的影响。甲同学设计实验方案如下
水解程度的影响。甲同学设计实验方案如下(表中溶液浓度均为
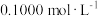 ):
):i.实验1和2探究加水稀释对
 水解程度的影响;
水解程度的影响;ii.实验1和3探究加入
 对
对 水解程度的影响;
水解程度的影响;iii.实验1和4探究温度对
 水解程度的影响。
水解程度的影响。| 序号 | 温度 | 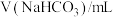 |  |  |  |
| 1 |  | 30.0 | 0 | 0 | 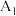 |
| 2 |  | 8.0 | 0 | 22.0 |  |
| 3 |  | 15.0 | a | b | 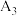 |
| 4 |  | 30.1 | 0 | 0 | 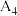 |

 。加水稀释
。加水稀释 的水解程度
的水解程度②已知
 水解为吸热反应,甲同学预测
水解为吸热反应,甲同学预测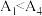 ,但实验结果为
,但实验结果为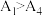 。实验结果与预测不一致的原因可能是
。实验结果与预测不一致的原因可能是
您最近半年使用:0次
名校
解题方法
10 . 室温下,某二元弱酸(用H2A表示)的 、
、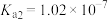 ,NH3⋅H2O的
,NH3⋅H2O的 ,通过下列实验探究NH4HA溶液的性质。
,通过下列实验探究NH4HA溶液的性质。
下列有关说法正确的是
 、
、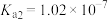 ,NH3⋅H2O的
,NH3⋅H2O的 ,通过下列实验探究NH4HA溶液的性质。
,通过下列实验探究NH4HA溶液的性质。| 实验 | 实验操作 |
| 1 | 用pH试纸测定0.1mol·L-1NH4HA溶液的pH,测得pH约为4.5 |
| 2 | 将0.1mol·L-1NH4HA溶液和0.1mol·L-1NaOH溶液等体积混合,无气体产生 |
| 3 | 向实验2所得溶液中继续滴加一定量0.1mol·L-1NaOH溶液,加热,使产生的气体完全逸出 |
| 4 | 将等体积0.1mol·L-1NH4HA溶液与0.05mol·L-1ZnSO4溶液混合,产生ZnA沉淀 |
A.由实验1可知,0.1mol⋅L-1NH4HA溶液中由水电离出的 |
B.实验2所得溶液中存在: |
C.实验3所得溶液中一定含有Na2A,故反应过程中一定有: |
D.由实验4可知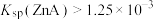 |
您最近半年使用:0次



