名校
解题方法
1 . 已知 的电离常数
的电离常数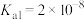 ,
,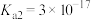 ,常温下,难溶物
,常温下,难溶物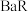 在不同浓度盐酸(足量)中恰好不再溶解时,测得混合液中
在不同浓度盐酸(足量)中恰好不再溶解时,测得混合液中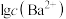 与
与 的关系如图所示,下列说法正确的是
的关系如图所示,下列说法正确的是
 的电离常数
的电离常数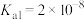 ,
,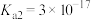 ,常温下,难溶物
,常温下,难溶物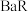 在不同浓度盐酸(足量)中恰好不再溶解时,测得混合液中
在不同浓度盐酸(足量)中恰好不再溶解时,测得混合液中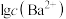 与
与 的关系如图所示,下列说法正确的是
的关系如图所示,下列说法正确的是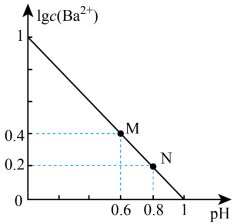
A. 约为 约为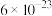 |
B. 点: 点: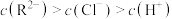 |
C.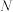 点: 点: 约为 约为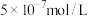 |
D.直线上任一点均满足: |
您最近半年使用:0次
解题方法
2 . 下列物质加入水中,能抑制水的电离,且水溶液呈酸性的是
| A.NH3 | B.KHSO4 | C.CuCl2 | D.CH3COONa |
您最近半年使用:0次
3 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 和 和 的混合气体中所含氮原子数为 的混合气体中所含氮原子数为 |
B. 熔融的 熔融的 中含有 中含有 个阳离子 个阳离子 |
C.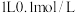 的 的 溶液中含有 溶液中含有 的数目为 的数目为 |
D. 的 的 溶液中含有 溶液中含有 的数目为 的数目为 |
您最近半年使用:0次
名校
4 . 常温下,向一定浓度邻苯二甲酸钠( 表示)溶液中通入
表示)溶液中通入 气体,保持溶液体积和温度不变,测得
气体,保持溶液体积和温度不变,测得 与
与 [
[ 为
为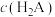 、
、 、
、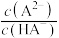 ;
; ]的变化关系如图所示,下列说法错误的是
]的变化关系如图所示,下列说法错误的是
 表示)溶液中通入
表示)溶液中通入 气体,保持溶液体积和温度不变,测得
气体,保持溶液体积和温度不变,测得 与
与 [
[ 为
为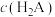 、
、 、
、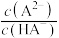 ;
; ]的变化关系如图所示,下列说法错误的是
]的变化关系如图所示,下列说法错误的是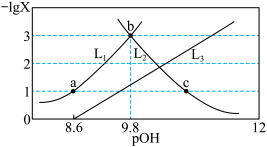
A.曲线 表示 表示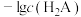 |
B. 点溶液中: 点溶液中: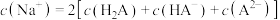 |
C. 的 的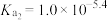 |
D.该溶液中通入和 等物质的量的 等物质的量的 时溶液显碱性 时溶液显碱性 |
您最近半年使用:0次
名校
5 . 钛白粉(纳米级)广泛应用于功能陶瓷、催化剂、化妆品和光敏材料等白色无机颜料。具有优良的遮盖力和着色牢度,适用于不透明的白色制品。其制备原料钛铁矿( )中往往含有
)中往往含有 、MgO、CaO、
、MgO、CaO、 、
、 等杂质。一种硫酸法制取白色颜料钛白粉(
等杂质。一种硫酸法制取白色颜料钛白粉( )的生产工艺如图:
)的生产工艺如图: 形式存在;
形式存在;
②强电解质 在溶液中仅能电离出
在溶液中仅能电离出 和一种阳离子;
和一种阳离子;
③ 不溶于水和稀酸。
不溶于水和稀酸。
(1)要提高酸浸速率,可采取的措施是________ (写出一条即可)。
(2)滤渣①中除铁粉外,还可能含有的成分是________ 。
(3)酸浸过程中, 发生反应的离子方程式为
发生反应的离子方程式为________ 。
(4)加入铁粉的目的是还原体系中的 。为探究最佳反应条件,某实验室做了如下尝试。
。为探究最佳反应条件,某实验室做了如下尝试。
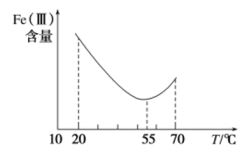
①在其他条件不变的情况下,体系中Fe(III)[指 和
和 等含正三价铁元素的微粒]含量随pH变化如图,试分析,在pH介于4~6之间时,Fe(III)主要以
等含正三价铁元素的微粒]含量随pH变化如图,试分析,在pH介于4~6之间时,Fe(III)主要以________ (填微粒化学式,已知pH>3时近似认为 沉淀完全)形式存在。
沉淀完全)形式存在。________ 。________ 。在实验室中,滤渣③一般在________ (填仪器名称)中灼烧。
 )中往往含有
)中往往含有 、MgO、CaO、
、MgO、CaO、 、
、 等杂质。一种硫酸法制取白色颜料钛白粉(
等杂质。一种硫酸法制取白色颜料钛白粉( )的生产工艺如图:
)的生产工艺如图: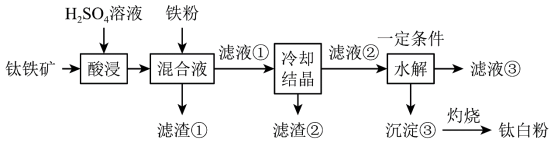
 形式存在;
形式存在;②强电解质
 在溶液中仅能电离出
在溶液中仅能电离出 和一种阳离子;
和一种阳离子;③
 不溶于水和稀酸。
不溶于水和稀酸。(1)要提高酸浸速率,可采取的措施是
(2)滤渣①中除铁粉外,还可能含有的成分是
(3)酸浸过程中,
 发生反应的离子方程式为
发生反应的离子方程式为(4)加入铁粉的目的是还原体系中的
 。为探究最佳反应条件,某实验室做了如下尝试。
。为探究最佳反应条件,某实验室做了如下尝试。①在其他条件不变的情况下,体系中Fe(III)[指
 和
和 等含正三价铁元素的微粒]含量随pH变化如图,试分析,在pH介于4~6之间时,Fe(III)主要以
等含正三价铁元素的微粒]含量随pH变化如图,试分析,在pH介于4~6之间时,Fe(III)主要以 沉淀完全)形式存在。
沉淀完全)形式存在。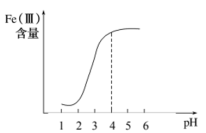
您最近半年使用:0次
解题方法
6 . 常温下:
(1)在0.001 mol/L HCl溶液中,c(H+)=___________ ,c(OH-)=___________ 。
(2)在0.001 mol/L NaOH溶液中,c(H+)=___________ ,由水电离出的c(H+)=___________ 。
(3)在pH=3的NH4Cl溶液中,水电离出的c(H+)=___________ 。
(1)在0.001 mol/L HCl溶液中,c(H+)=
(2)在0.001 mol/L NaOH溶液中,c(H+)=
(3)在pH=3的NH4Cl溶液中,水电离出的c(H+)=
您最近半年使用:0次
7 . 下列实验根据现象得出相应结论不正确的是
| 选项 | 实验 | 现象 | |
| A | 取少量乙酰水杨酸样品,加入3mL蒸馏水和少量乙醇,振荡,再加入1~2滴 |溶液 |溶液 | 呈紫色溶液 | 乙酰水杨酸样品中含有水杨酸 |
| B | 在25℃和50℃时,分别测量0.1  溶液的pH 溶液的pH | 升高温度,溶液的pH下降 | pH变化是 的改变与水解平衡移动共同作用的结果 的改变与水解平衡移动共同作用的结果 |
| C | 将石油裂解产生的气体通入 的 的 溶液 溶液 | 溶液褪色 | 石油裂解产物中含乙烯 |
| D | 室温下,取1mL 0.1 KI溶液和1mL 0.1 KI溶液和1mL 0.1  溶液充分反应后,再加2mL 溶液充分反应后,再加2mL  振荡、静置后,取上层清液滴加少色量KSCN溶液 振荡、静置后,取上层清液滴加少色量KSCN溶液 | 溶液变成红色 |  和 和 的反应有一定的限度 的反应有一定的限度 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
8 . 常温下, 溶液、
溶液、 溶液的
溶液的 均大于7。下列关于这两种溶液的说法正确的是
均大于7。下列关于这两种溶液的说法正确的是
 溶液、
溶液、 溶液的
溶液的 均大于7。下列关于这两种溶液的说法正确的是
均大于7。下列关于这两种溶液的说法正确的是A. 溶液中存在平衡: 溶液中存在平衡: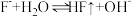 |
B.加热, 溶液的碱性增强 溶液的碱性增强 |
C. 溶液中: 溶液中: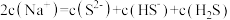 |
D. 溶液中: 溶液中: |
您最近半年使用:0次
解题方法
9 . 金属钛( )广泛应用于航空、军工、医疗等领域。某火电厂粉煤灰(主要成分为
)广泛应用于航空、军工、医疗等领域。某火电厂粉煤灰(主要成分为 、
、 、
、 、
、 、
、 、
、 等)的综合利用具有重要的经济价值和社会效益。工艺流程如下:
等)的综合利用具有重要的经济价值和社会效益。工艺流程如下: 形式存在,易水解;
形式存在,易水解;
②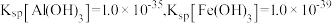 。
。
回答下列问题:
(1)基态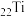 原子有
原子有_______ 个未成对电子,有_______ 个运动状态不同的电子。
(2)“酸浸”时,若要提高浸取速率,可采取的措施是_______ (任写一条)
(3)操作Ⅱ中加热将 水解得
水解得 ,写出其反应的离子方程式:
,写出其反应的离子方程式:_______ 。
(4)由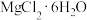 晶体得到无水
晶体得到无水 ,需要
,需要_______ 氛围中加热。
(5)为了使滤渣2沉淀完全(离子浓度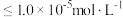 时认为沉淀完全),需“调
时认为沉淀完全),需“调 ”最小为
”最小为_______ 。
 )广泛应用于航空、军工、医疗等领域。某火电厂粉煤灰(主要成分为
)广泛应用于航空、军工、医疗等领域。某火电厂粉煤灰(主要成分为 、
、 、
、 、
、 、
、 、
、 等)的综合利用具有重要的经济价值和社会效益。工艺流程如下:
等)的综合利用具有重要的经济价值和社会效益。工艺流程如下: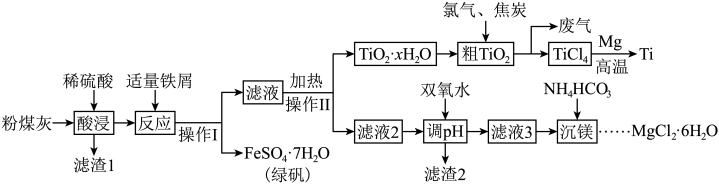
 形式存在,易水解;
形式存在,易水解;②
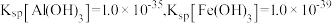 。
。回答下列问题:
(1)基态
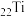 原子有
原子有(2)“酸浸”时,若要提高浸取速率,可采取的措施是
(3)操作Ⅱ中加热将
 水解得
水解得 ,写出其反应的离子方程式:
,写出其反应的离子方程式:(4)由
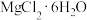 晶体得到无水
晶体得到无水 ,需要
,需要(5)为了使滤渣2沉淀完全(离子浓度
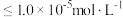 时认为沉淀完全),需“调
时认为沉淀完全),需“调 ”最小为
”最小为
您最近半年使用:0次
10 . 下列事实不能证明亚硝酸( )是弱电解质的是
)是弱电解质的是
 )是弱电解质的是
)是弱电解质的是A.常温下 溶液的 溶液的 |
B.常温下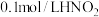 溶液的 溶液的 约为2 约为2 |
| C.亚硝酸溶液中滴加紫色石蕊试液,溶液变红色 |
D.常温下将 的 的 溶液加水稀释至100倍,稀释后溶液的 溶液加水稀释至100倍,稀释后溶液的 约为4.5 约为4.5 |
您最近半年使用:0次



