1 .  水解生成强酸
水解生成强酸 和弱酸
和弱酸 。乙硼烷(
。乙硼烷( )的标准燃烧热为2165
)的标准燃烧热为2165 。
。 与氨气可生成氨硼烷(
与氨气可生成氨硼烷(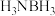 ),氨硼烷水解脱氢得
),氨硼烷水解脱氢得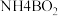 ,
, 与
与 反应也能生成氨硼烷。
反应也能生成氨硼烷。 能将醛、酮转化为相应的醇。下列化学反应表示
能将醛、酮转化为相应的醇。下列化学反应表示不正确 的是
 水解生成强酸
水解生成强酸 和弱酸
和弱酸 。乙硼烷(
。乙硼烷( )的标准燃烧热为2165
)的标准燃烧热为2165 。
。 与氨气可生成氨硼烷(
与氨气可生成氨硼烷(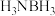 ),氨硼烷水解脱氢得
),氨硼烷水解脱氢得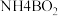 ,
, 与
与 反应也能生成氨硼烷。
反应也能生成氨硼烷。 能将醛、酮转化为相应的醇。下列化学反应表示
能将醛、酮转化为相应的醇。下列化学反应表示A.硼的制备: |
B.乙硼烷燃烧: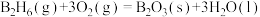  |
C.三氟化硼水解: |
D.氨硼烷的制备: |
您最近一年使用:0次
名校
2 . 实验室制备无水 并进行纯度测定。
并进行纯度测定。
已知:①氯化锌遇水生成 ,
, 受热分解。
受热分解。
②二甲酚橙为金属指示剂。
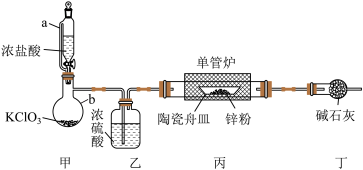
步骤一:利用如图所示装置(夹持装置已省略)制备无水 。
。
取m g试样配成250mL溶液,取25.00mL于锥形瓶中。加入磷酸三钠消除干扰离子后,滴入两滴二甲酚橙作指示剂,用0.4000 EDTA(
EDTA( )标准溶液滴定
)标准溶液滴定 ,终点时消耗EDTA标准溶液的平均体积为15.00mL,测定过程中发生反应
,终点时消耗EDTA标准溶液的平均体积为15.00mL,测定过程中发生反应 。
。
回答下列问题:
(1)盛放碱石灰的仪器的名称为___________ ,使用仪器a的优点:___________ 。
(2)丙装置中主要反应的化学方程式为___________ 。
(3)若不使用乙装置,丙装置得到的产物中会有部分水解而产生杂质,该水解反应的化学方程式为___________ 。
(4)丁装置中碱石灰的作用是___________ 。
(5)氯化锌试样中锌元素的百分含量为___________ %(用含m的代数式表示),滴定前,盛放EDTA标准溶液的滴定管尖嘴部分有气泡,滴定结束后气泡消失,则所测产品中锌元素的百分含量___________ (填“偏高”或“偏低”)。
 并进行纯度测定。
并进行纯度测定。已知:①氯化锌遇水生成
 ,
, 受热分解。
受热分解。②二甲酚橙为金属指示剂。
步骤一:利用如图所示装置(夹持装置已省略)制备无水
 。
。
取m g试样配成250mL溶液,取25.00mL于锥形瓶中。加入磷酸三钠消除干扰离子后,滴入两滴二甲酚橙作指示剂,用0.4000
 EDTA(
EDTA( )标准溶液滴定
)标准溶液滴定 ,终点时消耗EDTA标准溶液的平均体积为15.00mL,测定过程中发生反应
,终点时消耗EDTA标准溶液的平均体积为15.00mL,测定过程中发生反应 。
。回答下列问题:
(1)盛放碱石灰的仪器的名称为
(2)丙装置中主要反应的化学方程式为
(3)若不使用乙装置,丙装置得到的产物中会有部分水解而产生杂质,该水解反应的化学方程式为
(4)丁装置中碱石灰的作用是
(5)氯化锌试样中锌元素的百分含量为
您最近一年使用:0次
名校
解题方法
3 . 探究金属及其化合物的性质,依据下列实验的现象所得出的结论正确的是
| 实验方案 | 现象 | 结论 | |
| A | 往 溶液中滴加浓的 溶液中滴加浓的 溶液 溶液 | 溶液变浑浊 |  难溶于水 难溶于水 |
| B | 往 溶液中滴加KSCN溶液,再加入少量 溶液中滴加KSCN溶液,再加入少量 固体 固体 | 溶液先变成血红色,后无明显变化 |  与 与 的反应不可逆 的反应不可逆 |
| C | 向无水硫酸铜白色粉末中滴加2-3滴蒸馏水 | 白色粉末变蓝 | 无水硫酸铜可用做干燥剂 |
| D | 向 溶液中通过量的 溶液中通过量的 | 溶液变浑浊 |  酸性强于 酸性强于 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 我国科学家研制出一种高效率和高选择性地将 转化为
转化为 的方案,其原理为:
的方案,其原理为: 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 转化为
转化为 的方案,其原理为:
的方案,其原理为: 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.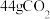 含有的 含有的 键数目为 键数目为 |
B.标准状况下,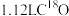 含有中子数为 含有中子数为 |
C.反应中若有 参与反应,则转移的电子数为 参与反应,则转移的电子数为 |
D.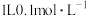 的 的 溶液加水稀释时溶液中 溶液加水稀释时溶液中 始终为 始终为 |
您最近一年使用:0次
解题方法
5 . 主族元素X、Y、Z、W的原子序数依次增加,且均不超过20。X、Y、Z最外层电子数之和为15。W+[Z-X≡Y]−是实验室常用的一种化学试剂,所有元素都满足8电子稳定结构。下列说法中正确的是
| A.简单离子半径:W>Z>Y | B.W2Z的水溶液中滴入酚酞显红色 |
| C.氢化物沸点高低:Y>X | D.最高价氧化物对应的水化物的酸性:X>Y |
您最近一年使用:0次
6 . 化学与生活、科技、社会发展息息相关。下列有关说法不正确的是
| A.卡塔尔世界杯球馆屋顶采用了折叠式PTFE(聚四氟乙烯)板材,该板材属于合成高分子材料 |
| B.乙醇、过氧化氢、次氯酸钠等消毒剂均能将病毒氧化而达到消毒的目的 |
| C.砖瓦是用黏土烧制而成,黏土主要成分为含水的铝硅酸盐 |
| D.高铁酸钾(K2FeO4)在水处理过程中涉及的变化过程有:胶体聚沉、盐类水解、氧化还原反应等 |
您最近一年使用:0次
名校
7 .  发生水解反应的机理如下图。下列说法正确是
发生水解反应的机理如下图。下列说法正确是
 发生水解反应的机理如下图。下列说法正确是
发生水解反应的机理如下图。下列说法正确是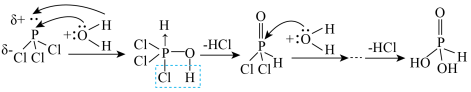
A. 为非极性分子 为非极性分子 | B. 中 中 为 为 杂化 杂化 |
C. 的水解产物 的水解产物 为二元酸 为二元酸 | D. 和 和 均能形成分子间氢键 均能形成分子间氢键 |
您最近一年使用:0次
2024-05-16更新
|
157次组卷
|
3卷引用:2024届重庆市南开中学校高三下学期5月月考化学试题
8 . 常温下,向20 mL浓度均为0.1 mol⋅L 盐酸和醋酸(
盐酸和醋酸(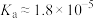 )的混合溶液中滴加0.1 mol⋅L
)的混合溶液中滴加0.1 mol⋅L 的氨水(
的氨水(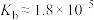 ),测得混合溶液的电阻率(电阻率越大,导电能力越弱)与加入氨水的体积的关系如图所示(忽略混合时体积变化),下列叙述正确的是
),测得混合溶液的电阻率(电阻率越大,导电能力越弱)与加入氨水的体积的关系如图所示(忽略混合时体积变化),下列叙述正确的是
 盐酸和醋酸(
盐酸和醋酸(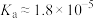 )的混合溶液中滴加0.1 mol⋅L
)的混合溶液中滴加0.1 mol⋅L 的氨水(
的氨水(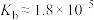 ),测得混合溶液的电阻率(电阻率越大,导电能力越弱)与加入氨水的体积的关系如图所示(忽略混合时体积变化),下列叙述正确的是
),测得混合溶液的电阻率(电阻率越大,导电能力越弱)与加入氨水的体积的关系如图所示(忽略混合时体积变化),下列叙述正确的是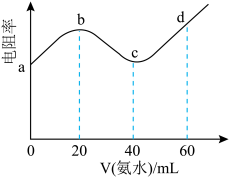
A.a→c过程中,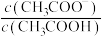 逐渐增大 逐渐增大 |
| B.c→d过程中,水的电离程度一直增大 |
C.c点溶液中,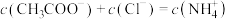 |
D.d点时,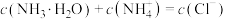 |
您最近一年使用:0次
9 . 磷酸氢二铵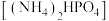 常用作干粉灭火剂,可用磷酸吸收氨气制备。设
常用作干粉灭火剂,可用磷酸吸收氨气制备。设 为阿伏加德罗常数的值,下列叙述错误的是
为阿伏加德罗常数的值,下列叙述错误的是
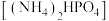 常用作干粉灭火剂,可用磷酸吸收氨气制备。设
常用作干粉灭火剂,可用磷酸吸收氨气制备。设 为阿伏加德罗常数的值,下列叙述错误的是
为阿伏加德罗常数的值,下列叙述错误的是A. 晶体中含有的离子总数为 晶体中含有的离子总数为 |
B.标准状况下,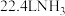 中含有的电子数为 中含有的电子数为 |
C.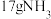 中含有的共价键数目为 中含有的共价键数目为 |
D.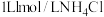 溶液中含有的阳离子数目小于 溶液中含有的阳离子数目小于 |
您最近一年使用:0次
解题方法
10 . 六水合硫酸镁铵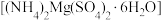 是一种常见复盐,白色晶体,微溶于冷水,难溶于乙醇。
是一种常见复盐,白色晶体,微溶于冷水,难溶于乙醇。
实验室制备步骤如下:
Ⅰ.称取 于100mL烧杯中,加入10mL蒸馏水,搅拌溶解。
于100mL烧杯中,加入10mL蒸馏水,搅拌溶解。
Ⅱ.称取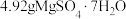 于100mL烧杯中,加入10mL蒸馏水,置于40℃水浴锅中。
于100mL烧杯中,加入10mL蒸馏水,置于40℃水浴锅中。
Ⅲ.将步骤Ⅰ所得的 溶液倒入步骤Ⅱ的
溶液倒入步骤Ⅱ的 溶液中,搅拌混合充分,冰水浴20min,析出晶体。
溶液中,搅拌混合充分,冰水浴20min,析出晶体。
Ⅳ.减压过滤。用无水乙醇洗涤产品1~2次,抽干后,将晶体转移到蒸发皿里,置于40℃水浴锅中约30min,即可得 晶体。
晶体。
Ⅴ.所得晶体称重为mg。
回答下列问题:
(1)称取固体应采用___________ (填“托盘天平”或“电子天平”)。
(2)步骤Ⅰ所得溶液pH___________ 7(填“>”“<”或“=”),原因是___________ 。
(3)步骤Ⅲ的化学方程式是___________ ,下列关于该反应的说法正确的是___________ (填标号)。
A.发生氧化还原反应
B.物质之间溶解度差异导致反应发生
C.冰水浴有助于晶体充分析出
(4)步骤Ⅱ与步骤Ⅳ中都有“置于40℃水浴锅中”,其目的分别是___________ 。
(5)步骤Ⅳ中用无水乙醇洗涤产品的优点是___________ 。
(6)减压过滤也叫抽滤,可加快过滤速度。如图为减压过滤装置,实验过程中操作顺序是___________ ⑤⑥(填序号)。
①打开抽气泵开关,倒入固液混合物 ②修剪滤纸,使其略小于布氏漏斗,让滤纸与漏斗紧密贴合 ③安装仪器,检查是否漏气 ④开始抽滤 ⑤断开吸滤瓶接管 ⑥关抽气泵。___________ (用含m的代数式表示)。
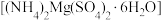 是一种常见复盐,白色晶体,微溶于冷水,难溶于乙醇。
是一种常见复盐,白色晶体,微溶于冷水,难溶于乙醇。实验室制备步骤如下:
Ⅰ.称取
 于100mL烧杯中,加入10mL蒸馏水,搅拌溶解。
于100mL烧杯中,加入10mL蒸馏水,搅拌溶解。Ⅱ.称取
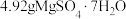 于100mL烧杯中,加入10mL蒸馏水,置于40℃水浴锅中。
于100mL烧杯中,加入10mL蒸馏水,置于40℃水浴锅中。Ⅲ.将步骤Ⅰ所得的
 溶液倒入步骤Ⅱ的
溶液倒入步骤Ⅱ的 溶液中,搅拌混合充分,冰水浴20min,析出晶体。
溶液中,搅拌混合充分,冰水浴20min,析出晶体。Ⅳ.减压过滤。用无水乙醇洗涤产品1~2次,抽干后,将晶体转移到蒸发皿里,置于40℃水浴锅中约30min,即可得
 晶体。
晶体。Ⅴ.所得晶体称重为mg。
回答下列问题:
(1)称取固体应采用
(2)步骤Ⅰ所得溶液pH
(3)步骤Ⅲ的化学方程式是
A.发生氧化还原反应
B.物质之间溶解度差异导致反应发生
C.冰水浴有助于晶体充分析出
(4)步骤Ⅱ与步骤Ⅳ中都有“置于40℃水浴锅中”,其目的分别是
(5)步骤Ⅳ中用无水乙醇洗涤产品的优点是
(6)减压过滤也叫抽滤,可加快过滤速度。如图为减压过滤装置,实验过程中操作顺序是
①打开抽气泵开关,倒入固液混合物 ②修剪滤纸,使其略小于布氏漏斗,让滤纸与漏斗紧密贴合 ③安装仪器,检查是否漏气 ④开始抽滤 ⑤断开吸滤瓶接管 ⑥关抽气泵。

您最近一年使用:0次



