解题方法
1 . 下列溶液因盐的水解而呈碱性的是
A. | B. | C. | D. |
您最近一年使用:0次
2024-03-21更新
|
34次组卷
|
2卷引用:新疆乌鲁木齐第六十一中学2023-2024学年高二上学期期中考试化学试题
2 . 某学生设计如下图Ⅰ装置,进行表演实验,研究2mol/L的硫酸溶液与锌粒和锌粉反应的速率差异。请回答:
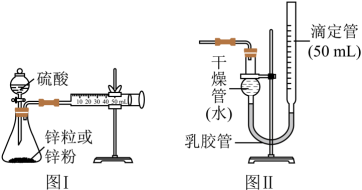
(1)装置图Ⅰ中放有硫酸的仪器名称是_____ 。
(2)按照图Ⅰ装置实验时,两次反应根据经验均超过10分钟,他决定两次实验研究时间均取10min,他还需要测定的另一个数据是_____ 。
(3)实验结束后,得到的结论是_____ 。
(4)该生又将图Ⅰ装置中的气体收集装置改为图Ⅱ,实验完毕待冷却后,该生准备读取滴定管上液面所在处的刻度数,发现滴定管中液面高于干燥管中液面,应首先采取的操作是_____ 。
(5)0.1mol/L的CH3COOH溶液里面离子浓度大小顺序为_____ ,水的电离被_____ (抑制、促进、没有改变)氯化铵溶液pH_____ 7

(1)装置图Ⅰ中放有硫酸的仪器名称是
(2)按照图Ⅰ装置实验时,两次反应根据经验均超过10分钟,他决定两次实验研究时间均取10min,他还需要测定的另一个数据是
(3)实验结束后,得到的结论是
(4)该生又将图Ⅰ装置中的气体收集装置改为图Ⅱ,实验完毕待冷却后,该生准备读取滴定管上液面所在处的刻度数,发现滴定管中液面高于干燥管中液面,应首先采取的操作是
(5)0.1mol/L的CH3COOH溶液里面离子浓度大小顺序为
您最近一年使用:0次
名校
3 . 已知:苹果酸[ ,简记为
,简记为 ]为二元弱酸。常温下,在含
]为二元弱酸。常温下,在含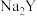 、
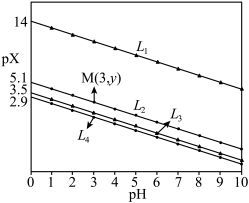
、 的溶液中滴加盐酸,混合液pX[pX=-lgX,
的溶液中滴加盐酸,混合液pX[pX=-lgX, 、
、 、
、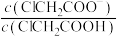 、
、 ]与pH关系如图所示。直线
]与pH关系如图所示。直线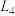 代表
代表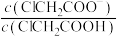 与pH关系。下列叙述错误的是
与pH关系。下列叙述错误的是
 ,简记为
,简记为 ]为二元弱酸。常温下,在含
]为二元弱酸。常温下,在含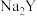 、
、 的溶液中滴加盐酸,混合液pX[pX=-lgX,
的溶液中滴加盐酸,混合液pX[pX=-lgX, 、
、 、
、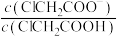 、
、 ]与pH关系如图所示。直线
]与pH关系如图所示。直线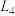 代表
代表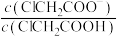 与pH关系。下列叙述错误的是
与pH关系。下列叙述错误的是
A. 、 、 分别代表 分别代表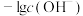 、 、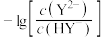 与pH关系 与pH关系 |
B. 电离常数的数量级为 电离常数的数量级为 ,M点的坐标为 ,M点的坐标为 |
C. 溶液中: 溶液中: |
D. 的平衡常数K约为 的平衡常数K约为 |
您最近一年使用:0次
名校
解题方法
4 . X、Y、Z、W、Q为原子序数依次增大的短周期主族元素,已知X、Q为同主族元素且这两种元素能组成离子化合物;Y元素的气态氢化物水溶液显碱性。下列说法正确的是
A.简单离子半径: 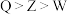 |
B.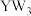 分子的空间结构为平面三角形 分子的空间结构为平面三角形 |
| C.X分别与Y、Z、W组成的常见化合物均为极性分子 |
| D.由Y、Z、Q组成的化合物的水溶液一定显中性 |
您最近一年使用:0次
2023-10-06更新
|
928次组卷
|
5卷引用:皖豫名校联盟2024届高三上学期第一次考试化学试题
皖豫名校联盟2024届高三上学期第一次考试化学试题安徽省巢湖市第一中学2024届高三10月月考化学试题(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)安徽省巢湖市第一中学2024届高三上学期10月月考化学试题江苏省淮安市高中校协作体2023-2024学年高三上学期期中联考化学试题
5 . 能促进水的电离,并使溶液中c(H+)>c(OH-)的操作是
(1)将水加热煮沸;(2)向水中投入一小块金属钠;(3)向水中通CO2;(4)向水中通NH3;(5)向水中加入明矾晶体;(6)向水中加入NaHCO3固体;(7)向水中加NaHSO4固体
(1)将水加热煮沸;(2)向水中投入一小块金属钠;(3)向水中通CO2;(4)向水中通NH3;(5)向水中加入明矾晶体;(6)向水中加入NaHCO3固体;(7)向水中加NaHSO4固体
| A.(1)(3)(6)(7) | B.(1)(3)(6) | C.(5)(7) | D.(5) |
您最近一年使用:0次
名校
解题方法
6 . 中山市马拉松赛事中,组委会设置了众多的补水点。研究表明,喝弱碱性水更符合人的机理特征。下列物质能促进水电离,且显碱性的是
| A.KCl | B.NaOH | C.Na2S | D.NH4Cl |
您最近一年使用:0次
7 . 硫及其化合物在日常生活、工业生产中都非常普遍。
(1)变废为宝是治理污染的常用手段。以 为催化剂,将
为催化剂,将 氧化为
氧化为 ,再进一步转化为硫酸,是工业上制取硫酸的常用方法。该过程可分为如下步骤:
,再进一步转化为硫酸,是工业上制取硫酸的常用方法。该过程可分为如下步骤:
(i)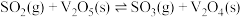
(ii)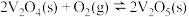
能量变化如图所示。
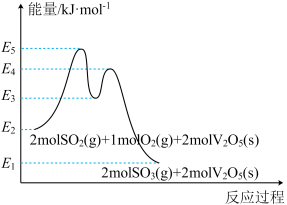
总反应 的
的
_____  (用
(用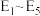 中的合理数据组成的代数式表示)。决定
中的合理数据组成的代数式表示)。决定 催化氧化总反应速率的是步骤
催化氧化总反应速率的是步骤____ (填i或ii),其活化能为______  (用
(用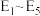 中的合理数据组成的代数式表示)。
中的合理数据组成的代数式表示)。
(2)在水中,硫酸是一种强酸,但实际上只有第一步电离是完全的,第二步电离并不完全,电离方程式可表示为: ,
, 。
。
① 时,
时, 溶液的
溶液的
_____ 7(填“>”“<”或“=”)。
② 的稀硫酸中,
的稀硫酸中,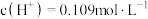 ,则硫酸第二步电离的电离常数
,则硫酸第二步电离的电离常数
_______ (只列式,不计算)。
(3)液态水中,水存在自偶电离: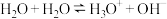 。平常书写的
。平常书写的 ,实际上是纯水或水溶液中
,实际上是纯水或水溶液中 的缩写。如
的缩写。如 在水中电离,完整写法是
在水中电离,完整写法是 。
。
①液态的醋酸(用 表示)中,同样存在
表示)中,同样存在 的自偶电离,其方程式可表示为
的自偶电离,其方程式可表示为____ 。
②用醋酸作溶剂时,硫酸是一种二元弱酸。将少量 溶于冰醋酸中,第一步电离的完整写法是
溶于冰醋酸中,第一步电离的完整写法是____ 。若保持温度不变,关于该所得溶液,下列说法正确的是____ 。
A.加入少量冰醋酸,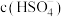 与
与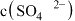 均减小
均减小
B.加入少量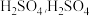 的电离程度增大
的电离程度增大
C.加入少量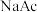 固体,
固体,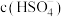 与
与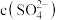 的比值减小
的比值减小
D.加入少量 固体,
固体,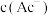 减小
减小
(1)变废为宝是治理污染的常用手段。以
 为催化剂,将
为催化剂,将 氧化为
氧化为 ,再进一步转化为硫酸,是工业上制取硫酸的常用方法。该过程可分为如下步骤:
,再进一步转化为硫酸,是工业上制取硫酸的常用方法。该过程可分为如下步骤:(i)
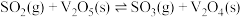
(ii)
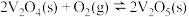
能量变化如图所示。

总反应
 的
的
 (用
(用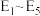 中的合理数据组成的代数式表示)。决定
中的合理数据组成的代数式表示)。决定 催化氧化总反应速率的是步骤
催化氧化总反应速率的是步骤 (用
(用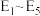 中的合理数据组成的代数式表示)。
中的合理数据组成的代数式表示)。(2)在水中,硫酸是一种强酸,但实际上只有第一步电离是完全的,第二步电离并不完全,电离方程式可表示为:
 ,
, 。
。①
 时,
时, 溶液的
溶液的
②
 的稀硫酸中,
的稀硫酸中,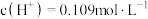 ,则硫酸第二步电离的电离常数
,则硫酸第二步电离的电离常数
(3)液态水中,水存在自偶电离:
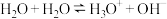 。平常书写的
。平常书写的 ,实际上是纯水或水溶液中
,实际上是纯水或水溶液中 的缩写。如
的缩写。如 在水中电离,完整写法是
在水中电离,完整写法是 。
。①液态的醋酸(用
 表示)中,同样存在
表示)中,同样存在 的自偶电离,其方程式可表示为
的自偶电离,其方程式可表示为②用醋酸作溶剂时,硫酸是一种二元弱酸。将少量
 溶于冰醋酸中,第一步电离的完整写法是
溶于冰醋酸中,第一步电离的完整写法是A.加入少量冰醋酸,
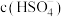 与
与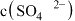 均减小
均减小B.加入少量
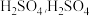 的电离程度增大
的电离程度增大C.加入少量
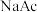 固体,
固体,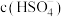 与
与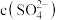 的比值减小
的比值减小D.加入少量
 固体,
固体, 减小
减小
您最近一年使用:0次
2024-02-14更新
|
73次组卷
|
2卷引用:海南省海南中学2023- 2024学年高三上学期第4次月考化学试题
名校
8 . 根据要求回答下列问题。
(1)常温下,将某一元酸HA(甲、乙代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
从甲组实验结果分析,该混合溶液中离子浓度由大到小的顺序是___________ 。
(2)pH相同的①NaCN ②NaClO ③Na2S三种溶液,其物质的量浓度由大到小的顺序为___________ (填序号)。(已知:弱酸的电离平衡常数HCN:Ka=4×10-10;H2S:Ka1=1×10-7,Ka2=7×10-15;HClO:Ka=3×10-8 )
(3)可溶性铝盐常用作净水剂的原因:_______ (用离子方程式表示)。
(4)在常温下,0.1 mol﹒L-1一元酸HB溶液的 ,常温下,有c(H+)相同、体积相同的盐酸和酸HB两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
,常温下,有c(H+)相同、体积相同的盐酸和酸HB两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是______ (填字母)。(①表示盐酸,②表示HB)
a.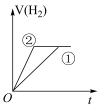 b.
b.  c.
c. 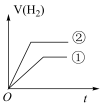 d.
d.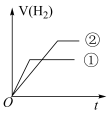
(5)相同物质的量浓度的五种溶液:①(NH4)2SO4 ②氨水 ③NH4HSO4 ④NH4Cl ⑤(NH4)2Fe(SO4)2 ,c( )由大到小顺序是
)由大到小顺序是___________ (用序号表示)。
(6)常温下,将0.2molH2C2O4加入300ml2mol/L的NaOH溶液中(假设溶液的体积不变),所得溶液的pH=a,则c(C2O )+2c(HC2O
)+2c(HC2O )+3c(H2C2O4)=
)+3c(H2C2O4)=_____ mol/L(用含a的代数式表示)。
(1)常温下,将某一元酸HA(甲、乙代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
| 实验编号 | 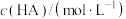 | 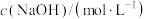 | 混合溶液的pH |
| 甲 | 0.2 | 0.1 | >7 |
| 乙 | 0.1 | 0.1 | =10 |
(2)pH相同的①NaCN ②NaClO ③Na2S三种溶液,其物质的量浓度由大到小的顺序为
(3)可溶性铝盐常用作净水剂的原因:
(4)在常温下,0.1 mol﹒L-1一元酸HB溶液的
 ,常温下,有c(H+)相同、体积相同的盐酸和酸HB两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
,常温下,有c(H+)相同、体积相同的盐酸和酸HB两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是a.
 b.
b.  c.
c.  d.
d.
(5)相同物质的量浓度的五种溶液:①(NH4)2SO4 ②氨水 ③NH4HSO4 ④NH4Cl ⑤(NH4)2Fe(SO4)2 ,c(
 )由大到小顺序是
)由大到小顺序是(6)常温下,将0.2molH2C2O4加入300ml2mol/L的NaOH溶液中(假设溶液的体积不变),所得溶液的pH=a,则c(C2O
 )+2c(HC2O
)+2c(HC2O )+3c(H2C2O4)=
)+3c(H2C2O4)=
您最近一年使用:0次
2024-02-02更新
|
140次组卷
|
3卷引用:四川省成都石室中学2023-2024学年高二上学期期中考试化学试卷
名校
解题方法
9 . 对浓度均为 的①
的① 溶液 ②
溶液 ② 溶液,下列分析
溶液,下列分析不正确 的是
 的①
的① 溶液 ②
溶液 ② 溶液,下列分析
溶液,下列分析| A.①、②中的离子种类相同 |
| B.①中水的电离程度比②中小 |
C.两种溶液的 大小:①>② 大小:①>② |
D.①、②均有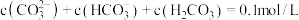 |
您最近一年使用:0次
解题方法
10 . 下列物质溶于水促进水的电离且使溶液显酸性的是
| A.KHSO3 | B.AlCl3 | C.NaHSO4 | D.H2SO4 |
您最近一年使用:0次



