22. Ⅰ.在火箭推进器中装有强还原剂肼(N
2H
4)和强氧化剂(H
2O
2),当它们混合时,即产生大量的N
2和水蒸气,并放出大量热.已知0.4 mol液态肼和足量H
2O
2反应,生成氮气和水蒸气,放出256 kJ的热量.
(1)写出该反应的热化学方程式
____________________________________________________.
(2)已知H
2O(l)=H
2O(g);△
H=+44 kJ/mol,则16 g液态肼燃烧生成氮气和液态水时,放出的热量是
______kJ.
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是
______________________________________________________.
Ⅱ.中和热的测定是高中重要的定量实验.取0.55 moL的NaOH溶液50 mL与0.25 mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
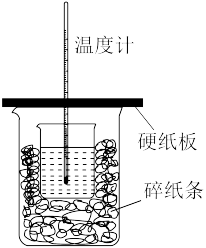
(4)从图中实验装置看,其中尚缺少的一种玻璃用品是
________________________________.
(5)若改用60 mL 0.25 mol·L
-1 H
2SO
4和50 mL 0.55 mol·L
-1 NaOH溶液进行反应与上述实验相比,所放出的热量
______________(填“相等”、“不相等”),若实验操作均正确,则所求中和热
______________(填“相等”、“不相等”) .
(6)将50 mL 0.55 mol/L NaOH溶液和50 mL 0.25 mol/L硫酸溶液(密度都近似为1g/cm
3)进行以上实验,经过多次实验测出反应前后温度差平均值为3.4℃.已知中和后生成溶液的比热容
c=4.18J/(g·℃),则中和热△
H=
______________kJ/mol(取小数点后一位).
(7)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是
__________(填字母).
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H
2SO
4溶液的温度