15. 已知碳化铝(Al
4C
3)与水反应生成氢氧化铝和甲烷。为了探究甲烷性质,某同学设计如下两组实验方案:
甲方案探究甲烷与氧化剂反应(如图1所示);
乙方案探究甲烷与氯气反应的条件(如图2所示)。
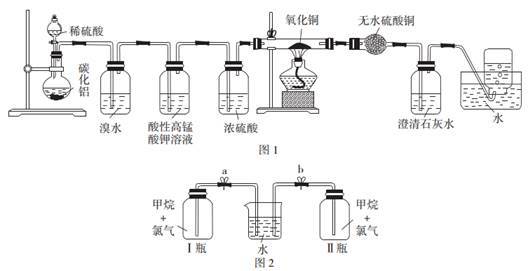
甲方案实验现象:溴水不褪色,无水硫酸铜变蓝色,澄清石灰水变浑浊。
乙方案实验操作过程:通过排饱和食盐水的方法收集两瓶甲烷与氯气(体积比为1:4)的混合气体,I瓶放在光亮处,Ⅱ瓶用预先准备好的黑色纸套套上,按图2安装好装置,并加紧弹簧夹a和b。
(1)碳化铝与稀硫酸反应的化学方程式为
____________________。
(2)实验甲中浓硫酸的作用是
_______________,集气瓶中收集到的气体
_________(填“能”或“不能”)直接排入空气中。
(3)下列对甲方案实验中的有关现象与结论的叙述都正确的是
_________(填标号)。
| A.酸性高锰酸钾溶液不褪色,结论是通常条件下甲烷不能与强氧化剂反应 |
| B.硬质玻璃管里黑色粉末无颜色变化,结论是甲烷不与氧化铜反应 |
| C.硬质玻璃管里黑色粉末变红色,推断氧化铜与甲烷反应只生成水和二氧化碳 |
| D.甲烷不能与溴水反应,推知甲烷不能与卤素单质反应 |
(4)写出甲方案实验中硬质玻璃管里可能发生反应的化学方程式:
________________(假设消耗甲烷与氧化铜的物质的量之比为2:7)。
(5)一段时间后,观察到图2装置中出现的实验现象是
____________________;然后打开弹簧夹a、b,观察到的实验现象是
______________________。