20. (Ⅰ)50mL0.5mol·L
-1的盐酸与50mL0.55mol·L
-1的NaOH溶液在下图所示的位置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,可知下图装置有三处不妥之处,请指出
____________。

(2)在测定中和热的实验中,计算反应热时需要的数据有
_________①酸的浓度和体积
②碱的浓度和体积
③比热容
④反应前后溶液的温度差
⑤操作所需时间
A.①②③⑤
B. ①②③④
C. ②③④⑤
D. ①③④⑤
(3)实验中改用60mL0.50mol·L
-1的盐酸跟50mL0.55mol·L
-1的NaOH溶液进行反应,与上述实验相比,所求中和热
_________(填“相等”或“不相等”),所放出的热量
________(填“相等”或“不相等”)。
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会
______(填“偏大”、“偏小”或“无影响”).
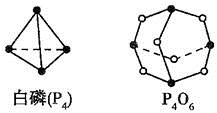
(Ⅱ)(5)化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量,已知白磷和P
4O
6 的分子结构如下图所示,现提供以下化学键的键能:

:
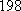
kJ·mol
-1,

:
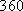
kJ·mol
-1,
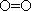
:

kJ·mol
-1,则反应P
4(白磷) +3O
2=P
4O
6的热化学反应方程式为
__________________。
(6)肼(N
2H
4)可作为火箭发动机的燃料,与氧化剂N
2O
4反应生成N
2和水蒸气。
已知:①N
2(g)+2O
2(g)═N
2O
4(l)
△H
1═-19.5kJ•mol
-1②N
2H
4(l)+O
2(g)═N
2(g)+2H
2O(g)
△H
2═-534.2kJ•mol
-1写出肼和N
2O
4反应的热化学方程式
___________________ 。
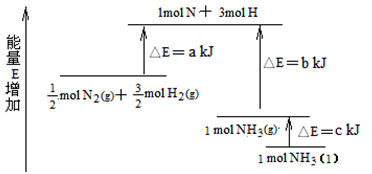
(7)化学反应N
2+3H
2
2NH
3的能量变化如图所示,该反应生成NH
3(I)的热化学方程式是
______________。