20. 向一体积不变的密闭容器中加入2 mol A、0.6 mol C和一定量的B三种气体。一定条件下发生反应2A(g) + B(g)
⇌3C(g)
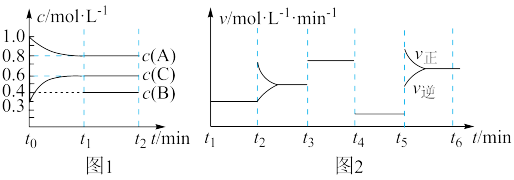
ΔH>0,各物质浓度随时间变化如图1所示。图2为t
2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知t
3~t
4阶段为使用催化剂;图1中t
0~t
1阶段c(B)未画出。
(1)若t
1=15 min,则t
0~t
1阶段以C浓度变化表示的反应速率为v(C)=
________。
(2)t
4~t
5阶段改变的条件为
_______,B的起始物质的量为
______。各阶段平衡时对应的平衡常数如表所示:
| t1~t2 | t2~t3 | t3~t4 | t4~t5 | t5~t6 |
| K1 | K2 | K3 | K4 | K5 |
则K
1=
______(计算式),K
1、K
2、K
3、K
4、K
5之间的关系为
_____(用“>”“<”或“=”连接)。
(3)t
5~t
6阶段保持容器内温度不变,若A的物质的量共变化了0.01 mol,而此过程中容器与外界的热交换总量为a kJ,该反应的热化学方程式:2A(g) + B(g)
⇌3C(g)
ΔH,用含有a的代数式表达 ΔH =
________。
(4)在相同条件下,若起始时容器中加入4mol A、2 mol B和1.2 mol C,达到平衡时,体系中 C的百分含量比t
1时刻C的百分含量
_____(填“大于”“小于”“等于”)。
(5)能说明该反应已达到平衡状态的是
______。
a.v(A)=2v(B)
b.容器内压强保持不变
c.2v
逆(c)=3v
正(A)
d.容器内密度保持不变
(6)为使该反应的反应速率增大,且平衡向正反应方向移动的是
____。
a.及时分离出C气体
b.适当升高温度
c.增大O
2的浓度
d.选择高效催化剂