(1) 对于Fe+2H+===Fe2++H2↑改变下列条件对反应速率和产量有何影响 (填“增大”“减小”或“不变”):把铁片改成铁粉:________ ;滴加几滴浓硫酸_______ ;加压:________ ;
(2) 某小组利用H2C2O4溶液和硫酸酸化的KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性KMnO4溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:
①表中V1=__________ mL
②探究温度对化学反应速率影响的实验编号是________ (填编号)
③实验③测得KMnO4溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=________ mol·L-1·min-1。
(2) 某小组利用H2C2O4溶液和硫酸酸化的KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性KMnO4溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案。已知:
| 实验 编号 | 0.1mol/L酸性KMnO4溶液的体积/mL | 0.6mol/LH2C2O4溶液的体积/mL | H2O的体积/mL | 实验温度/℃ | 溶液褪色所需时间/min |
| ① | 10 | V1 | 35 | 25 | |
| ② | 10 | 10 | 30 | 25 | |
| ③ | 10 | 10 | V2 | 50 |
①表中V1=
②探究温度对化学反应速率影响的实验编号是
③实验③测得KMnO4溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=
18-19高二上·宁夏银川·期末 查看更多[6]
湖南省衡阳师范学院祁东附属中学2019-2020学年高二上学期期中考试化学试题吉林省延边第二中学2020-2021学年高二上学期第一次考试月考化学试题(已下线)2.2+影响化学反应速率的因素-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)山东省济宁市泗水县2019-2020学年高二上学期期中考试化学试题(已下线)2.1.2 影响化学反应速率的因素(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)【全国百强校】宁夏回族自治区银川市第一中学2018-2019学年高二上学期期末考试化学试题
更新时间:2019-01-16 10:14:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】碘及其化合物在生产生活中有重要作用。
(1)单质碘可与氢气反应生成碘化氢。将物质的量比为 的氢气和碘蒸气放入恒容密闭容器中进行反应:
的氢气和碘蒸气放入恒容密闭容器中进行反应: ,反应经过5分钟后达平衡,测得碘化氢的浓度为0.1mol/L,碘蒸气的浓度为0.05mol/L。
,反应经过5分钟后达平衡,测得碘化氢的浓度为0.1mol/L,碘蒸气的浓度为0.05mol/L。
①前5分钟平均反应速率
___________ , 的初始浓度是
的初始浓度是___________ mol/L。
②反应分别进行至3min和7min时假设容器内气体的密度分别用 和
和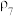 表示,则其大小为关系为
表示,则其大小为关系为
___________ 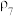 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③下列能说明反应已达平衡状态的是___________ (填序号)。
a.混合体系总压强保持不变
b.单位时间内断裂的 键数目与断裂的
键数目与断裂的 键数目相等
键数目相等
c.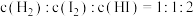
d.
e.反应混合体系的颜色不再发生变化
(2)某小组同学在室温下进行“碘钟实验”:将浓度均为0.01mol/L的 、
、 、
、 、
、 溶液及淀粉混合,一定时间后溶液变为蓝色。
溶液及淀粉混合,一定时间后溶液变为蓝色。
已知:“碘钟实验”的总反应的离子方程式为
反应分两步进行:
反应A:……
反应B:
①反应A的离子方程式是___________ 。对于总反应, 的作用是
的作用是___________ 。
②为探究溶液变蓝快慢的影响因素,进行实验Ⅰ、Ⅱ(溶液浓度均为0.01mol/L)
溶液从混合时的无色变为蓝色的时间:实验Ⅰ是30min、实验Ⅱ是40min。实验Ⅱ中,z所对应的数值是___________ ;对比实验Ⅰ、Ⅱ可得出的实验结论是___________ 。
(1)单质碘可与氢气反应生成碘化氢。将物质的量比为
 的氢气和碘蒸气放入恒容密闭容器中进行反应:
的氢气和碘蒸气放入恒容密闭容器中进行反应: ,反应经过5分钟后达平衡,测得碘化氢的浓度为0.1mol/L,碘蒸气的浓度为0.05mol/L。
,反应经过5分钟后达平衡,测得碘化氢的浓度为0.1mol/L,碘蒸气的浓度为0.05mol/L。①前5分钟平均反应速率

 的初始浓度是
的初始浓度是②反应分别进行至3min和7min时假设容器内气体的密度分别用
 和
和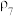 表示,则其大小为关系为
表示,则其大小为关系为
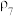 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③下列能说明反应已达平衡状态的是
a.混合体系总压强保持不变
b.单位时间内断裂的
 键数目与断裂的
键数目与断裂的 键数目相等
键数目相等c.
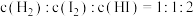
d.

e.反应混合体系的颜色不再发生变化
(2)某小组同学在室温下进行“碘钟实验”:将浓度均为0.01mol/L的
 、
、 、
、 、
、 溶液及淀粉混合,一定时间后溶液变为蓝色。
溶液及淀粉混合,一定时间后溶液变为蓝色。已知:“碘钟实验”的总反应的离子方程式为

反应分两步进行:
反应A:……
反应B:

①反应A的离子方程式是
 的作用是
的作用是②为探究溶液变蓝快慢的影响因素,进行实验Ⅰ、Ⅱ(溶液浓度均为0.01mol/L)
| 用量试剂 |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 |  溶液(含淀粉) 溶液(含淀粉) |  |
| 实验Ⅰ | 5 | 4 | 8 | 3 | 0 |
| 实验Ⅱ | 5 | 2 | x | y | z |
溶液从混合时的无色变为蓝色的时间:实验Ⅰ是30min、实验Ⅱ是40min。实验Ⅱ中,z所对应的数值是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知: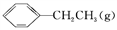
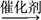
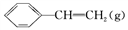 +H2(g) ΔH=+124 kJ·mol-1,若反应体系达到平衡后,各物质的浓度在不同条件下(只改变一种条件)的变化状况如图所示(第10 min到14 min的
+H2(g) ΔH=+124 kJ·mol-1,若反应体系达到平衡后,各物质的浓度在不同条件下(只改变一种条件)的变化状况如图所示(第10 min到14 min的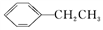 浓度变化曲线未表示出):
浓度变化曲线未表示出):
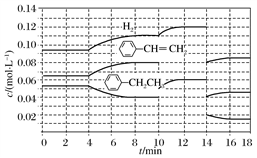
(1)第2min反应温度T(2)与第8 min反应温度T(8)的高低:T(2)________ (填“<”、“>”或“=”)T(8);第10 min时反应改变的条件是______________________________________________ 。
(2)比较产物苯乙烯在2~3min、5~6min和12~13min时平均反应速率[平均反应速率分别以v(2~3)、v(5~6)、v(12~13)表示]的大小________________________ 。
(3)反应物乙苯在5~6min和15~16min时平均反应速率的大小:v(5~6)大于v(15~16),原因是________________________________________ 。
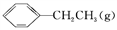
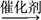
 +H2(g) ΔH=+124 kJ·mol-1,若反应体系达到平衡后,各物质的浓度在不同条件下(只改变一种条件)的变化状况如图所示(第10 min到14 min的
+H2(g) ΔH=+124 kJ·mol-1,若反应体系达到平衡后,各物质的浓度在不同条件下(只改变一种条件)的变化状况如图所示(第10 min到14 min的 浓度变化曲线未表示出):
浓度变化曲线未表示出):
(1)第2min反应温度T(2)与第8 min反应温度T(8)的高低:T(2)
(2)比较产物苯乙烯在2~3min、5~6min和12~13min时平均反应速率[平均反应速率分别以v(2~3)、v(5~6)、v(12~13)表示]的大小
(3)反应物乙苯在5~6min和15~16min时平均反应速率的大小:v(5~6)大于v(15~16),原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮氧化合物是大气污染物,利用甲烷( )与
)与 反应可以消除氮氧化合物,反应如下:
反应可以消除氮氧化合物,反应如下: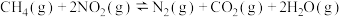
 ,回答下列问题:
,回答下列问题:
(1)为了加快化学反应速率,同时提高 的平衡浓度,可以采取的措施是
的平衡浓度,可以采取的措施是____________ 。
(2)温度为T1和T2时,在体积为2L的某刚性密闭容器中,加入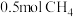 和
和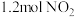 气体,发生上述反应,测得有关数据如表:
气体,发生上述反应,测得有关数据如表:
①温度为T1时,在0~10min内用 表示的平均反应速率
表示的平均反应速率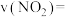
______  。
。
②温度T1______ T2(填“大于”或“小于”),a=______ mol。
③
______ 0(填“大于”或“小于”),分析原因是____________ 。
(3)在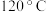 ,100kPa下用氦气作为稀释气体发生:
,100kPa下用氦气作为稀释气体发生:
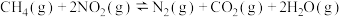 (主反应①)
(主反应①)
同时能发生下列两个副反应:
 (副反应②)
(副反应②)  (副反应③)
(副反应③)
在以上反应体系中 转化为
转化为 、
、 和NO的选择性用S表示(
和NO的选择性用S表示(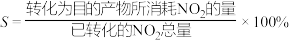 ),各反应的
),各反应的 的选择性S随
的选择性S随 平衡转化率的变化曲线如图所示:
平衡转化率的变化曲线如图所示:
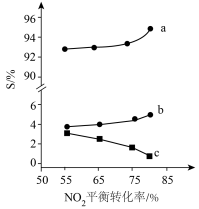
其中曲线b代表的反应是______ (填“①”、“②”或“③”),理由是____________ 。
 )与
)与 反应可以消除氮氧化合物,反应如下:
反应可以消除氮氧化合物,反应如下: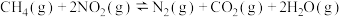
 ,回答下列问题:
,回答下列问题:(1)为了加快化学反应速率,同时提高
 的平衡浓度,可以采取的措施是
的平衡浓度,可以采取的措施是(2)温度为T1和T2时,在体积为2L的某刚性密闭容器中,加入
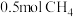 和
和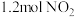 气体,发生上述反应,测得有关数据如表:
气体,发生上述反应,测得有关数据如表:| 时间/min | 0 | 10 | 20 | 40 | 50 | |
| T1 | 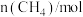 | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | 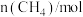 | 0.50 | 0.30 | 0.218 | a | 0.15 |
 表示的平均反应速率
表示的平均反应速率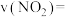
 。
。②温度T1
③

(3)在
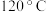 ,100kPa下用氦气作为稀释气体发生:
,100kPa下用氦气作为稀释气体发生: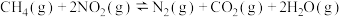 (主反应①)
(主反应①)同时能发生下列两个副反应:
 (副反应②)
(副反应②)  (副反应③)
(副反应③)在以上反应体系中
 转化为
转化为 、
、 和NO的选择性用S表示(
和NO的选择性用S表示(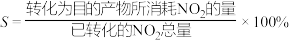 ),各反应的
),各反应的 的选择性S随
的选择性S随 平衡转化率的变化曲线如图所示:
平衡转化率的变化曲线如图所示:
其中曲线b代表的反应是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)已知在2L的容器中进行下列可逆反应,各物质的有关数据如表:
aA(g) + bB(g) C(g)
C(g)
则:
①该可逆反应的化学方程式可表示为_______ ;
②0到2s用物质C来表示的反应速率为_______ ;
③从反应开始到2s末,B的转化率为_______ ;
④下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是_______ 。
A.vB(消耗)=vC(生成) B.容器内气体的总压强保持不变
C.容器内气体的密度不变 D.容器内气体A的物质的量分数保持不变
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验:
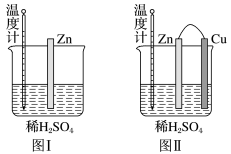
①下列说法正确的是_______ 。
A.图Ⅰ低于图Ⅱ的示数
B.图Ⅰ和图Ⅱ中的温度计示数相等,均高于室温
C.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面
D.图Ⅱ中产生气体的速率比图Ⅰ快
②写出在碱性条件下,氢氧燃料电池的负极反应方程式_______ ;当外电路有2mol电子通过时,消耗在标准状况下氧气的体积为_______ L 。
③原电池中,电解质溶液的阳离子流向_______ 极(填“正”或“负”)。
(1)已知在2L的容器中进行下列可逆反应,各物质的有关数据如表:
aA(g) + bB(g)
 C(g)
C(g)| 物质 | A | B | C |
| 起始物质的量(mol) | 2 | 2 | 0 |
| 2s末物质的量(mol) | 1.4 | 0.8 | 0.6 |
则:
①该可逆反应的化学方程式可表示为
②0到2s用物质C来表示的反应速率为
③从反应开始到2s末,B的转化率为
④下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
A.vB(消耗)=vC(生成) B.容器内气体的总压强保持不变
C.容器内气体的密度不变 D.容器内气体A的物质的量分数保持不变
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验:

①下列说法正确的是
A.图Ⅰ低于图Ⅱ的示数
B.图Ⅰ和图Ⅱ中的温度计示数相等,均高于室温
C.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面
D.图Ⅱ中产生气体的速率比图Ⅰ快
②写出在碱性条件下,氢氧燃料电池的负极反应方程式
③原电池中,电解质溶液的阳离子流向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
(1)某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。
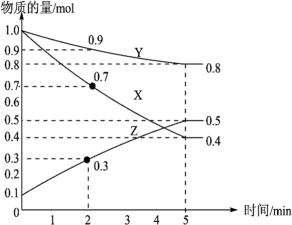
由图中的数据分析,该反应的化学方程式为_______ ;反应开始至2min时Z的平均反应速率为_______ ;
(2)把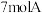 气体和
气体和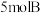 气体混合放入2L密闭容器中,在一定条件下发生反应:
气体混合放入2L密闭容器中,在一定条件下发生反应: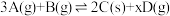 ,经5min达到平衡,此时生成
,经5min达到平衡,此时生成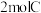 ,测得D的平均反应速率为
,测得D的平均反应速率为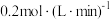 ,求:
,求:
①x的值_______ ,B的转化率_______ 。
②平衡时压强与初始时压强之比_______ 。
③该温度下此反应的平衡常数_______ 。
(1)某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。

由图中的数据分析,该反应的化学方程式为
(2)把
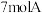 气体和
气体和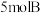 气体混合放入2L密闭容器中,在一定条件下发生反应:
气体混合放入2L密闭容器中,在一定条件下发生反应: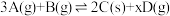 ,经5min达到平衡,此时生成
,经5min达到平衡,此时生成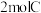 ,测得D的平均反应速率为
,测得D的平均反应速率为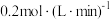 ,求:
,求:①x的值
②平衡时压强与初始时压强之比
③该温度下此反应的平衡常数
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】一定温度下,向1.0 L密闭容器中加入0.60 mol X(g),发生反应X(g) Y(s)+2Z(g) ΔH>0,测得反应物X浓度与反应时间的数据如下表:
Y(s)+2Z(g) ΔH>0,测得反应物X浓度与反应时间的数据如下表:
(1)3 min时用Z表示的平均反应速率v(Z)=________________________ 。
(2)分析该反应中反应物的浓度与时间的规律,得出的结论是______________ 。
由此规律推出反应在6 min时反应物的浓度a为__________ mol·L-1。
 Y(s)+2Z(g) ΔH>0,测得反应物X浓度与反应时间的数据如下表:
Y(s)+2Z(g) ΔH>0,测得反应物X浓度与反应时间的数据如下表:| 反应时间t/min | 0 | 1 | 2 | 3 | 4 | 6 | 8 |
| c(X)/mol·L-1 | 0.60 | 0.42 | 0.30 | 0.21 | 0.15 | a | 0.037 5 |
(2)分析该反应中反应物的浓度与时间的规律,得出的结论是
由此规律推出反应在6 min时反应物的浓度a为
您最近一年使用:0次



