26. CH
4、H
2、C都是优质的能源物质,它们燃烧的热化学方程式分别为
①CH
4(g)+2O
2(g)=CO
2(g)+2H
2O(l)
△H=-890.3kJ•mol
-1,
②2H
2(g)+O
2(g)=2H
2O(l) △
H=-571.6kJ•mol
-1③C(s)+O
2(g)=CO
2(g)
△H=-393.5kJ•mol
-1(1)在深海中存在一种甲烷细菌,它们依靠甲烷与O
2在酶的催化作用下产生的能量存活,在甲烷细菌使1mol甲烷转化为CO
2气体与液态水的过程中,放出的能量
___(填“>”“<”或“=”)890.3kJ。
(2)甲烷与CO
2可用于生产合成气(主要成分是一氧化碳和氢气):CH
4(g)+CO
2(g)=2CO(g)+2H
2(g),1gCH
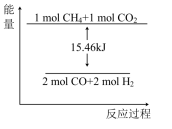
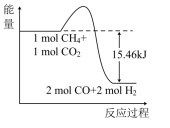
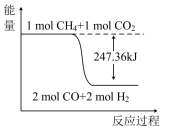
4完全反应可释放15.46kJ的热量。则:
①如图能表示该反应过程的能量变化的是
____(填序号)。
A.
B.

C.
D.
②若将物质的量均为1mol的CH
4与CO
2充入某恒容密闭容器中,体系放出的热量随着时间的变化曲线如图所示,则CH
4的转化率为
___。

(3)C(s)与H
2(g)很难发生反应,所以C(s)+2H
2(g)=CH
4(g)的反应热无法直接测量,但通过上述反应可求出C(s)+2H
2(g)=CH
4(g)的反应热
△H=
____。
(4)目前对题干所述的三种物质的研究是燃料研究的重点,下列关于这三种物质的研究方向中可行的是
____(填序号)。
A.寻找优质催化剂,使CO
2与H
2O反应生成CH
4与O
2,并放出热量
B.寻找优质催化剂,在常温常压下使CO
2分解生成碳与O
2C.寻找优质催化剂,利用太阳能使大气中的CO
2与海底开采的CH
4反应生产合成气(CO、H
2)
D.用固态碳合成C
60,以C
60作为燃料