8. 中和热的测定是高中重要的定量实验。某实验小组用0.8 mol·L
-1NaOH溶液和0.3 mol·L
-1硫酸溶液进行中和热的测定。回答下列问题:
Ⅰ.配制0.3 mol/L硫酸溶液
(1)实验中大约要使用238 mL硫酸溶液,需要量取15 mol·L
-1硫酸溶液的体积为
_______。
(2)若定容时俯视刻度线,则所配浓度将
____________(填“增大、减小、或不变”)。
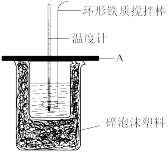
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
(3)如图有无错误,若无,此小题不用作答。若有,请说明错误的原因
___________。
(4)取40 mL NaOH溶液和50 mL硫酸溶液进行实验,实验数据如表:
温度
实验次数 | 起始温度t1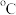 | 终止温度t2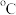 |
H2SO4 | NaOH |
1 | 26.2 | 26.0 | 29.5 |
2 | 27.0 | 27.4 | 32.3 |
3 | 25.9 | 25.9 | 29.2 |
4 | 26.4 | 26.2 | 29.8 |
已知: 0.8mol/L NaOH溶液和0.3 mol/L硫酸溶液的密度都是1 g/cm
3,中和后生成溶液的比热容c=4.18J/(g·℃)。则中和热ΔH=
 _______
_______。
(5)上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是
_______(填字母)。
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计量0.3 mol/L硫酸溶液的温度后立即量0.8mol/L NaOH溶液的温度
Ⅲ. 学生用2 mol/L的硫酸来测定与锌粒和锌粉反应的快慢,设计如图(Ⅰ)装置:
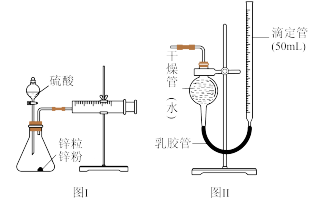
(6)该生两次实验测定时间均设定为10 min,那么他还
要测定的另一个数据是
____________________。
(7)如果将图Ⅰ装置中的气体收集装置改为图Ⅱ,实验完毕待冷却后,该生准备读取滴定管上液面所处刻度数,发现滴定管中液面高于干燥管中液面,应先采取的操作是
_________________________。
(8)该实验中,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的
_______。
A.甲酸钠固体
B.KNO
3溶液
C.KCl溶液
D.NaHCO
3溶液
E.CuCl
2溶液