19. 在一定条件下,二氧化硫和氧气发生如下反应:2SO
2(g)+O
2(g)
⇌2SO
3(g) △H<0;
(1)写出该反应的化学平衡常数表达式K=
__________(2)降低温度,该反应K值
__________,二氧化硫转化率
___________,化学反应速率
___________(以上均填增大、减小或不变)。
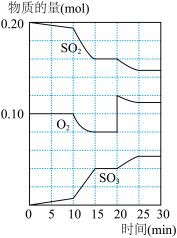
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO
2、O
2、SO
3物质的量变化如图,反应处于平衡状态时间是
___________________________。
(4)据图判断,反应进行至20min时,曲线发生变化的原因是
_______________________(用文字表达)。
(5)10min到15min的曲线变化的原因可能是
____________(填写编号)。
A、加了催化剂
B、缩小容器体积
C、降低温度
D、增加SO
3的物质的量。
(6)若该反应的密闭容器为2L,则反应15min时,v(SO
2)=
___________(7)为使该反应的反应速率增大,且平衡向正反应方向移动的是
( )A、及时分离出SO
3气体
B、适当升高温度
C、增大O
2的浓度
D、选择高效的催化剂