18. (1)一定条件下,向容积为2L的恒容密闭容器中充入1 mol CH
3OH(g)和3 mol H
2O(g),CH
3OH(g) + H
2O(g)

CO
2(g) + 3H
2(g)
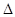
H(298K)=+ 49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
①达平衡时混合气体的压强是反应前的
__________倍。
②该条件下反应达平衡状态的依据是(填序号)
_____________。
| A.v正(CH3OH)=v正(CO2) | B.混合气体的密度不变 |
| C.c(CH3OH)=c(H2O) | D.混合气体的总物质的量不变 |
(2)在25 ℃、101 kPa下,1 g甲醇燃烧生成CO
2和液态水时放热Q kJ。则表示甲醇燃烧热的热化学方程式为
_____________________。
(3)对于H
2O
2分解反应,Cu
2+也有一定的催化作用。为比较Fe
3+和Cu
2+对H
2O
2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
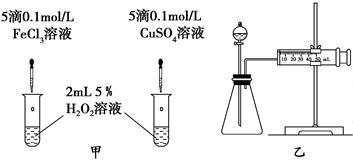
①定性分析:如图甲可通过观察
__________________,定性比较得出结论。有同学提出将FeCl
3改为Fe
2(SO
4)
3更为合理,其理由是
___________。
②定量分析:用图乙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是
________________,实验中需要测量的数据是
___________________。