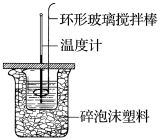
16. 利用如图所示装置测定中和热的实验步骤如下:
①用量筒量取50 mL 0.50 mol·L
-1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50 mL 0.55 mol·L
-1 NaOH溶液,并用同一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。回答下列问题:
(1)为什么所用NaOH溶液要稍过量?
_______。
(2)倒入NaOH溶液的正确操作是
_______(填序号)。
A.沿玻璃棒缓慢倒入
B.分三次少量倒入
C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是_______(填序号)。
| A.用温度计小心搅拌 |
| B.揭开硬纸片用玻璃棒搅拌 |
| C.轻轻地振荡烧杯 |
| D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动 |
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1 L 1 mol·L
-1的稀盐酸恰好完全反应,其反应热分别为ΔH
1、ΔH
2、ΔH
3,则ΔH
1、ΔH
2、ΔH
3的大小关系为
_______。
(5)假设盐酸和氢氧化钠溶液的密度都是1 g·cm
-3,又知中和反应后生成溶液的比热容c=4.18 J·g
-1·℃
-1.为了计算中和热,某学生实验记录数据如下:
| 起始温度t1/℃ | 终止温度t2/℃ |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=
_______(结果保留一位小数)。
(6)
_______(填“能”或“不能”)用Ba(OH)
2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是
_______。