11. 实验小组制备高铁酸钾(K
2FeO
4)并探究其性质。
资料:K
2FeO
4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O
2,在碱性溶液中较稳定。
(1)制备K
2FeO
4(夹持装置略)
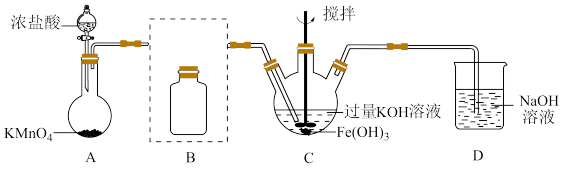
①A为氯气发生装置。A中反应方程式是
________________(锰被还原为Mn
2+)。
②将除杂装置B补充完整并标明所用试剂。
_______③C中得到紫色固体和溶液,C中Cl
2发生的反应有
3Cl
2+2Fe(OH)
3+10KOH

2K
2FeO
4+6KCl+8H
2O,另外还有
________________。
(2)探究K
2FeO
4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl
2。为证明是否K
2FeO
4氧化了Cl
-而产生Cl
2,设计以下方案:
| 方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
Ⅰ.由方案Ⅰ中溶液变红可知a中含有
______离子,但该离子的产生不能判断一定是K
2FeO
4将Cl
-氧化,还可能由
________________产生(用方程式表示)。
Ⅱ.方案Ⅱ可证明K
2FeO
4氧化了Cl
-。用KOH溶液洗涤的目的是
________________。
②根据K
2FeO
4的制备实验得出:氧化性Cl
2________
(填“>”或“<”),而方案Ⅱ实验表明,Cl
2和

的氧化性强弱关系相反,原因是
________________。
③资料表明,酸性溶液中的氧化性

>

,验证实验如下:将溶液b滴入MnSO
4和足量H
2SO
4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性

>

。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
________________。