21. 入冬以来,太原市为减少“雾霾”的发生,开始对机动车限号行驶。“雾霾”中含有二氧化硫、氮氧化物和可吸入颗粒物等污染性物质。请回答下列问题:
(1)汽车尾气中的主要污染物为NO,用H
2催化还原NO可以达到消除污染的目的。
已知:①2NO(g)

N
2(g)+O
2(g) ΔH=-180.5 kJ·mol
-1②2H
2O(l)=2H
2(g)+O
2(g) ΔH=+571.6 kJ·mol
-1写出H
2(g)与NO(g)反应生成N
2(g)和H
2O(l)的热化学方程式
__________________。
(2)用焦炭还原NO的反应为2NO(g)+C(s)

N
2(g)+CO
2(g),向容积均为2 L的甲、乙两个恒容恒温(反应温度分别为400 ℃、T ℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间(t)的变化情况如下表所示:
| t/min | 0 | 40 | 80 | 120 | 160 |
| n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO)(乙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
①该反应为
________(填“放热”或“吸热”)反应。
②求400 ℃下该反应的平衡常数
__________。
(3)在一定条件下,将NO和O
3通入绝热恒容密闭容器中发生反应NO(g)+O
3(g)

NO
2(g)+O
2(g),正反应速率随时间的变化如图所示。下列说法正确的是
______。

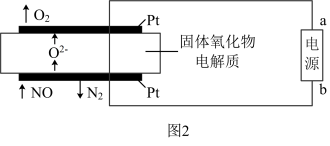
A.反应在c点达到平衡状态
B.反应物浓度:b点小于c点
C.反应物的总能量低于生成物的总能量
D.Δt
1=Δt
2时,NO的转化量:a~b段小于b~c段
(4)园园老师带领研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na
2SO
3溶液进行电解,其中阴、阳膜组合电解装置如图所示,电极材料为石墨。
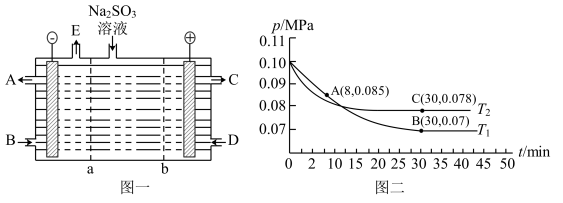
①a表示
________(填“阴”或“阳”)离子交换膜。A~E分别代表生产中的原料或产品,其中C为硫酸,则A表示
________。
②阳极的电极反应式为
______________。