17. 肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N
2H
4·H
2O)。
已知:N
2H
4·H
2O高温易分解,易氧化
制备原理:CO(NH
2)
2+2NaOH+NaClO=Na
2CO
3+N
2H
4·H
2O+NaCl
【实验一】 制备NaClO溶液(实验装置如图所示
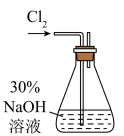
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外,还有
_____(填标号)
A.容量瓶
B.烧杯
C.烧瓶
D.玻璃棒
(2)锥形瓶中发生反应化学程式是
_____________________________。
【实验二】 制取水合肼。(实验装置如图所示)
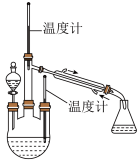
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108-114馏分。
(3)分液漏斗中的溶液是
____________(填标号)。
A.CO(NH
2)
2溶液
B.NaOH和NaClO混合溶液
选择的理由是
____________。蒸馏时需要减压,原因是
______________。
【实验三】 测定馏分中肼含量。
(4)水合肼具有还原性,可以生成氮气。测定水合肼的质量分数可采用下列步骤:
a.称取馏分5.000g,加入适量NaHCO
3固体(保证滴定过程中溶液的pH保持在6.5左右),配制1000mL溶液。
b.移取10.00 mL于锥形瓶中,加入10mL水,摇匀。
c.用0.2000mol/L碘溶液滴定至溶液出现
______________,记录消耗碘的标准液的体积。
d.进一步操作与数据处理
(5)滴定时,碘的标准溶液盛放在
______________滴定管中(选填:“酸式”或“碱式”)水合肼与碘溶液反应的化学方程式
________________________。
(6)若本次滴定消耗碘的标准溶液为8.20mL,馏分中水合肼(N
2H
4·H
2O)的质量分数为
______。