19. 汽车尾气中含有上百种不同的化合物,其中的污染物有固体悬浮微粒、一氧化碳、二氧化碳、碳氢化合物、氮氧化合物等。汽车尾气是城市主要空气污染物,汽车内燃机工作时发生反应:N
2(g) + O
2(g)
⇌ 2NO(g),是导致汽车尾气中含有 NO 的原因之一。
(1)已知H
2或 CO 可以催化还原 NO 以达到消除污染的目的。
N
2(g) + O
2(g) = 2NO(g) ΔH = + 180.5 kJ·mol-1
2H
2(g) + O
2(g) = 2H
2O(l) ΔH = - 571.6 kJ·mol-1
写出H
2(g)与NO(g)反应生成 N
2(g)和H
2O(l)的热化学方程式是
________, 判断该反应自发进行的条件:
_____(填“高温自发”或“低温自发”)。
(2)当质量一定时,增大固体催化剂的表面积可提高化学反应速率。如图表示在其他条件不变时,反应 2NO(g) + 2CO(g)

2CO
2(g) + N
2(g) 中 NO 的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
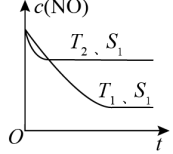
①则该反应 ΔH
_____0(填“>”或“<”)。
②若催化剂的表面积 S
1 > S
2,在该图中画出 c(NO)在 T
1、S
2条件下达到平衡过程中的变化曲线
_____________。
(3)某研究小组往一恒温恒压容器充入 9 mol N
2和 23 mol H
2模拟合成氨反应,下图为不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系图。若体系在 T
2、60 MPa 下达到平衡。
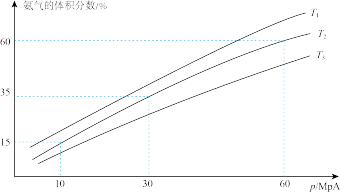
此时N
2的平衡分压为
_____MPa。(分压 = 总压 × 物质的量分数)。计算出此时的平衡常数 Kp =
_____(用平衡分压代替平衡浓度计算,结果保留 2 位有效数字)。