9. 环戊二烯(

)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
(1)已知:

(g)=

(g)+H
2(g)
Δ
H1=100.3 kJ·mol
−1 ①
H
2(g)+ I
2(g)=2HI(g)
Δ
H2=﹣11.0 kJ·mol
−1 ②
对于反应:
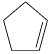
(g)+ I
2(g)=
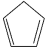
(g)+2HI(g)
③
Δ
H3=
___________kJ·mol
−1。
(2)某温度下,等物质的量的碘和环戊烯(

)在刚性容器内发生反应③,起始总压为10
5Pa,平衡时总压增加了20%,环戊烯的转化率为
_________,该反应的平衡常数
Kp=
_________Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有
__________(填标号)。
A.通入惰性气体
B.提高温度
C.增加环戊烯浓度
D.增加碘浓度
(3)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是
__________(填标号)。

A.
T1>
T2B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L
−1(4)环戊二烯可用于制备二茂铁(Fe(C
5H
5)
2结构简式为

),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
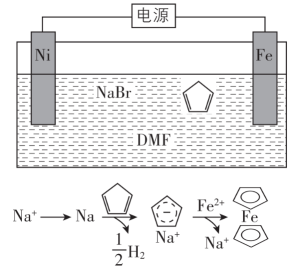
该电解池的阳极为
____________,总反应为
__________________。电解制备需要在无水条件下进行,原因为
_________________________。