18. (1)用焦炭还原NO
2的反应为:2NO
2(g)+2C(s)

N
2(g)+2CO
2(g),在恒温条件下,1 mol NO
2和足量C发生该反应,测得平衡时NO
2和CO
2的物质的量浓度与平衡总压的关系如图所示:
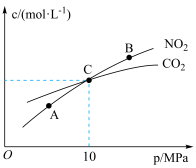
①A、B两点的浓度平衡常数关系:
Kc(A)_____Kc(B)(填“﹥”、“<”或“﹦”)。
②A、B、C三点中NO
2的转化率最高的是
_____(填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数
Kp(C)=
______(
Kp是用平衡分压代替平衡浓度计算,分压=总压物质的量分数)。
(2)对于可逆反应Fe(s)+CO
2(g)

FeO(s)+CO(g),该反应的逆反应速率随时间变化的关系如图所示。
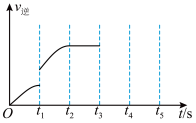
①从图中看到,反应在
t2时达平衡,在
t1时改变了某种条件,改变的条件可能是
________。
A.升温
B.增大CO
2浓度
C.使用催化剂
②如果在
t3时从混合物中分离出部分CO,
t4~
t5时间段反应处于新平衡状态,请在图上画出
t3~
t5的
v(逆)变化曲线。
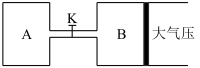
_________(3)如下图所示,当关闭K时,向A中充入2 mol X、7 mol Y,向B中充入4 mol X、14 mol Y,起始时
V(A)=
V(B)=a L,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g)

Z(g)+2W(g)
△H<0达到平衡(Ⅰ)时
V(B)=0.9a L,试回答:
①B中X的转化率α(X)
B为
_________________________;
②打开K,过一段时间重新达平衡(Ⅱ)时,B的体积为
__________________L(用含a的代数式表示,连通管中气体体积不计)。