19. 如何降低大气中CO
2的含量及有效地开发利用CO
2引起了全世界的普遍重视。目前工业上有一种方法是用CO
2来生产燃料甲醇。为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入1molCO
2和3molH
2。在500℃下发生发应,CO
2(g)+3H
2(g)

CH
3OH(g)+H
2O(g)。实验测得CO
2和CH
3OH(g)的物质的量(n)随时间变化如下图1所示:
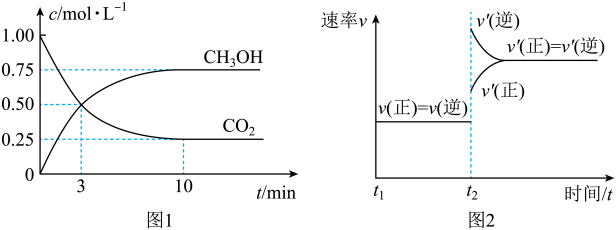
(1)从反应开始到平衡,氢气的平均反应速率v(H
2)=
________。
(2)500℃该反应的平衡常数为
_____(结果保留一位小数),图2是改变温度时化学反应速率随时间变化的示意图,若提高温度到800℃进行,达平衡时,K值
_____(填“增大”“减小”或“不变”)。
(3)下列措施中不能使CO
2的转化率增大的是
_______。
A 在原容器中再充入1mol H
2 B 在原容器中再充入1molCO
2C 缩小容器的容积
D 使用更有效的催化剂
E 将水蒸气从体系中分离出
(4)500℃条件下,测得某时刻,CO
2(g)、H
2(g)、CH
3OH(g)和H
2O(g)的浓度均为0.5mol/L,则此时v(正)
____ v(逆)(填“>”“<”或“=”)。