19. 氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用。
Ⅰ.联氨(N
2H
4,常温下是无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)已知12.8 g的液态高能燃料联氨在氧气中燃烧,生成气态N
2和液态水,放出248.8kJ的热量。写出表示液态联氨燃烧热的热化学方程式
_____________。
(2)已知①2O
2(g)+N
2(g)=N
2O
4(l) Δ
H1②N
2(g)+2H
2(g)=N
2H
4(l) Δ
H2③O
2(g)+2H
2(g)=2H
2O(g) Δ
H3④2 N
2H
4(l) + N
2O
4(l)= 3N
2(g)+ 4H
2O(g) Δ
H4=-1048.9kJ/mol
上述反应热效应之间的关系式为Δ
H4=
___________Ⅱ.对反应N
2O
4(g)
⇌2NO
2(g)
△H > 0 ,在温度分别为
T1、
T2时,平衡体系中NO
2的体积分数随压强变化曲线如图所示,下列说法正确的是
______。
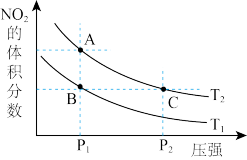
A. A、C两点的反应速率:A>C
B. A、C两点的化学平衡常数:A>C
C. A、C两点N
2O
4的转化率:A>C
D. 由状态B到状态A,可以用加热的方法
Ⅲ.一定温度下,在2L密闭容器中充入1molN
2和3molH
2并发生反应。若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的
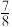
,则N
2的转化率

(N
2)=
_____________, 此时NH
3的浓度为
______________。