某温度下,在恒容密闭容器中发生可逆反应的平衡常数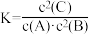 ,当反应达到平衡时,n(A) : n(B) : n(C) = 2 : 2 : 1。若保持温度不变,以2 : 2 : 1的物质的量之比再充入A、B、C,则下列说法正确的是
,当反应达到平衡时,n(A) : n(B) : n(C) = 2 : 2 : 1。若保持温度不变,以2 : 2 : 1的物质的量之比再充入A、B、C,则下列说法正确的是
| A.K值增大 | B.达到新平衡后,C的体积分数增大 |
| C.平衡不移动 | D.达到新平衡后,v逆(A)比原平衡小 |
更新时间:2020-10-27 19:21:04
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】恒温、恒压下,反应N2 (g)+3H2 (g)  2NH3 (g)从两条途径分别建立平衡:
2NH3 (g)从两条途径分别建立平衡:
Ⅰ.N2、H2的起始浓度分别为1 mol / L和3 mol / L;
Ⅱ.NH3的起始浓度为4 mol / L。下列有关叙述不正确的是:
 2NH3 (g)从两条途径分别建立平衡:
2NH3 (g)从两条途径分别建立平衡:Ⅰ.N2、H2的起始浓度分别为1 mol / L和3 mol / L;
Ⅱ.NH3的起始浓度为4 mol / L。下列有关叙述不正确的是:
| A.途径Ⅰ与途径Ⅱ所得混合气体的百分组成相同 |
| B.途径Ⅰ的平衡速率v (N2)与途径Ⅱ的平衡速率v (NH3)的比值为1∶2 |
| C.途径Ⅰ所得NH3的浓度与途径Ⅱ所得NH3的浓度之比为1∶2 |
| D.途径Ⅰ与途径Ⅱ所得平衡混合气体的物质的量之比为1∶2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,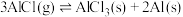 .在密闭容器中投入足量的
.在密闭容器中投入足量的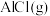 ,一定温度下发生上述反应,达到平衡后
,一定温度下发生上述反应,达到平衡后 ,保持温度不变,将体积缩小至原来的三分之一且保持体积不变,达到第二次平衡.下列叙述不正确的是
,保持温度不变,将体积缩小至原来的三分之一且保持体积不变,达到第二次平衡.下列叙述不正确的是
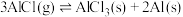 .在密闭容器中投入足量的
.在密闭容器中投入足量的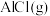 ,一定温度下发生上述反应,达到平衡后
,一定温度下发生上述反应,达到平衡后 ,保持温度不变,将体积缩小至原来的三分之一且保持体积不变,达到第二次平衡.下列叙述不正确的是
,保持温度不变,将体积缩小至原来的三分之一且保持体积不变,达到第二次平衡.下列叙述不正确的是A.达到第二次平衡时, |
| B.整个过程中平衡常数保持不变 |
| C.第二次平衡与第一次平衡时相比:气体密度增大 |
D.第二次平衡与第一次平衡时相比: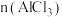 增大 增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】对于平衡体系mA(g)+nB(g) pC(g)+qD(g) △H<0。下列结论中正确的是
pC(g)+qD(g) △H<0。下列结论中正确的是
 pC(g)+qD(g) △H<0。下列结论中正确的是
pC(g)+qD(g) △H<0。下列结论中正确的是| A.若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的1.8倍,则m+n<p+q |
| B.反应达平衡时,A、B的转化率一定相等 |
| C.若m+n=p+q,则往含有amol气体的平衡体系中再加入amol的B,达到新平衡时,气体的总物质的量等于2amol |
D.若温度不变,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的 要小 要小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列事实中,不能用勒夏特列原理解释的是
| A.氯水应密闭避光保存,放置于阴凉处 |
| B.工业合成氨气过程中,使用过量的氮气,以提高氢气利用率 |
| C.对2HI(g)⇌H2(g)+I2(g)平衡体系,增大平衡体系的压强可使气体颜色变深 |
| D.溴水中有下列平衡Br2+H2O⇌HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
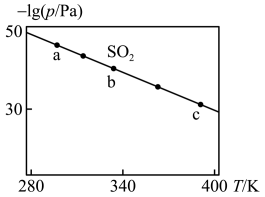
【推荐1】煤燃烧排放的烟气中含有SO2,SO2易形成酸雨,污染大气。采用NaClO2溶液作为吸收剂可对烟气进行脱硫,发生如下反应: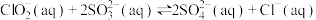
 。在不同温度下,测得反应中SO2的压强变化如图所示,下列说法错误的是
。在不同温度下,测得反应中SO2的压强变化如图所示,下列说法错误的是
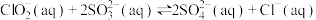
 。在不同温度下,测得反应中SO2的压强变化如图所示,下列说法错误的是
。在不同温度下,测得反应中SO2的压强变化如图所示,下列说法错误的是
| A.△H<0 |
B.该反应的平衡常数表达式为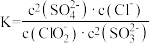 |
| C.减小压强,有利于该反应朝正反应方向进行 |
| D.平衡常数:K(a)>K(b)>K(c) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】氮氧化物与悬浮在大气中海盐粒子的相互反应:4NO2(g)+2NaCl(s)  2NaNO3(s)+2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g)  在恒温条件下,向2L恒容密闭容器中加入0.4molNO2和0.2molNaCl,10min反应达到平衡时n(NaNO3)=0.1mol,NO2的转化率为
在恒温条件下,向2L恒容密闭容器中加入0.4molNO2和0.2molNaCl,10min反应达到平衡时n(NaNO3)=0.1mol,NO2的转化率为 。下列叙述中正确的是
。下列叙述中正确的是
 2NaNO3(s)+2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g)  在恒温条件下,向2L恒容密闭容器中加入0.4molNO2和0.2molNaCl,10min反应达到平衡时n(NaNO3)=0.1mol,NO2的转化率为
在恒温条件下,向2L恒容密闭容器中加入0.4molNO2和0.2molNaCl,10min反应达到平衡时n(NaNO3)=0.1mol,NO2的转化率为 。下列叙述中正确的是
。下列叙述中正确的是| A.10min内NO浓度变化表示的速率υ(NO)=0.01mol·L-1·min-1 |
B.若升高温度,平衡逆向移动,则该反应的 |
| C.若起始时向该容器中充入0.1molNO2(g)、0.2molNO(g)和0.1molCl2(g)(固体物质足量),则反应将向逆反应方向进行 |
D.若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率小于 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】在10 L的恒容密闭容器中通入X(g)和Y(g),发生反应X(g)+Y(g) M(g)+N(g),所得实验数据如下表所示:
M(g)+N(g),所得实验数据如下表所示:
下列说法正确的是
 M(g)+N(g),所得实验数据如下表所示:
M(g)+N(g),所得实验数据如下表所示:实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.40 | 0.10 | 0.090 |
② | 800 | 0.10 | 0.40 | 0.080 |
③ | 800 | 0.20 | 0.30 | a |
④ | 900 | 0.15 | 0.20 | b |
A.实验①中,该反应的平衡常数K=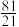 |
| B.实验②中,若5 min时测得n(N)=0.050 mol,则0~5 min内,用X表示的平均反应速率v(X)=7×10-3 mol·L-1·min-1 |
| C.实验③中,反应达到平衡时,Y的转化率为40% |
D.实验④中,反应达到平衡时,b>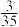 |
您最近一年使用:0次

 和1mol
和1mol  分别置于相同温度下相同体积的甲乙两密闭容器中发生反应:
分别置于相同温度下相同体积的甲乙两密闭容器中发生反应: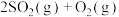
 并达到平衡,甲容器始终保持恒温恒容,乙容器始终保持恒温恒压,达到平衡时,下述说法不正确的是
并达到平衡,甲容器始终保持恒温恒容,乙容器始终保持恒温恒压,达到平衡时,下述说法不正确的是 的百分含量:乙<甲
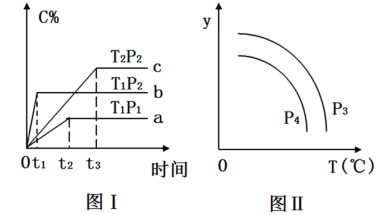
的百分含量:乙<甲 xC(g),C的体积分数(C%)跟温度(T)和压强(p)的关系如图I所示。下列对图II的说法正确的是
xC(g),C的体积分数(C%)跟温度(T)和压强(p)的关系如图I所示。下列对图II的说法正确的是