2024高三·全国·专题练习
1 . H2S和CO2反应生成的羰基硫(COS)可用于粮食熏蒸,能防止某些昆虫、线虫和真菌的危害,反应热化学方程式为:CO2(g)+H2S(g) COS(g)+H2O(g);ΔH>0.下列说法正确的是
COS(g)+H2O(g);ΔH>0.下列说法正确的是
 COS(g)+H2O(g);ΔH>0.下列说法正确的是
COS(g)+H2O(g);ΔH>0.下列说法正确的是| A.上述反应中消耗34 g H2S,生成22.4 L水蒸气 |
B.上述反应的平衡常数K=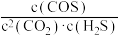 |
| C.已知该反应在加热条件下能自发进行,则其ΔS>0 |
| D.实际应用中,通过增加H2S的量来提高CO2的转化率,能有效减少碳排放 |
您最近半年使用:0次
2 . 工业上常用 和
和 为原料合成甲醇
为原料合成甲醇 ,过程中发生如下反应:
,过程中发生如下反应: 。在
。在 温度下,向
温度下,向 刚性容器中充入
刚性容器中充入 和一定物质的量的
和一定物质的量的 ,随着充入
,随着充入 的物质的量的不同,平衡时容器中
的物质的量的不同,平衡时容器中 的体积分数变化曲线如图所示。下列说法错误的是
的体积分数变化曲线如图所示。下列说法错误的是
 和
和 为原料合成甲醇
为原料合成甲醇 ,过程中发生如下反应:
,过程中发生如下反应: 。在
。在 温度下,向
温度下,向 刚性容器中充入
刚性容器中充入 和一定物质的量的
和一定物质的量的 ,随着充入
,随着充入 的物质的量的不同,平衡时容器中
的物质的量的不同,平衡时容器中 的体积分数变化曲线如图所示。下列说法错误的是
的体积分数变化曲线如图所示。下列说法错误的是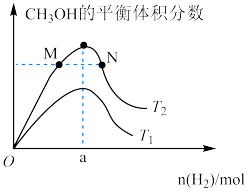
A. | B. |
C.平衡常数 | D.该反应在高温高压条件下自发进行 |
您最近半年使用:0次
3 . 在一定容积的密闭容器中,进行如下化学反应: ,其化学平衡常数K和温度T的关系如表所示:
,其化学平衡常数K和温度T的关系如表所示:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=____________ 。
(2)该反应为________ (填“吸热”或“放热”)反应。
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________ ℃。该温度下加入1 mol CO2(g)和1 mol H2(g),充分反应,达到平衡时,CO2的转化率为________ 。
 ,其化学平衡常数K和温度T的关系如表所示:
,其化学平衡常数K和温度T的关系如表所示:T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=
(2)该反应为
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
您最近半年使用:0次
名校
解题方法
4 . 一定条件下CO2与NH3合成尿素:2NH3(g)+CO2(g)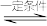 CO(NH2)2(s)+H2O(l) ΔH,其反应过程中能量变化如图所示,下列有关说法正确的是
CO(NH2)2(s)+H2O(l) ΔH,其反应过程中能量变化如图所示,下列有关说法正确的是
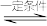 CO(NH2)2(s)+H2O(l) ΔH,其反应过程中能量变化如图所示,下列有关说法正确的是
CO(NH2)2(s)+H2O(l) ΔH,其反应过程中能量变化如图所示,下列有关说法正确的是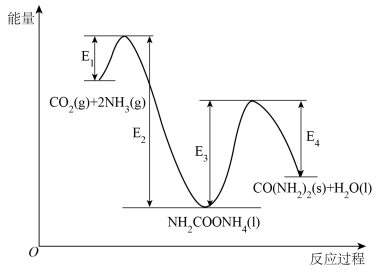
| A.ΔH>0 |
B.该反应平衡常数K=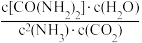 |
| C.升高温度,可分离得到更多的NH2COONH4(l) |
| D.合成尿素的反应快慢主要取决于NH2COONH4(l)的分解速率 |
您最近半年使用:0次
名校
解题方法
5 . 对于反应2SO2(g)+O2(g) 2SO3(g) ΔH<0,在其他条件相同时,下列说法正确的是
2SO3(g) ΔH<0,在其他条件相同时,下列说法正确的是
 2SO3(g) ΔH<0,在其他条件相同时,下列说法正确的是
2SO3(g) ΔH<0,在其他条件相同时,下列说法正确的是| A.增大压强,平衡正向移动,化学平衡常数增大 |
| B.加入V2O5,改变了反应的活化能,平衡不发生移动 |
| C.升高温度,v(逆)增大,v(正)减小,平衡逆向移动 |
| D.当c(SO2)∶c(O2)=2∶1时,可以判断该反应一定已经达到化学平衡 |
您最近半年使用:0次
名校
解题方法
6 . 研究二氧化碳的转化是实现“双碳”目标的途径之一。可通过电化学、热化学等方法,将 转化为
转化为 等化学品。现有反应过程如下:
等化学品。现有反应过程如下:
①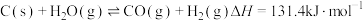
②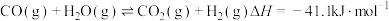
(1)写出 的结构式
的结构式___________ ,写出 的电离方程式
的电离方程式___________ 。
(2)反应①的平衡常数表达式
___________ 。
 转化为
转化为 等化学品。现有反应过程如下:
等化学品。现有反应过程如下:①
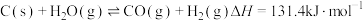
②
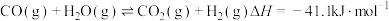
(1)写出
 的结构式
的结构式 的电离方程式
的电离方程式(2)反应①的平衡常数表达式

您最近半年使用:0次
解题方法
7 . 利用 干重整反应:
干重整反应: ,不仅可以对天然气资源综合利用,还可以缓解温室效应对环境的影响。
,不仅可以对天然气资源综合利用,还可以缓解温室效应对环境的影响。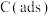 为吸附活性炭,该反应一般认为通过如图步骤来实现:
为吸附活性炭,该反应一般认为通过如图步骤来实现:
 干重整反应:
干重整反应: ,不仅可以对天然气资源综合利用,还可以缓解温室效应对环境的影响。
,不仅可以对天然气资源综合利用,还可以缓解温室效应对环境的影响。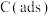 为吸附活性炭,该反应一般认为通过如图步骤来实现:
为吸附活性炭,该反应一般认为通过如图步骤来实现: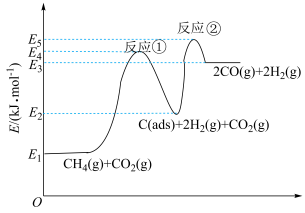
| A.反应①、②在高温条件下均能自发进行 |
| B.该反应速率主要由反应①决定 |
C.该反应的平衡常数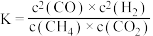 |
D.该反应中每产生 ,转移电子的数目约为 ,转移电子的数目约为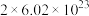 |
您最近半年使用:0次
名校
8 . 哈伯法合成氨的反应原理为 ,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是
,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是
 ,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是
,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是A.该反应在低温下能自发进行,则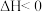 |
B.选用高效催化剂,可降低该反应的 |
C.其它条件不变,增大起始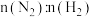 的比值,可提高N2的平衡转化率 的比值,可提高N2的平衡转化率 |
| D.提高体系的压强可增大反应的化学平衡常数 |
您最近半年使用:0次
名校
解题方法
9 . 亚硝酰氯(NOCl)是有机合成试剂,实验室中可用反应(I)进行合成:
 。
。
(1)在常温下,常用高锰酸钾和浓盐酸反应制备氯气,反应的离子方程式为___________ 。
(2)已知几种物质的相对能量如下:
根据表格中数据估算上述反应(I)的反应热
___________  。
。
(3) ,可逆反应
,可逆反应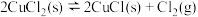 用气体物质的分压表示的平衡常数
用气体物质的分压表示的平衡常数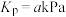 。(提示:分压=总压
。(提示:分压=总压 该物质的物质的量分数)
该物质的物质的量分数) 下,在某真空容器中加入足量的
下,在某真空容器中加入足量的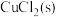 并充入
并充入 ,测得起始压强为
,测得起始压强为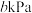 ,发生上述反应(I)达到平衡时测得
,发生上述反应(I)达到平衡时测得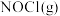 的压强为
的压强为 。平衡时
。平衡时 的转化率为
的转化率为___________ ;该温度下,反应(I)的平衡常数
___________  。
。
(4) 的速率方程可表示为:
的速率方程可表示为: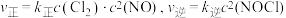 ,其中
,其中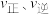 表示正、逆反应速率,k正、k逆表示正、逆反应的速率常数,只与温度、催化剂、接触面有关,与浓度无关。
表示正、逆反应速率,k正、k逆表示正、逆反应的速率常数,只与温度、催化剂、接触面有关,与浓度无关。
①上述反应(I)的平衡常数
___________ (用k正、k逆表示)。
②加入催化剂,k正增大的倍数___________ (填“大于”“小于”或“等于”)k逆增大的倍数。
③已知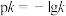 ,当温度降低时,如图所示中的2条直线代表
,当温度降低时,如图所示中的2条直线代表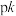 与
与 关系,其中代表pk正与
关系,其中代表pk正与 关系的是直线
关系的是直线___________ (填字母)。判断理由是___________ 。

 。
。(1)在常温下,常用高锰酸钾和浓盐酸反应制备氯气,反应的离子方程式为
(2)已知几种物质的相对能量如下:
| 物质 | Cl2 | NO(g) | NOCl(g) |
| 相对能量/kJ·mol—1 | 0 | 90.25 | 51.71 |

 。
。(3)
 ,可逆反应
,可逆反应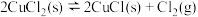 用气体物质的分压表示的平衡常数
用气体物质的分压表示的平衡常数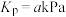 。(提示:分压=总压
。(提示:分压=总压 该物质的物质的量分数)
该物质的物质的量分数) 下,在某真空容器中加入足量的
下,在某真空容器中加入足量的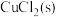 并充入
并充入 ,测得起始压强为
,测得起始压强为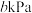 ,发生上述反应(I)达到平衡时测得
,发生上述反应(I)达到平衡时测得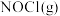 的压强为
的压强为 。平衡时
。平衡时 的转化率为
的转化率为
 。
。(4)
 的速率方程可表示为:
的速率方程可表示为: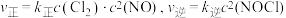 ,其中
,其中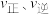 表示正、逆反应速率,k正、k逆表示正、逆反应的速率常数,只与温度、催化剂、接触面有关,与浓度无关。
表示正、逆反应速率,k正、k逆表示正、逆反应的速率常数,只与温度、催化剂、接触面有关,与浓度无关。①上述反应(I)的平衡常数

②加入催化剂,k正增大的倍数
③已知
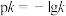 ,当温度降低时,如图所示中的2条直线代表
,当温度降低时,如图所示中的2条直线代表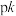 与
与 关系,其中代表pk正与
关系,其中代表pk正与 关系的是直线
关系的是直线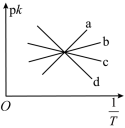
您最近半年使用:0次
名校
10 . 在盛有 载氧体的恒容密闭容器中充入空气[氧气的物质的量分数为
载氧体的恒容密闭容器中充入空气[氧气的物质的量分数为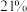 ],发生反应:
],发生反应: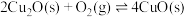
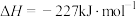 。平衡时氧气的物质的量分数
。平衡时氧气的物质的量分数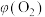 随反应温度
随反应温度 变化的曲线如图所示。下列说法错误的是
变化的曲线如图所示。下列说法错误的是
 载氧体的恒容密闭容器中充入空气[氧气的物质的量分数为
载氧体的恒容密闭容器中充入空气[氧气的物质的量分数为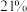 ],发生反应:
],发生反应: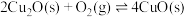
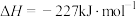 。平衡时氧气的物质的量分数
。平衡时氧气的物质的量分数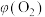 随反应温度
随反应温度 变化的曲线如图所示。下列说法错误的是
变化的曲线如图所示。下列说法错误的是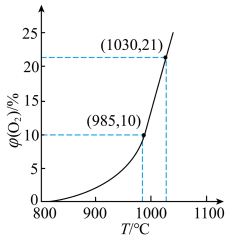
A.升高温度,平衡向逆反应方向移动导致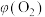 增大 增大 |
B.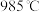 时达平衡后容器内总压为 时达平衡后容器内总压为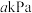 ,则此时反应的压强平衡常数为 ,则此时反应的压强平衡常数为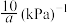 |
C.平衡时保持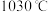 不变,向容器中充入等体积的空气,再次平衡后氧气物质的量浓度增大, 不变,向容器中充入等体积的空气,再次平衡后氧气物质的量浓度增大,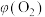 减小 减小 |
D.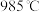 时 时 的平衡转化率 的平衡转化率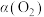 约为 约为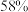 |
您最近半年使用:0次



