名校
1 . 向1L恒容密闭容器中加入 和一定量的
和一定量的 ,发生反应
,发生反应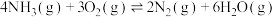 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比 随温度的变化曲线如图所示。下列说法正确的是
随温度的变化曲线如图所示。下列说法正确的是
 和一定量的
和一定量的 ,发生反应
,发生反应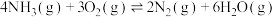 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比 随温度的变化曲线如图所示。下列说法正确的是
随温度的变化曲线如图所示。下列说法正确的是
A. |
B.反应速率: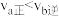 |
C.点a、b、c对应的平衡常数: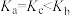 |
D.若 ,反应温度为 ,反应温度为 ,b点 ,b点 的物质的量分数约为26.6% 的物质的量分数约为26.6% |
您最近一年使用:0次
名校
2 . 乙酸水蒸气重整制氢气是一项极具前景的制氢工艺,该过程中发生下列反应:
反应Ⅰ:
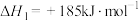
反应Ⅱ:

回答下列问题:
(1)反应Ⅰ在___________ 条件下能自发进行。
(2)已知:水碳比(S/C)是指转化进料中水蒸气分子总数与碳原子总数的比值,水碳比(S/C)分别为2和4时,反应温度对H2(g)平衡产率的影响如图1所示:___________ (填“a”或“b”);
②水碳比(S/C)=2时,H2(g)平衡产率随温度升高先增大后逐渐减小,H2(g)平衡产率逐渐减小的原因可能是___________ 。
(3)已知:S表示选择性,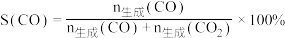 。在
。在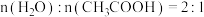 时,1 MPa下,平衡时S(CO)和S(CO2)随温度的变化;350℃下,平衡时S(CO)和S(CO2)随压强的变化均如图2所示。平衡常数随温度变化如图3所示
时,1 MPa下,平衡时S(CO)和S(CO2)随温度的变化;350℃下,平衡时S(CO)和S(CO2)随压强的变化均如图2所示。平衡常数随温度变化如图3所示___________ (填字母)。
②图中B、C、D、M、N、P、Q7个点中与A点处于相同化学平衡状态的点有___________ 个。
③在一定温度和压强下,向容积可变的密闭容器中通入2 mol H2O和1 mol CH3COOH,同时发生反应Ⅰ和反应Ⅱ达到平衡点C,测得平衡时体系中气体物质的量增加40%,则反应Ⅱ的
___________ (保留2位有效数字)。
反应Ⅰ:

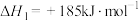
反应Ⅱ:


回答下列问题:
(1)反应Ⅰ在
(2)已知:水碳比(S/C)是指转化进料中水蒸气分子总数与碳原子总数的比值,水碳比(S/C)分别为2和4时,反应温度对H2(g)平衡产率的影响如图1所示:

②水碳比(S/C)=2时,H2(g)平衡产率随温度升高先增大后逐渐减小,H2(g)平衡产率逐渐减小的原因可能是
(3)已知:S表示选择性,
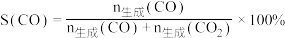 。在
。在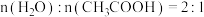 时,1 MPa下,平衡时S(CO)和S(CO2)随温度的变化;350℃下,平衡时S(CO)和S(CO2)随压强的变化均如图2所示。平衡常数随温度变化如图3所示
时,1 MPa下,平衡时S(CO)和S(CO2)随温度的变化;350℃下,平衡时S(CO)和S(CO2)随压强的变化均如图2所示。平衡常数随温度变化如图3所示
②图中B、C、D、M、N、P、Q7个点中与A点处于相同化学平衡状态的点有
③在一定温度和压强下,向容积可变的密闭容器中通入2 mol H2O和1 mol CH3COOH,同时发生反应Ⅰ和反应Ⅱ达到平衡点C,测得平衡时体系中气体物质的量增加40%,则反应Ⅱ的

您最近一年使用:0次
名校
解题方法
3 . 醛、酮与 可发生加成反应:
可发生加成反应: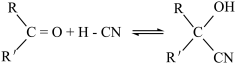 ,平衡常数为K。微量碱存在时的催化机理如下所示:
,平衡常数为K。微量碱存在时的催化机理如下所示:
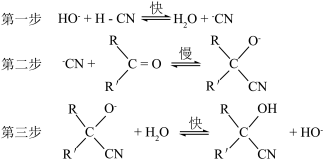
| -R | -R′ | 平衡常数K | |
| ① | -H |
| 210 |
| ② | -H |
| 530 |
| ③ | -CH3 | -CH2CH3 | 38 |
| ④ | -C(CH3)3 | -C(CH3)3 | ≪1 |
| A.HCN中C是sp杂化 |
| B.若将微量碱改成加入酸,则反应速率减慢 |
C.由①②可知推电子基团可以使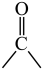 上的C原子活化,增大平衡常数 上的C原子活化,增大平衡常数 |
D.④的平衡常数小于③,可能是因为④中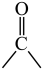 受到的空间位阻更大 受到的空间位阻更大 |
您最近一年使用:0次
名校
4 . 实验室常用 (铁氰化钾)检验
(铁氰化钾)检验 。一种制备铁氰化钾的流程如下:
。一种制备铁氰化钾的流程如下:
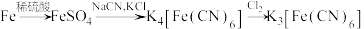
已知:

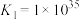
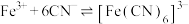
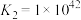
下列叙述错误的是
 (铁氰化钾)检验
(铁氰化钾)检验 。一种制备铁氰化钾的流程如下:
。一种制备铁氰化钾的流程如下: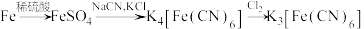
已知:

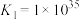
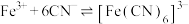
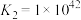
下列叙述错误的是
A.NaCN中 健和 健和 键数之比为1∶2 键数之比为1∶2 | B. 中 中 轨道和 轨道和 轨道以“头对头”重叠成键 轨道以“头对头”重叠成键 |
C. 中 中 的配位数为6 的配位数为6 | D.稳定性: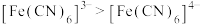 |
您最近一年使用:0次
7日内更新
|
190次组卷
|
2卷引用:湖北省T8联盟2024届高三下学期压轴考试(二模)化学试题
5 . 甲醇是重要的化工原料。CO2与H2反应可合成甲醇,反应如下: ,恒容密闭容器中,a mol CO2和3a mol H2,反应达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
,恒容密闭容器中,a mol CO2和3a mol H2,反应达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
 ,恒容密闭容器中,a mol CO2和3a mol H2,反应达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
,恒容密闭容器中,a mol CO2和3a mol H2,反应达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
| A.随温度升高该反应的平衡常数变大 |
| B.加入合适催化剂有利于提高CO2的平衡转化率 |
C. ℃时,恒容下充入Ar,压强增大,平衡正向移动,平衡时浓度变小 ℃时,恒容下充入Ar,压强增大,平衡正向移动,平衡时浓度变小 |
D.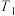 ℃时,恒压下2a mol ℃时,恒压下2a mol  与6a mol 与6a mol  反应达到平衡时 反应达到平衡时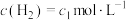 |
您最近一年使用:0次
名校
解题方法
6 . 湖北省十堰地区发现大量铌、钽等稀土矿产。萃取剂P204用于萃取稀土金属铌的反应为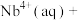
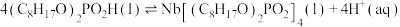 。某温度下,萃取铌离子的溶液中
。某温度下,萃取铌离子的溶液中 与时间变化关系如图所示。
与时间变化关系如图所示。
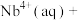
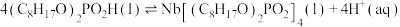 。某温度下,萃取铌离子的溶液中
。某温度下,萃取铌离子的溶液中 与时间变化关系如图所示。
与时间变化关系如图所示。
A.其他条件不变, 时萃取反应已停止 时萃取反应已停止 |
B. 增大,萃取平衡向左移动,平衡常数减小 增大,萃取平衡向左移动,平衡常数减小 |
C.萃取反应的正反应速率: |
D. 段 段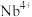 平均反应速率 平均反应速率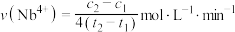 |
您最近一年使用:0次
7日内更新
|
155次组卷
|
3卷引用:湖北省T8联盟2024届高三下学期压轴考试(二模)化学试题
7 . 某小组模拟汽车尾气处理。某温度下,将一定量 和
和 投入体积为
投入体积为 、盛有催化剂的密闭容器中,发生反应:
、盛有催化剂的密闭容器中,发生反应: 。测得
。测得 的物质的量浓度随时间变化的关系如图所示。下列说法
的物质的量浓度随时间变化的关系如图所示。下列说法不正确 的是
 和
和 投入体积为
投入体积为 、盛有催化剂的密闭容器中,发生反应:
、盛有催化剂的密闭容器中,发生反应: 。测得
。测得 的物质的量浓度随时间变化的关系如图所示。下列说法
的物质的量浓度随时间变化的关系如图所示。下列说法
A. 段 段 的反应速率 的反应速率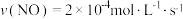 |
B.达平衡时,理论上该反应放出的热量约为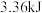 |
C.该温度下,反应的平衡常数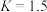 |
| D.升高温度,该反应的平衡常数减小 |
您最近一年使用:0次
8 . 某实验室测定并计算了在136~180℃范围内下列反应的平衡常数 :
:
①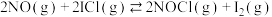

②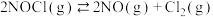
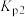
得到 和
和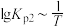 均为线性关系,如下图所示,有关下列说法错误的是
均为线性关系,如下图所示,有关下列说法错误的是
 :
:①
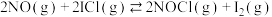

②
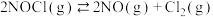
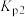
得到
 和
和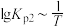 均为线性关系,如下图所示,有关下列说法错误的是
均为线性关系,如下图所示,有关下列说法错误的是
| A.反应②高温下可自发进行 |
B.反应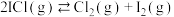 的 的 |
| C.升温,反应体系中分子总数会增大 |
| D.当混合气体颜色不变时,说明反应①和②已达平衡状态 |
您最近一年使用:0次
9 . 常温下,在含HgI2(s)的溶液中,一定c(I-)范围内,存在平衡关系:HgI2(s)  HgI2(aq);HgI2(aq)
HgI2(aq);HgI2(aq)  Hg2+(aq)+2I-(aq); HgI2(aq)
Hg2+(aq)+2I-(aq); HgI2(aq)  HgI+(aq)+I-(aq);HgI2(aq) +I-(aq)
HgI+(aq)+I-(aq);HgI2(aq) +I-(aq) 
 (aq);HgI2(aq) +2I-(aq)
(aq);HgI2(aq) +2I-(aq) 
 (aq),平衡常数依次为K0、K1、K2、K3、K4。已知
(aq),平衡常数依次为K0、K1、K2、K3、K4。已知 、
、 、
、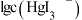 、
、 随
随 的变化关系如图所示,下列说法错误的是
的变化关系如图所示,下列说法错误的是
 HgI2(aq);HgI2(aq)
HgI2(aq);HgI2(aq)  Hg2+(aq)+2I-(aq); HgI2(aq)
Hg2+(aq)+2I-(aq); HgI2(aq)  HgI+(aq)+I-(aq);HgI2(aq) +I-(aq)
HgI+(aq)+I-(aq);HgI2(aq) +I-(aq) 
 (aq);HgI2(aq) +2I-(aq)
(aq);HgI2(aq) +2I-(aq) 
 (aq),平衡常数依次为K0、K1、K2、K3、K4。已知
(aq),平衡常数依次为K0、K1、K2、K3、K4。已知 、
、 、
、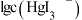 、
、 随
随 的变化关系如图所示,下列说法错误的是
的变化关系如图所示,下列说法错误的是
A. |
B.线 表示 表示 的变化情况 的变化情况 |
C.随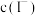 的增大, 的增大, 保持不变 保持不变 |
D.溶液中 元素和 元素和 元素的物质的量之比始终为 元素的物质的量之比始终为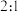 |
您最近一年使用:0次
10 . 高纯度 可用作玻璃擦光剂、搪瓷抛光剂、催化剂等。利用水解反应制备高纯度
可用作玻璃擦光剂、搪瓷抛光剂、催化剂等。利用水解反应制备高纯度 的原理为
的原理为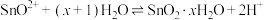 。某温度下,测得体系中
。某温度下,测得体系中 、
、 (
( 电离产生的
电离产生的 不考虑)与时间的关系如图所示。下列叙述正确的是
不考虑)与时间的关系如图所示。下列叙述正确的是
 可用作玻璃擦光剂、搪瓷抛光剂、催化剂等。利用水解反应制备高纯度
可用作玻璃擦光剂、搪瓷抛光剂、催化剂等。利用水解反应制备高纯度 的原理为
的原理为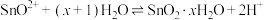 。某温度下,测得体系中
。某温度下,测得体系中 、
、 (
( 电离产生的
电离产生的 不考虑)与时间的关系如图所示。下列叙述正确的是
不考虑)与时间的关系如图所示。下列叙述正确的是
| A.正反应速率:a>c | B.平衡后增大 ,平衡常数K减小 ,平衡常数K减小 |
| C.b点时水解反应已停止 | D. |
您最近一年使用:0次