1 . 向体积均为 的甲、乙两个恒容密闭容器中分别充入
的甲、乙两个恒容密闭容器中分别充入 和
和 ,发生反应:
,发生反应: 。分别在绝热、恒温条件下进行,两反应体系的压强随时间的变化曲线如图所示。下列说法错误的是
。分别在绝热、恒温条件下进行,两反应体系的压强随时间的变化曲线如图所示。下列说法错误的是
 的甲、乙两个恒容密闭容器中分别充入
的甲、乙两个恒容密闭容器中分别充入 和
和 ,发生反应:
,发生反应: 。分别在绝热、恒温条件下进行,两反应体系的压强随时间的变化曲线如图所示。下列说法错误的是
。分别在绝热、恒温条件下进行,两反应体系的压强随时间的变化曲线如图所示。下列说法错误的是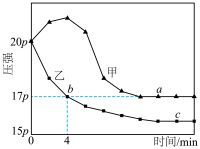
| A.正反应在较低温度下能自发进行 |
B.乙在恒温条件下进行, |
| C.a点的正反应速率大于c点的正反应速率 |
| D.甲条件下平衡常数K小于20.25 |
您最近一年使用:0次
解题方法
2 . 氯及其化合物在生产生活中有广泛应用。回答下列问题:
(1)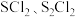 常用于硫化橡胶工业。
常用于硫化橡胶工业。
已知:① ;
;
② ;
;
③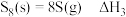 。
。
则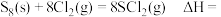
___________ (用含 的式子表示)。
的式子表示)。
(2)光气 在有机合成中常作氯化剂。工业上,可用
在有机合成中常作氯化剂。工业上,可用 和氯气混合合成光气。已知:合成
和氯气混合合成光气。已知:合成 时放出
时放出 热量,写出该反应的热化学方程式:
热量,写出该反应的热化学方程式:___________ 。
(3)在恒温恒容的密闭容器中充入 和
和 ,发生反应:
,发生反应: ,下列情况表明该反应已达到平衡状态的是___________(填字母)。
,下列情况表明该反应已达到平衡状态的是___________(填字母)。
(4)硫酰氯 常用于有机合成。制备原理:
常用于有机合成。制备原理: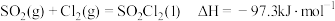 。实验测得速率方程为
。实验测得速率方程为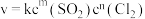 (k为速率常数,只与温度、催化剂有关,与浓度无关。m、n为反应级数,可以为整数、分数、正数、负数和0)。
(k为速率常数,只与温度、催化剂有关,与浓度无关。m、n为反应级数,可以为整数、分数、正数、负数和0)。
①为了测得反应级数,实验数据记录如下:
根据上述实验结果,计算
___________ ,
___________ 。
②已知: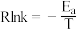 (R为常数,
(R为常数, 为活化能,T为温度)。测得
为活化能,T为温度)。测得 及在催化剂
及在催化剂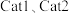 作用下随
作用下随 的变化如图所示。
的变化如图所示。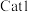 对应的活化能为
对应的活化能为___________  。催化效果:
。催化效果: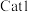
___________ (填“大于”“小于”或“等于”)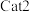 。
。
(5)我国古代采用“地康法”制备氯气: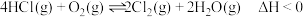 。为了探究制氯气的原理,总压强保持恒定为
。为了探究制氯气的原理,总压强保持恒定为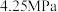 ,向密闭容器中充入
,向密闭容器中充入 和
和 ,发生上述反应,在温度
,发生上述反应,在温度 下,测得
下,测得 的平衡转化率与投料比
的平衡转化率与投料比 的关系如图所示。
的关系如图所示。
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。 时平衡常数
时平衡常数
___________  (
( 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数,结果保留两位小数)。从工业生产角度分析,投料比过大的缺点是
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数,结果保留两位小数)。从工业生产角度分析,投料比过大的缺点是___________ 。
(1)
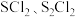 常用于硫化橡胶工业。
常用于硫化橡胶工业。已知:①
 ;
;②
 ;
;③
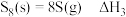 。
。则
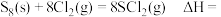
 的式子表示)。
的式子表示)。(2)光气
 在有机合成中常作氯化剂。工业上,可用
在有机合成中常作氯化剂。工业上,可用 和氯气混合合成光气。已知:合成
和氯气混合合成光气。已知:合成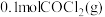 时放出
时放出 热量,写出该反应的热化学方程式:
热量,写出该反应的热化学方程式:(3)在恒温恒容的密闭容器中充入
 和
和 ,发生反应:
,发生反应: ,下列情况表明该反应已达到平衡状态的是___________(填字母)。
,下列情况表明该反应已达到平衡状态的是___________(填字母)。| A.混合气体密度不随时间变化 |
| B.气体总压强不随时间变化 |
C. 的消耗速率等于 的消耗速率等于 的生成速率 的生成速率 |
| D.Q(浓度商)不随时间变化 |
(4)硫酰氯
 常用于有机合成。制备原理:
常用于有机合成。制备原理: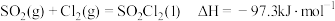 。实验测得速率方程为
。实验测得速率方程为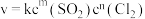 (k为速率常数,只与温度、催化剂有关,与浓度无关。m、n为反应级数,可以为整数、分数、正数、负数和0)。
(k为速率常数,只与温度、催化剂有关,与浓度无关。m、n为反应级数,可以为整数、分数、正数、负数和0)。①为了测得反应级数,实验数据记录如下:
| 序号 |  | 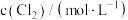 | 速率/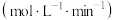 |
| a | 0.10 | 0.10 |  |
| b | 0.20 | 0.10 |  |
| c | 0.10 | 0.05 |  |


②已知:
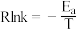 (R为常数,
(R为常数, 为活化能,T为温度)。测得
为活化能,T为温度)。测得 及在催化剂
及在催化剂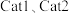 作用下随
作用下随 的变化如图所示。
的变化如图所示。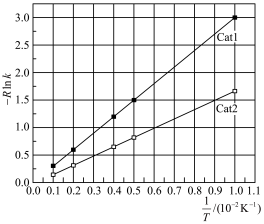
 对应的活化能为
对应的活化能为 。催化效果:
。催化效果:
 。
。(5)我国古代采用“地康法”制备氯气:
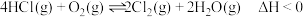 。为了探究制氯气的原理,总压强保持恒定为
。为了探究制氯气的原理,总压强保持恒定为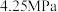 ,向密闭容器中充入
,向密闭容器中充入 和
和 ,发生上述反应,在温度
,发生上述反应,在温度 下,测得
下,测得 的平衡转化率与投料比
的平衡转化率与投料比 的关系如图所示。
的关系如图所示。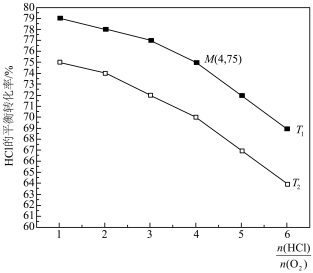

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。 时平衡常数
时平衡常数
 (
( 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数,结果保留两位小数)。从工业生产角度分析,投料比过大的缺点是
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数,结果保留两位小数)。从工业生产角度分析,投料比过大的缺点是
您最近一年使用:0次
名校
解题方法
3 . 利用下列反应可减少 排放,是实现“双碳”目标的途径之一。
排放,是实现“双碳”目标的途径之一。
I.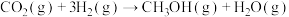

II.
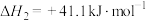
III.

请回答:
(1)反应I自发进行的条件是___________ 。(填“高温”、“低温”或“任何温度”)
(2)一定压强下,往某密闭容器中按投料比 充入
充入 和
和 反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。___________ 。
A.图中X、Y分别代表CO、
B.增大 的比值,
的比值, 的平衡转化率增大
的平衡转化率增大
C.若容器内混合气体的密度不再随时间改变时,说明反应已达到平衡状态
D.250℃时,反应II的平衡常数K<1
②体系中的 物质的量分数受温度的影响不大,试分析原因
物质的量分数受温度的影响不大,试分析原因___________ 。
(3)在一定温度下,在一容积固定的密闭容器中充入1mol (g)和3mol
(g)和3mol  (g),仅发生反应I。起始时容器内气体的总压强为16p kPa,平衡时
(g),仅发生反应I。起始时容器内气体的总压强为16p kPa,平衡时 (g)的体积分数为30%,则该温度下反应I的平衡常数
(g)的体积分数为30%,则该温度下反应I的平衡常数
___________ 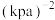 (用含p的表达式表示)。(已知:用气体分压计算的平衡常数为
(用含p的表达式表示)。(已知:用气体分压计算的平衡常数为 ,分压=总压×物质的量分数)。
,分压=总压×物质的量分数)。
(4)多相催化反应是在催化剂表面通过“扩散→吸附→反应→脱附”四个基本过程进行的。 的平衡转化率随着
的平衡转化率随着 浓度的增加先增大后减小,减小的原因是
浓度的增加先增大后减小,减小的原因是___________ 。如图,我国学者发现T℃时,在铜催化剂上二氧化碳加氢的反应机理如下,其中反应II为慢反应,请画出反应能量变化图像。___________
 排放,是实现“双碳”目标的途径之一。
排放,是实现“双碳”目标的途径之一。I.
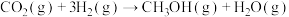

II.

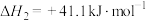
III.


请回答:
(1)反应I自发进行的条件是
(2)一定压强下,往某密闭容器中按投料比
 充入
充入 和
和 反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
A.图中X、Y分别代表CO、

B.增大
 的比值,
的比值, 的平衡转化率增大
的平衡转化率增大C.若容器内混合气体的密度不再随时间改变时,说明反应已达到平衡状态
D.250℃时,反应II的平衡常数K<1
②体系中的
 物质的量分数受温度的影响不大,试分析原因
物质的量分数受温度的影响不大,试分析原因(3)在一定温度下,在一容积固定的密闭容器中充入1mol
 (g)和3mol
(g)和3mol  (g),仅发生反应I。起始时容器内气体的总压强为16p kPa,平衡时
(g),仅发生反应I。起始时容器内气体的总压强为16p kPa,平衡时 (g)的体积分数为30%,则该温度下反应I的平衡常数
(g)的体积分数为30%,则该温度下反应I的平衡常数
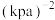 (用含p的表达式表示)。(已知:用气体分压计算的平衡常数为
(用含p的表达式表示)。(已知:用气体分压计算的平衡常数为 ,分压=总压×物质的量分数)。
,分压=总压×物质的量分数)。(4)多相催化反应是在催化剂表面通过“扩散→吸附→反应→脱附”四个基本过程进行的。
 的平衡转化率随着
的平衡转化率随着 浓度的增加先增大后减小,减小的原因是
浓度的增加先增大后减小,减小的原因是
您最近一年使用:0次
名校
4 . 常温下向 的混合液中滴加
的混合液中滴加 溶液,混合液中
溶液,混合液中 与
与 的关系如图所示,
的关系如图所示, 或
或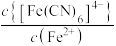 或
或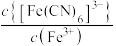 。下列叙述正确的是
。下列叙述正确的是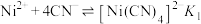 ;
;
② ;
;
③ ,且
,且 。
。
 的混合液中滴加
的混合液中滴加 溶液,混合液中
溶液,混合液中 与
与 的关系如图所示,
的关系如图所示, 或
或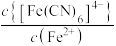 或
或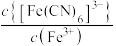 。下列叙述正确的是
。下列叙述正确的是
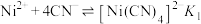 ;
;②
 ;
;③
 ,且
,且 。
。A.直线a代表 与 与 的关系 的关系 |
B.平衡常数 的数量级为 的数量级为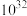 |
C.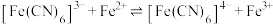 不易发生 不易发生 |
D.向含相同浓度的 和 和 的溶液中滴加 的溶液中滴加 溶液,先生成 溶液,先生成 |
您最近一年使用:0次
2024-06-04更新
|
172次组卷
|
3卷引用:辽宁省沈阳市第二中学2023-2024学年高三下学期第五次模拟考试化学试卷
解题方法
5 . 三元催化转换器可除去汽车尾气中90%以上的污染物.在一恒容密闭容器中加入 和一定量的NO,发生反应
和一定量的NO,发生反应 ,按不同投料比
,按不同投料比 时,CO的平衡转化率随温度的变化曲线如图所示。下列说法错误的是
时,CO的平衡转化率随温度的变化曲线如图所示。下列说法错误的是
 和一定量的NO,发生反应
和一定量的NO,发生反应 ,按不同投料比
,按不同投料比 时,CO的平衡转化率随温度的变化曲线如图所示。下列说法错误的是
时,CO的平衡转化率随温度的变化曲线如图所示。下列说法错误的是
A. |
B.a、b、c对应平衡常数 |
C.反应温度为 时,向平衡体系充入适量NO,可实现由c到b的转化 时,向平衡体系充入适量NO,可实现由c到b的转化 |
| D.使用三元催化转换器可提高该反应的平衡转化率 |
您最近一年使用:0次
名校
解题方法
6 . 一定压强下,向 密闭容器中充入
密闭容器中充入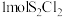 和
和 ,发生反应
,发生反应 。
。 与
与 的消耗速率
的消耗速率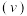 与温度
与温度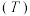 的关系如图,下列说法正确的是
的关系如图,下列说法正确的是
 密闭容器中充入
密闭容器中充入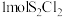 和
和 ,发生反应
,发生反应 。
。 与
与 的消耗速率
的消耗速率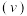 与温度
与温度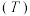 的关系如图,下列说法正确的是
的关系如图,下列说法正确的是
A. 四点中只有 四点中只有 点达到平衡状态 点达到平衡状态 |
| B.正反应的活化能小于逆反应的活化能 |
C.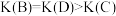 |
D. ,反应达平衡后缩小容器体积,各物质浓度不变 ,反应达平衡后缩小容器体积,各物质浓度不变 |
您最近一年使用:0次
2024-05-03更新
|
265次组卷
|
2卷引用:辽宁省重点高中协作校2024届高三下学期第二次模拟考试化学试题
7 . MTP是一类重要的药物中间体,可以由TOME经环化后合成。其反应式为: ,反应过程中液体体积变化忽略不计。下列说法错误的是
,反应过程中液体体积变化忽略不计。下列说法错误的是
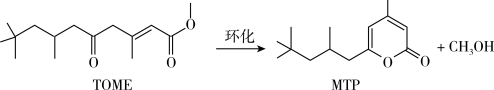
 ,反应过程中液体体积变化忽略不计。下列说法错误的是
,反应过程中液体体积变化忽略不计。下列说法错误的是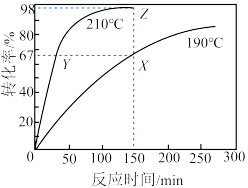
A.190℃时,0至150min之间MTP的平均反应速率为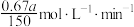 |
B.若Z点处于化学平衡状态,则210℃时反应平衡常数 |
| C.X、Y两点虽温度不同,但MTP的物质的量浓度相等 |
| D.从溶液体系中及时移出部分甲醇可提高TOME的转化率 |
您最近一年使用:0次
名校
8 . 工业上,常用离子交换法软化自来水,其原理是 ,
, 。常温下,向一定体积的自来水中加入离子交换树脂(NaR),测得自来水中
。常温下,向一定体积的自来水中加入离子交换树脂(NaR),测得自来水中 变化如图所示。下列叙述正确的是
变化如图所示。下列叙述正确的是
 ,
, 。常温下,向一定体积的自来水中加入离子交换树脂(NaR),测得自来水中
。常温下,向一定体积的自来水中加入离子交换树脂(NaR),测得自来水中 变化如图所示。下列叙述正确的是
变化如图所示。下列叙述正确的是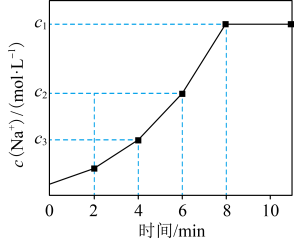
| A.反应达到平衡后,加入少量NaCl,离子交换反应的平衡常数减小 |
| B.6 min时的逆反应速率大于4 min时的逆反应速率 |
| C.其他条件不变时,10 min时离子交换反应已停止 |
D.4~8 min内平均反应速率: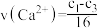 mol⋅L mol⋅L ⋅min ⋅min |
您最近一年使用:0次
2024-04-10更新
|
421次组卷
|
3卷引用:2024届辽宁省抚顺市六校协作体高三下学期第三次模拟化学试卷
名校
9 . 某小组利用不同膜反应器(可选择性地让某些气体通过而离开体系)研究 的分解率,工作原理如下图所示.图a、b和c反应区温度维持恒定且相等,仅发生
的分解率,工作原理如下图所示.图a、b和c反应区温度维持恒定且相等,仅发生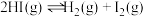 且在反应区内进行。投料均为
且在反应区内进行。投料均为 的
的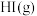 ,反应同时开始,
,反应同时开始, 时图b反应区处于瞬时平衡状态,其化学平衡常数
时图b反应区处于瞬时平衡状态,其化学平衡常数 。
。
下列说法正确的是
 的分解率,工作原理如下图所示.图a、b和c反应区温度维持恒定且相等,仅发生
的分解率,工作原理如下图所示.图a、b和c反应区温度维持恒定且相等,仅发生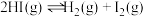 且在反应区内进行。投料均为
且在反应区内进行。投料均为 的
的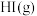 ,反应同时开始,
,反应同时开始, 时图b反应区处于瞬时平衡状态,其化学平衡常数
时图b反应区处于瞬时平衡状态,其化学平衡常数 。
。 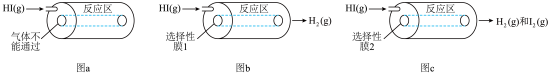
图a装置 | 图b装置 | 图c装置 | |
| 0.10 | 0.30 | x |
A.图a装置的化学平衡常数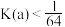 |
| B.图a装置中,HI(g)分解率为10% |
C.图b装置中,前 内 内 的平均渗透速率约为 的平均渗透速率约为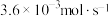 |
| D.图c装置中,x一定大于0.3 |
您最近一年使用:0次
2024-04-01更新
|
580次组卷
|
6卷引用:化学(辽宁卷01)-2024年高考押题预测卷
(已下线)化学(辽宁卷01)-2024年高考押题预测卷2024届浙江省温州市高三下学期第二次适应性考试(二模)化学试题浙江省温州市普通高中2024届高三下学期第二次适应性考试(二模)化学试题江西师大附中2024届高三下学期三模化学试卷2024届山东省泰安肥城市高考仿真模拟(一)化学试题(已下线)压轴题04 化学反应机理 历程 能垒图分析(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
10 . 双加压法工艺流程是世界上先进的制硝酸工艺。请回答相关问题:
(1)部分物质的∆fH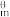 如下表所示(注:∆fH
如下表所示(注:∆fH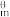 表示在25℃、标准压力下,由稳定的单质生成单位物质的量该物质的焓变)。
表示在25℃、标准压力下,由稳定的单质生成单位物质的量该物质的焓变)。
4NH₃(g)+5O₂(g)=4NO(g)+6H₂O(g) △H=_______ kJ/mol,该反应_______ (填“一定”、“一定不”或“不一定”)能自发进行。
(2)氨催化氧化后的取样气体中有2.8 mol NO、9.7 mol N2、1.45 mol O2,将该气体冷却到160℃,恒容条件下继续发生如下两个反应:
i.2NO+O2 2NO2 △H₁<0
2NO2 △H₁<0
ii.2NO2 N2O4
N2O4
①下列可以作为体系达到平衡状态的标志是_______ 。
A.容器内气体的密度不变 B.反应i 中v正(O2)=2v逆(NO2)
C.气体的压强不变 D.反应i 和ii的平衡常数均不变
E.容器内气体颜色不变
达到平衡时气体的总压强为0.8 MPa,体系中N2O4、O2均为0.1mol,则反应ii的平衡常数KP=____ MP-1。
②测得温度、压强对NO平衡转化率的影响如下图所示。
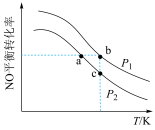
根据图像可知:P1____ P2(填“>”“<”或“=”);反应i 的平衡常数Ka、Kb、Kc的大小关系为____ 。
(3)从吸收塔出来的尾气中主要含有NO,NO与 NH3,在一定质量的催化剂( Mn-ZrOx)作用下,生成N2和H2O。发生的反应为:4NH3+4NO+O2=4N2+6H2O,v(NO)表示NO的转化速率,转化速率方程为v(NO)=k·cx(NO)cy(NH3)cz(O2)[k表示NO 的转化速率常数]。
①根据表中数据可知y=_______ ,Z =_______ 。
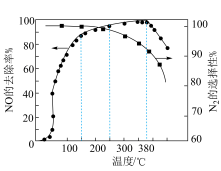
②NO 的去除率与N2的选择率如下图所示,当反应温度高于380 ℃时,NO 的去除率明显下降的原因可能有:a.平衡逆向移动;b._____ ;c._____ 。
(1)部分物质的∆fH
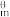 如下表所示(注:∆fH
如下表所示(注:∆fH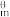 表示在25℃、标准压力下,由稳定的单质生成单位物质的量该物质的焓变)。
表示在25℃、标准压力下,由稳定的单质生成单位物质的量该物质的焓变)。| 物质 | NH3 | O2 | NO | H2O |
∆fH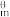 (kJ/mol) (kJ/mol) | —45.8 | 0 | +90.3 | —241.9 |
(2)氨催化氧化后的取样气体中有2.8 mol NO、9.7 mol N2、1.45 mol O2,将该气体冷却到160℃,恒容条件下继续发生如下两个反应:
i.2NO+O2
 2NO2 △H₁<0
2NO2 △H₁<0ii.2NO2
 N2O4
N2O4①下列可以作为体系达到平衡状态的标志是
A.容器内气体的密度不变 B.反应i 中v正(O2)=2v逆(NO2)
C.气体的压强不变 D.反应i 和ii的平衡常数均不变
E.容器内气体颜色不变
达到平衡时气体的总压强为0.8 MPa,体系中N2O4、O2均为0.1mol,则反应ii的平衡常数KP=
②测得温度、压强对NO平衡转化率的影响如下图所示。

根据图像可知:P1
(3)从吸收塔出来的尾气中主要含有NO,NO与 NH3,在一定质量的催化剂( Mn-ZrOx)作用下,生成N2和H2O。发生的反应为:4NH3+4NO+O2=4N2+6H2O,v(NO)表示NO的转化速率,转化速率方程为v(NO)=k·cx(NO)cy(NH3)cz(O2)[k表示NO 的转化速率常数]。
| c(NH3)(mmol/L) | c(NO)(mmol/L) | c(O2)(mmol/L) | v(NO)[mmol/(g·min)] |
| 0.1 | 1.0 | 1.0 | 1.0 k |
| 0.1 | 1.0 | 4.0 | 2.0 k |
| 0.2 | 1.0 | 4.0 | 2.0 k |
②NO 的去除率与N2的选择率如下图所示,当反应温度高于380 ℃时,NO 的去除率明显下降的原因可能有:a.平衡逆向移动;b.

您最近一年使用:0次

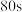 时反应区
时反应区 的物质的量/
的物质的量/


