1 . 羰基硫(COS)是一种粮食熏蒸剂,其合成原理为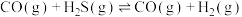
 ,在恒容密闭容器中发生该反应并达到平衡状态。下列说法正确的是
,在恒容密闭容器中发生该反应并达到平衡状态。下列说法正确的是
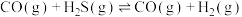
 ,在恒容密闭容器中发生该反应并达到平衡状态。下列说法正确的是
,在恒容密闭容器中发生该反应并达到平衡状态。下列说法正确的是A.催化剂能改变 |
| B.升温,平衡常数增大 |
| C.通入He(g),压强增大,H2S的转化率增大 |
| D.该反应正反应的活化能小于逆反应的活化能 |
您最近一年使用:0次
2 . 已知: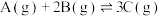
 ,向一恒温恒容的密闭容器中充入
,向一恒温恒容的密闭容器中充入 和
和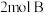 发生反应,
发生反应, 时达到平衡状态Ⅰ,在
时达到平衡状态Ⅰ,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如下图所示。下列说法正确的是
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如下图所示。下列说法正确的是
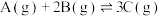
 ,向一恒温恒容的密闭容器中充入
,向一恒温恒容的密闭容器中充入 和
和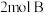 发生反应,
发生反应, 时达到平衡状态Ⅰ,在
时达到平衡状态Ⅰ,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如下图所示。下列说法正确的是
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如下图所示。下列说法正确的是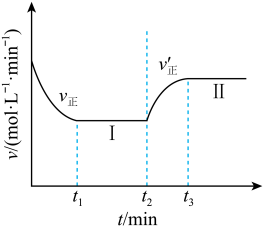
| A.容器内压强不变,表明反应达到平衡 | B.平衡时A的体积分数 : : (Ⅰ)> (Ⅰ)> (Ⅱ) (Ⅱ) |
C. 时改变的条件:向容器中加入C 时改变的条件:向容器中加入C | D.平衡常数K:K(Ⅱ)<K(Ⅰ) |
您最近一年使用:0次
3 . 镀锌钢板广泛运用于汽车行业。当镀层质量不合格时,先利用强酸将镀件表面的镀锌层清洗,再检测其中含有的 、
、 、
、 等离子的浓度。
等离子的浓度。
(1)测定原理:EDTA(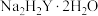 )可与
)可与 、
、 、
、 等多种金属离子形成络合物,如下表。其中
等多种金属离子形成络合物,如下表。其中 是乙二胺四乙酸根(
是乙二胺四乙酸根( )的简写。
)的简写。
①EDTA在水溶液中可看作“六元酸”的一种微粒可表示为___________ (用H、Y表示)。
②表中最稳定的金属络合物是___________ (填化学式)。
(2)测定过程:已知EDTA标准溶液滴定 的相关信息如下表:
的相关信息如下表:
可采用连续滴定法测定 、
、 、
、 的浓度,具体步骤如下:
的浓度,具体步骤如下:
I.先测定 (
( 、
、 不影响Fe3+的滴定):
不影响Fe3+的滴定):
请补充完整实验方案:
①按规定操作分别将0.01000 EDTA标准溶液和待测溶液[其中
EDTA标准溶液和待测溶液[其中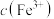 约为0.01
约为0.01 ]装入如图所示的滴定管中;
]装入如图所示的滴定管中;___________ 。(可选用的实验试剂有:磺基水杨酸、氨水溶液、盐酸溶液)
③实验测得 的浓度偏大,其原因可能是
的浓度偏大,其原因可能是___________ 。
II.再测定 :在
:在 的锥形瓶中继续加入适量过硫酸铵
的锥形瓶中继续加入适量过硫酸铵 ,轻微摇晃使
,轻微摇晃使 转化为
转化为 ,继续用EDTA标准溶液滴定到终点。写出
,继续用EDTA标准溶液滴定到终点。写出 转化为
转化为 的离子方程式:
的离子方程式:___________ 。
III.最后测定 :在
:在 的锥形瓶中继续加入一定量过量的EDTA标准溶液,调节溶液pH至5.0~6.0,再用
的锥形瓶中继续加入一定量过量的EDTA标准溶液,调节溶液pH至5.0~6.0,再用 标准溶液滴定到终点。
标准溶液滴定到终点。 不影响
不影响 滴定的原因是
滴定的原因是___________ 。
 、
、 、
、 等离子的浓度。
等离子的浓度。(1)测定原理:EDTA(
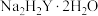 )可与
)可与 、
、 、
、 等多种金属离子形成络合物,如下表。其中
等多种金属离子形成络合物,如下表。其中 是乙二胺四乙酸根(
是乙二胺四乙酸根( )的简写。
)的简写。| 络合反应 | 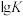 (K为平衡常数) |
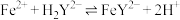 | 14.3 |
 | 16.5 |
 | 25.1 |
②表中最稳定的金属络合物是
(2)测定过程:已知EDTA标准溶液滴定
 的相关信息如下表:
的相关信息如下表:| 滴定对象 |  |
| 滴定时溶液pH范围 | 1.5~2.0 |
| 指示剂 | 磺基水杨酸 |
| 滴定终点现象 | 紫红色→亮黄色 |
 、
、 、
、 的浓度,具体步骤如下:
的浓度,具体步骤如下:I.先测定
 (
( 、
、 不影响Fe3+的滴定):
不影响Fe3+的滴定):请补充完整实验方案:
①按规定操作分别将0.01000
 EDTA标准溶液和待测溶液[其中
EDTA标准溶液和待测溶液[其中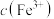 约为0.01
约为0.01 ]装入如图所示的滴定管中;
]装入如图所示的滴定管中;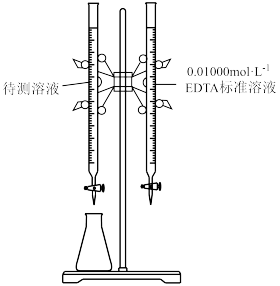
③实验测得
 的浓度偏大,其原因可能是
的浓度偏大,其原因可能是II.再测定
 :在
:在 的锥形瓶中继续加入适量过硫酸铵
的锥形瓶中继续加入适量过硫酸铵 ,轻微摇晃使
,轻微摇晃使 转化为
转化为 ,继续用EDTA标准溶液滴定到终点。写出
,继续用EDTA标准溶液滴定到终点。写出 转化为
转化为 的离子方程式:
的离子方程式:III.最后测定
 :在
:在 的锥形瓶中继续加入一定量过量的EDTA标准溶液,调节溶液pH至5.0~6.0,再用
的锥形瓶中继续加入一定量过量的EDTA标准溶液,调节溶液pH至5.0~6.0,再用 标准溶液滴定到终点。
标准溶液滴定到终点。 不影响
不影响 滴定的原因是
滴定的原因是
您最近一年使用:0次
4 . 反应 是汽车尾气无害化处理中的反应之一、下列说法正确的是
是汽车尾气无害化处理中的反应之一、下列说法正确的是
 是汽车尾气无害化处理中的反应之一、下列说法正确的是
是汽车尾气无害化处理中的反应之一、下列说法正确的是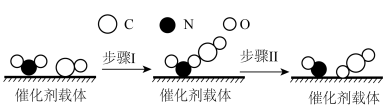
A.该反应的 , , |
B.该反应的平衡常数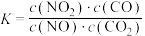 |
C.如图所示的反应机理中,步骤I可理解为 和CO仅在一定方向上才发生有效碰撞 和CO仅在一定方向上才发生有效碰撞 |
D.反应中每消耗22.24L  ,转移电子的数目为 ,转移电子的数目为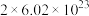 |
您最近一年使用:0次
名校
解题方法
5 . 甲烷在地壳中储量丰富,该物质是一种重要的燃料和工业原料。请回答下列问题:
(1)甲烷的燃烧热 kJ⋅mol
kJ⋅mol ,则一定量
,则一定量 完全燃烧生成1 mol
完全燃烧生成1 mol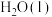 时放出的热量为
时放出的热量为_______ kJ。
(2)甲烷、水蒸气重整可获取合成气(CO、 ),涉及的主反应和副反应如下:
),涉及的主反应和副反应如下:
主反应:


副反应:
 kJ⋅mol
kJ⋅mol

两个反应的平衡常数随温度的变化曲线如图所示,则表示主反应的曲线是_______ (填“甲”或“乙”);温度为 K时,反应
K时,反应 的平衡常数
的平衡常数
_______ (用含a的代数式表示)。 )有利于实现“碳中和”,该甲烷重整的反应为
)有利于实现“碳中和”,该甲烷重整的反应为

①下列措施能使甲烷平衡转化率提高的是_______ (填字母,下同),能使平衡常数增大的是_______ 。
A增大 的浓度 B.升高温度 C.增大压强 D.减小
的浓度 B.升高温度 C.增大压强 D.减小 的浓度
的浓度
②一定条件下,在2 L恒容密闭容器中充入2 mol 和一定量的
和一定量的 发生上述反应,测得初始压强为
发生上述反应,测得初始压强为 ,10 min时容器内压强不再变化,且压强为
,10 min时容器内压强不再变化,且压强为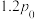 ,0~10min内平均反应速率
,0~10min内平均反应速率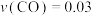 mol⋅L
mol⋅L ⋅min
⋅min ,达到平衡时
,达到平衡时 的转化率为
的转化率为_______ %,初始时加入的 为
为_______ mol。
(1)甲烷的燃烧热
 kJ⋅mol
kJ⋅mol ,则一定量
,则一定量 完全燃烧生成1 mol
完全燃烧生成1 mol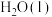 时放出的热量为
时放出的热量为(2)甲烷、水蒸气重整可获取合成气(CO、
 ),涉及的主反应和副反应如下:
),涉及的主反应和副反应如下:主反应:



副反应:

 kJ⋅mol
kJ⋅mol

两个反应的平衡常数随温度的变化曲线如图所示,则表示主反应的曲线是
 K时,反应
K时,反应 的平衡常数
的平衡常数
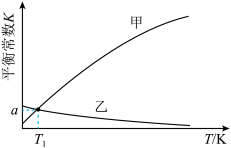
 )有利于实现“碳中和”,该甲烷重整的反应为
)有利于实现“碳中和”,该甲烷重整的反应为

①下列措施能使甲烷平衡转化率提高的是
A增大
 的浓度 B.升高温度 C.增大压强 D.减小
的浓度 B.升高温度 C.增大压强 D.减小 的浓度
的浓度②一定条件下,在2 L恒容密闭容器中充入2 mol
 和一定量的
和一定量的 发生上述反应,测得初始压强为
发生上述反应,测得初始压强为 ,10 min时容器内压强不再变化,且压强为
,10 min时容器内压强不再变化,且压强为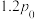 ,0~10min内平均反应速率
,0~10min内平均反应速率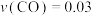 mol⋅L
mol⋅L ⋅min
⋅min ,达到平衡时
,达到平衡时 的转化率为
的转化率为 为
为
您最近一年使用:0次
2024-05-07更新
|
110次组卷
|
2卷引用:2024届海南省琼海市嘉积中学高三下学期模拟预测化学试题
2024·江苏·模拟预测
6 . 对于二氧化硫的催化氧化反应:2SO2(g)+O2(g) 2SO3(g),下列有关说法正确的是
2SO3(g),下列有关说法正确的是
 2SO3(g),下列有关说法正确的是
2SO3(g),下列有关说法正确的是| A.该反应的ΔS>0 |
B.该反应平衡常数的表达式为K=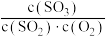 |
| C.反应中每消耗22.4LO2(标准状况),转移电子数约为2×6.02×1023 |
| D.温度不变,提高O2的起始浓度或增大反应压强,均能提高反应速率和SO2的转化率 |
您最近一年使用:0次
7 . 常温下,在含有 (s)的溶液中,一定pH范围内,存在平衡:
(s)的溶液中,一定pH范围内,存在平衡: ;
;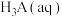
 ;
;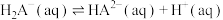 ;
;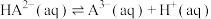 。平衡常数依次为
。平衡常数依次为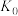 、
、 、
、 、
、 。已知
。已知 、
、 、
、 、
、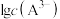 随pH变化关系如图所示。其中,
随pH变化关系如图所示。其中, 和
和 交点
交点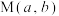 ,
, 和
和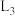 交点为
交点为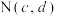 ,
, 和
和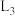 交点为
交点为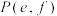 。下列说法错误的是
。下列说法错误的是
 (s)的溶液中,一定pH范围内,存在平衡:
(s)的溶液中,一定pH范围内,存在平衡: ;
;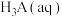
 ;
;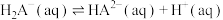 ;
;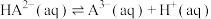 。平衡常数依次为
。平衡常数依次为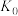 、
、 、
、 、
、 。已知
。已知 、
、 、
、 、
、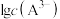 随pH变化关系如图所示。其中,
随pH变化关系如图所示。其中, 和
和 交点
交点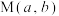 ,
, 和
和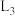 交点为
交点为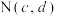 ,
, 和
和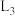 交点为
交点为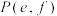 。下列说法错误的是
。下列说法错误的是
A.直线 表示 表示 的变化情况 的变化情况 |
B.N点时,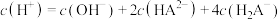 |
| C.随pH增大,溶液中含A微粒的总浓度一直增大 |
D. |
您最近一年使用:0次
名校
解题方法
8 . 一定压强下,向 密闭容器中充入
密闭容器中充入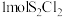 和
和 ,发生反应
,发生反应 。
。 与
与 的消耗速率
的消耗速率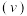 与温度
与温度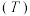 的关系如图,下列说法正确的是
的关系如图,下列说法正确的是
 密闭容器中充入
密闭容器中充入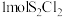 和
和 ,发生反应
,发生反应 。
。 与
与 的消耗速率
的消耗速率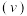 与温度
与温度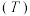 的关系如图,下列说法正确的是
的关系如图,下列说法正确的是
A. 四点中只有 四点中只有 点达到平衡状态 点达到平衡状态 |
| B.正反应的活化能小于逆反应的活化能 |
C.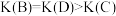 |
D. ,反应达平衡后缩小容器体积,各物质浓度不变 ,反应达平衡后缩小容器体积,各物质浓度不变 |
您最近一年使用:0次
2024-05-03更新
|
265次组卷
|
2卷引用:辽宁省重点高中协作校2024届高三下学期第二次模拟考试化学试题
解题方法
9 . 化石燃料燃烧、硫酸工业等都会释放出大量的二氧化硫,针对二氧化硫排放量大的问题,我国已经采取了一系列的治理措施,减少二氧化硫排放,保障环境的稳定和持续发展。
回答下列问题:
(1)“钙基固硫”是燃煤时加入 或CaO可减少二氧化硫的排放,涉及的反应有:
或CaO可减少二氧化硫的排放,涉及的反应有:
①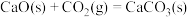

②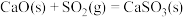
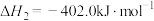
③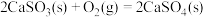

则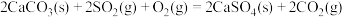

________ 。
(2)硝化法是一种古老的生产硫酸的方法,同时实现了二氧化硫的处理,主要反应: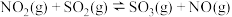
 。
。 ℃时,向1L密闭容器中加入等物质的量的
℃时,向1L密闭容器中加入等物质的量的 和
和 ,达到平衡时NO和
,达到平衡时NO和 的浓度之比为
的浓度之比为 :
: ,该温度下该反应的化学平衡常数为
,该温度下该反应的化学平衡常数为________ ,温度升高,平衡常数________ (填“增大”“减小”或“不变”)。保持温度不变,向1L密闭容器中同时充入 、
、 、
、 、NO各1mol
、NO各1mol
________  (填“>”“<”或“=”),达到平衡时二氧化硫的转化率为
(填“>”“<”或“=”),达到平衡时二氧化硫的转化率为________ 。
(3)模仿工业上用反应: 以得到硫酸,除去工业废气中的
以得到硫酸,除去工业废气中的 。现在一容积固定为1L的密闭容器中进行该反应,测得如下数据:
。现在一容积固定为1L的密闭容器中进行该反应,测得如下数据:
①分析第1组和第2组实验数据,可以得出有关反应速率的结论是________ 。
②已知,反应中,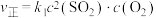 ,
, ,
, 、
、 为速率常数,只与温度有关。若实验组2,1min时,
为速率常数,只与温度有关。若实验组2,1min时, ,则
,则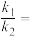
________ ,
________ 。
回答下列问题:
(1)“钙基固硫”是燃煤时加入
 或CaO可减少二氧化硫的排放,涉及的反应有:
或CaO可减少二氧化硫的排放,涉及的反应有:①
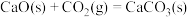

②
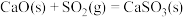
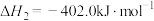
③
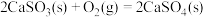

则
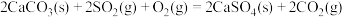

(2)硝化法是一种古老的生产硫酸的方法,同时实现了二氧化硫的处理,主要反应:
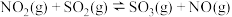
 。
。 ℃时,向1L密闭容器中加入等物质的量的
℃时,向1L密闭容器中加入等物质的量的 和
和 ,达到平衡时NO和
,达到平衡时NO和 的浓度之比为
的浓度之比为 :
: ,该温度下该反应的化学平衡常数为
,该温度下该反应的化学平衡常数为 、
、 、
、 、NO各1mol
、NO各1mol
 (填“>”“<”或“=”),达到平衡时二氧化硫的转化率为
(填“>”“<”或“=”),达到平衡时二氧化硫的转化率为(3)模仿工业上用反应:
 以得到硫酸,除去工业废气中的
以得到硫酸,除去工业废气中的 。现在一容积固定为1L的密闭容器中进行该反应,测得如下数据:
。现在一容积固定为1L的密闭容器中进行该反应,测得如下数据:| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | |
 |  |  | |||
| 1 | 550 | 2 | 1 |  | 10 |
| 2 | 650 | 1 |  | 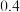 | 4 |
②已知,反应中,
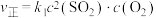 ,
, ,
, 、
、 为速率常数,只与温度有关。若实验组2,1min时,
为速率常数,只与温度有关。若实验组2,1min时, ,则
,则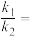

您最近一年使用:0次
10 .  催化氧化法将
催化氧化法将 转化为
转化为 的反应为
的反应为 。下列关于
。下列关于 催化氧化法制
催化氧化法制 的说法中错误的是
的说法中错误的是
 催化氧化法将
催化氧化法将 转化为
转化为 的反应为
的反应为 。下列关于
。下列关于 催化氧化法制
催化氧化法制 的说法中错误的是
的说法中错误的是A.该反应的 |
B.该反应的平衡常数 |
C.使用合适的催化剂可提高化学反应速率,但不影响 的平衡转化率 的平衡转化率 |
| D.该反应在高温下可自发进行 |
您最近一年使用:0次



