1 . 甲醇是重要的化工原料。CO2与H2反应可合成甲醇,反应如下: ,恒容密闭容器中,a mol CO2和3a mol H2,反应达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
,恒容密闭容器中,a mol CO2和3a mol H2,反应达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
 ,恒容密闭容器中,a mol CO2和3a mol H2,反应达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
,恒容密闭容器中,a mol CO2和3a mol H2,反应达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
| A.随温度升高该反应的平衡常数变大 |
| B.加入合适催化剂有利于提高CO2的平衡转化率 |
C. ℃时,恒容下充入Ar,压强增大,平衡正向移动,平衡时浓度变小 ℃时,恒容下充入Ar,压强增大,平衡正向移动,平衡时浓度变小 |
D.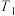 ℃时,恒压下2a mol ℃时,恒压下2a mol  与6a mol 与6a mol  反应达到平衡时 反应达到平衡时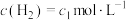 |
您最近一年使用:0次
解题方法
2 . 在恒容密闭容器中发生反应: ,Y的平衡转化率按不同投料比
,Y的平衡转化率按不同投料比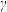 (
(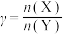 )随温度变化的曲线如图所示。下列说法正确的是
)随温度变化的曲线如图所示。下列说法正确的是
 ,Y的平衡转化率按不同投料比
,Y的平衡转化率按不同投料比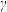 (
(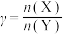 )随温度变化的曲线如图所示。下列说法正确的是
)随温度变化的曲线如图所示。下列说法正确的是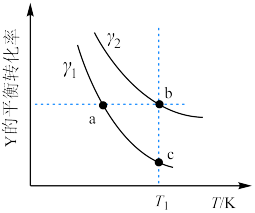
A.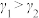 |
B.平衡常数: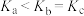 |
| C.当容器内气体密度不变时,反应达到平衡 |
D. 温度下增大压强,c点向a点方向移动 温度下增大压强,c点向a点方向移动 |
您最近一年使用:0次
3 . 一定条件下, 在恒容密闭容器中发生分解反应:
在恒容密闭容器中发生分解反应: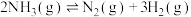
 ,
, 随时间的变化如图所示。已知
随时间的变化如图所示。已知 时反应达到平衡,
时反应达到平衡, 时改变某单一条件(浓度、温度或催化剂等),下列说法不正确的是
时改变某单一条件(浓度、温度或催化剂等),下列说法不正确的是
 在恒容密闭容器中发生分解反应:
在恒容密闭容器中发生分解反应: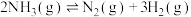
 ,
, 随时间的变化如图所示。已知
随时间的变化如图所示。已知 时反应达到平衡,
时反应达到平衡, 时改变某单一条件(浓度、温度或催化剂等),下列说法不正确的是
时改变某单一条件(浓度、温度或催化剂等),下列说法不正确的是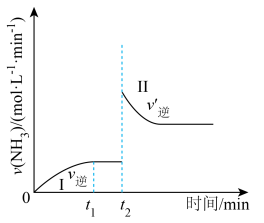
A.由0到 , , 的浓度不断增大 的浓度不断增大 |
B.由 到 到 , ,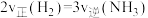 |
C. 时,可能向容器中通入了 时,可能向容器中通入了 |
D.平衡常数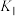 可能小于 可能小于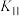 |
您最近一年使用:0次
解题方法
4 . I已知:①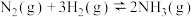
 ;
;
②
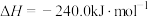 ;
;
③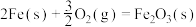
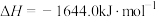 。
。
(1)则反应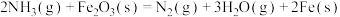

_____  。
。
Ⅱ化学反应的速率和限度对人类生产生活有重要的意义。
(2)已知 。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响,设计实验如表(所取溶液体积均为2mL):
。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响,设计实验如表(所取溶液体积均为2mL):
①上述实验中溶液最先变浑浊的是_________ (填实验编号,下同)。
②控制变量是科学研究的重要方法,为探究浓度对化学反应速率的影响,应选择__________ 。
(3)在10L的密闭容器中,进行如下化学反应: ,其化学平衡常数K和温度t的关系如下表:
,其化学平衡常数K和温度t的关系如下表:
请回答:
①该反应的化学平衡常数表达式为K=________ 。
②该反应为________ (填“吸热”或“放热”)反应。
③能说明该反应达到化学平衡状态的是_________ (填字母)。
a.容器中压强不变 b.混合气体中 不变
不变
c. d.
d.
④某温度下,平衡浓度符合下式: ,试判断此时的温度为
,试判断此时的温度为_______ ℃。
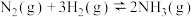
 ;
;②

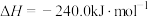 ;
;③
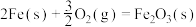
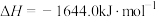 。
。(1)则反应
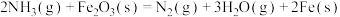

 。
。Ⅱ化学反应的速率和限度对人类生产生活有重要的意义。
(2)已知
 。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响,设计实验如表(所取溶液体积均为2mL):
。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响,设计实验如表(所取溶液体积均为2mL):| 实验编号 | 温度/℃ | 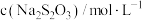 | 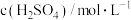 |
| I | 25 | 0.1 | 0.1 |
| Ⅱ | 25 | 0.2 | 0.1 |
| Ⅲ | 50 | 0.2 | 0.1 |
②控制变量是科学研究的重要方法,为探究浓度对化学反应速率的影响,应选择
(3)在10L的密闭容器中,进行如下化学反应:
 ,其化学平衡常数K和温度t的关系如下表:
,其化学平衡常数K和温度t的关系如下表:| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
①该反应的化学平衡常数表达式为K=
②该反应为
③能说明该反应达到化学平衡状态的是
a.容器中压强不变 b.混合气体中
 不变
不变c.
 d.
d.
④某温度下,平衡浓度符合下式:
 ,试判断此时的温度为
,试判断此时的温度为
您最近一年使用:0次
5 . I. 300℃时将2molA和2molB两种气体混合于2L密闭容器中,发生反应:3A(g)+B(g) 2C(g)+2D(g)
2C(g)+2D(g)  ,2min末达到平衡,生成0.8molD。
,2min末达到平衡,生成0.8molD。
(1)300℃时,该反应的平衡常数表达式为K=___________ ,已知K300℃<K350℃,则
___________ (填“>”或“<”0)。
(2)在2min末时,B的平衡浓度为___________ 。
(3)若温度不变,缩小容器容积,则A的转化率___________  填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。
Ⅱ.在一定条件下,可逆反应:mA+nB pC达到平衡,若:
pC达到平衡,若:
(4)A、B、C都是气体,减小压强,平衡向正反应方向移动,则,m+n___________ (填“>”“<”或“ ”p)。
”p)。
(5)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是___________ 。(填“逆向移动”、“正向移动”或“不移动”)
(6)加热后,可使C的质量增加,则正反应是___________ (填“放热”或“吸热”)反应。
 2C(g)+2D(g)
2C(g)+2D(g)  ,2min末达到平衡,生成0.8molD。
,2min末达到平衡,生成0.8molD。(1)300℃时,该反应的平衡常数表达式为K=

(2)在2min末时,B的平衡浓度为
(3)若温度不变,缩小容器容积,则A的转化率
 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。Ⅱ.在一定条件下,可逆反应:mA+nB
 pC达到平衡,若:
pC达到平衡,若:(4)A、B、C都是气体,减小压强,平衡向正反应方向移动,则,m+n
 ”p)。
”p)。(5)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是
(6)加热后,可使C的质量增加,则正反应是
您最近一年使用:0次
解题方法
6 . 在密闭窗口中进行反应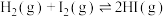
 ,该反应的反应速率(v)随时间(t)变化的关系如图所示,若
,该反应的反应速率(v)随时间(t)变化的关系如图所示,若 、
、 时刻只改变一个条件,下列说法中不正确的
时刻只改变一个条件,下列说法中不正确的

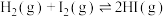
 ,该反应的反应速率(v)随时间(t)变化的关系如图所示,若
,该反应的反应速率(v)随时间(t)变化的关系如图所示,若 、
、 时刻只改变一个条件,下列说法中不正确的
时刻只改变一个条件,下列说法中不正确的
A.该反应的平衡常数: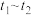 的 的 与 与 的 的 相等 相等 |
B. 时刻,采取的措施一定是增大压强 时刻,采取的措施一定是增大压强 |
C. 的转化率: 的转化率: 的转化率可能小于 的转化率可能小于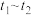 的转化率 的转化率 |
D.若将 改为 改为 ,在其他条件都相同时, ,在其他条件都相同时, 要缩短 要缩短 |
您最近一年使用:0次
7 . 对于可逆反应: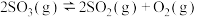
 ,下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都增大的是
,下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都增大的是
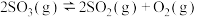
 ,下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都增大的是
,下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都增大的是| A.増大压强 | B.升高温度 | C.使用催化剂 | D.增大 浓度 浓度 |
您最近一年使用:0次
解题方法
8 . 氨基甲酸铵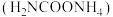 是一种重要的化工原料,可用于药物合成、制备化学肥料、灭火剂或洗涤剂等。某化学兴趣小组用如图所示装置制取氨基甲酸铵:
是一种重要的化工原料,可用于药物合成、制备化学肥料、灭火剂或洗涤剂等。某化学兴趣小组用如图所示装置制取氨基甲酸铵:
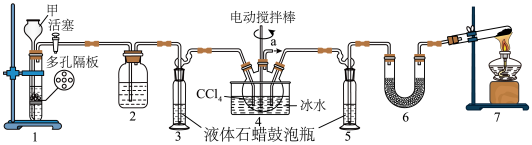
已知:①制取氨基甲酸铵反应为: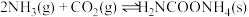
 。
。
②氨基甲酸铵溶于水后生成 和
和 。
。
回答下列问题:
(1)仪器甲的名称是___________ ,装置2的作用是除去 中的水蒸气,其盛装的试剂是
中的水蒸气,其盛装的试剂是___________ 。
(2)装置7是实验室制备氨气,其化学方程式为___________ 。
(3)液体石蜡鼓泡瓶的作用是___________ 。
(4)实验制得产品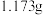 ,其中可能含有碳酸氢铵杂质(不考虑碳酸氢铵与一水合氨的之间的反应)。设计方案进行成分探究,请填写表中空格。
,其中可能含有碳酸氢铵杂质(不考虑碳酸氢铵与一水合氨的之间的反应)。设计方案进行成分探究,请填写表中空格。
限选试剂:蒸馏水、稀硝酸、 溶液、澄清石灰水、
溶液、澄清石灰水、 溶液、稀盐酸。
溶液、稀盐酸。
通过计算氨基甲酸铵的质量分数是___________ 。(保留小数点后两位)[ 、
、 ]
]
(5)氨基甲酸铵易分解,用如图所示装置测定 时该分解反应的化学平衡常数
时该分解反应的化学平衡常数 ,实验步骤如下:
,实验步骤如下:

(Ⅰ)关闭 ,打开
,打开 和
和 ,开启真空泵抽气至测压仪数值稳定后关闭
,开启真空泵抽气至测压仪数值稳定后关闭 。
。
(Ⅱ)关闭 ,
,___________ ,读取压强数值。
测得 时压强为
时压强为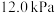 。
。
①请在空白处完善步骤Ⅱ的实验操作。
②若步骤I中测压仪数值未稳定即关闭 ,
, 测量值
测量值___________ (选填“偏大”、“偏小”或“无影响”)。
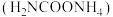 是一种重要的化工原料,可用于药物合成、制备化学肥料、灭火剂或洗涤剂等。某化学兴趣小组用如图所示装置制取氨基甲酸铵:
是一种重要的化工原料,可用于药物合成、制备化学肥料、灭火剂或洗涤剂等。某化学兴趣小组用如图所示装置制取氨基甲酸铵:
已知:①制取氨基甲酸铵反应为:
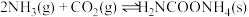
 。
。②氨基甲酸铵溶于水后生成
 和
和 。
。回答下列问题:
(1)仪器甲的名称是
 中的水蒸气,其盛装的试剂是
中的水蒸气,其盛装的试剂是(2)装置7是实验室制备氨气,其化学方程式为
(3)液体石蜡鼓泡瓶的作用是
(4)实验制得产品
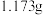 ,其中可能含有碳酸氢铵杂质(不考虑碳酸氢铵与一水合氨的之间的反应)。设计方案进行成分探究,请填写表中空格。
,其中可能含有碳酸氢铵杂质(不考虑碳酸氢铵与一水合氨的之间的反应)。设计方案进行成分探究,请填写表中空格。限选试剂:蒸馏水、稀硝酸、
 溶液、澄清石灰水、
溶液、澄清石灰水、 溶液、稀盐酸。
溶液、稀盐酸。| 实验步骤 | 预期现象和结论 |
| 步骤1:取固体样品于试管中,加入蒸馏水至固体溶解 | 得到无色溶液 |
| 步骤2:向试管中继续加入足量澄清石灰水 | |
步骤3:过滤、洗涤、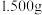 | 证明样品中有碳酸氢铵 |
 、
、 ]
](5)氨基甲酸铵易分解,用如图所示装置测定
 时该分解反应的化学平衡常数
时该分解反应的化学平衡常数 ,实验步骤如下:
,实验步骤如下:
(Ⅰ)关闭
 ,打开
,打开 和
和 ,开启真空泵抽气至测压仪数值稳定后关闭
,开启真空泵抽气至测压仪数值稳定后关闭 。
。(Ⅱ)关闭
 ,
,测得
 时压强为
时压强为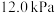 。
。①请在空白处完善步骤Ⅱ的实验操作。
②若步骤I中测压仪数值未稳定即关闭
 ,
, 测量值
测量值
您最近一年使用:0次
名校
9 . 常温下,向某溶剂(不参与反应)中加入一定量X、Y和M,所得溶液中同时存在如下平衡:
(ⅰ)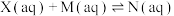
(ⅱ)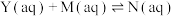
(ⅲ)
X、Y的物质的量浓度 随反应时间
随反应时间 的变化关系如图所示,300 s后反应体系达到平衡状态。
的变化关系如图所示,300 s后反应体系达到平衡状态。
下列说法正确的是
(ⅰ)
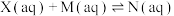
(ⅱ)
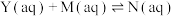
(ⅲ)

X、Y的物质的量浓度
 随反应时间
随反应时间 的变化关系如图所示,300 s后反应体系达到平衡状态。
的变化关系如图所示,300 s后反应体系达到平衡状态。下列说法正确的是
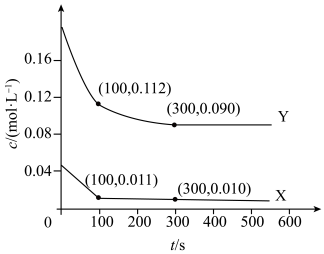
A.100~300 s内,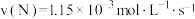 |
B. 时,反应(ⅲ)的逆反应速率大于正反应速率 时,反应(ⅲ)的逆反应速率大于正反应速率 |
C.若反应(ⅲ)的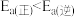 ,则X比Y更稳定 ,则X比Y更稳定 |
D.若再向容器中加入上述溶剂,则 、 、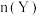 均不变 均不变 |
您最近一年使用:0次
2024-03-22更新
|
588次组卷
|
3卷引用:2024届广东省深圳市高三下学期一模考试化学试卷
名校
10 . 已知:
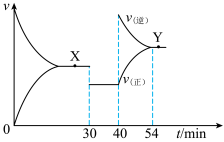
 ,一定条件下CO与H2O(g)反应的
,一定条件下CO与H2O(g)反应的 图像如下。30 min、40 min时分别只改变一个条件。下列说法错误的是
图像如下。30 min、40 min时分别只改变一个条件。下列说法错误的是

 ,一定条件下CO与H2O(g)反应的
,一定条件下CO与H2O(g)反应的 图像如下。30 min、40 min时分别只改变一个条件。下列说法错误的是
图像如下。30 min、40 min时分别只改变一个条件。下列说法错误的是
A.平衡常数: | B.40 min时,增加CO2或H2的浓度 |
| C.30 min时,降低反应体系的温度 | D.CO转化率: |
您最近一年使用:0次



