名校
1 . 下列对于反应 的有关说法正确的是
的有关说法正确的是
 的有关说法正确的是
的有关说法正确的是A.加入催化剂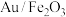 ,反应的焓变 ,反应的焓变 变小 变小 |
B.该反应的 , , |
| C.向固定容积的反应体系中充入氦气,压强增大,因此反应速率加快 |
D.其他条件相同,增大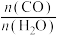 ,反应的平衡常数K不变 ,反应的平衡常数K不变 |
您最近一年使用:0次
名校
2 . 哈伯法合成氨的反应原理为 ,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是
,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是
 ,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是
,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是A.该反应在低温下能自发进行,则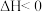 |
B.选用高效催化剂,可降低该反应的 |
C.其它条件不变,增大起始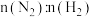 的比值,可提高N2的平衡转化率 的比值,可提高N2的平衡转化率 |
| D.提高体系的压强可增大反应的化学平衡常数 |
您最近一年使用:0次
2024-05-08更新
|
121次组卷
|
2卷引用:江苏省徐州市第一中学2023-2024学年高二下学期4月期中考试化学试题
3 . 镀锌钢板广泛运用于汽车行业。当镀层质量不合格时,先利用强酸将镀件表面的镀锌层清洗,再检测其中含有的 、
、 、
、 等离子的浓度。
等离子的浓度。
(1)测定原理:EDTA(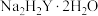 )可与
)可与 、
、 、
、 等多种金属离子形成络合物,如下表。其中
等多种金属离子形成络合物,如下表。其中 是乙二胺四乙酸根(
是乙二胺四乙酸根( )的简写。
)的简写。
①EDTA在水溶液中可看作“六元酸”的一种微粒可表示为___________ (用H、Y表示)。
②表中最稳定的金属络合物是___________ (填化学式)。
(2)测定过程:已知EDTA标准溶液滴定 的相关信息如下表:
的相关信息如下表:
可采用连续滴定法测定 、
、 、
、 的浓度,具体步骤如下:
的浓度,具体步骤如下:
I.先测定 (
( 、
、 不影响Fe3+的滴定):
不影响Fe3+的滴定):
请补充完整实验方案:
①按规定操作分别将0.01000 EDTA标准溶液和待测溶液[其中
EDTA标准溶液和待测溶液[其中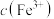 约为0.01
约为0.01 ]装入如图所示的滴定管中;
]装入如图所示的滴定管中;___________ 。(可选用的实验试剂有:磺基水杨酸、氨水溶液、盐酸溶液)
③实验测得 的浓度偏大,其原因可能是
的浓度偏大,其原因可能是___________ 。
II.再测定 :在
:在 的锥形瓶中继续加入适量过硫酸铵
的锥形瓶中继续加入适量过硫酸铵 ,轻微摇晃使
,轻微摇晃使 转化为
转化为 ,继续用EDTA标准溶液滴定到终点。写出
,继续用EDTA标准溶液滴定到终点。写出 转化为
转化为 的离子方程式:
的离子方程式:___________ 。
III.最后测定 :在
:在 的锥形瓶中继续加入一定量过量的EDTA标准溶液,调节溶液pH至5.0~6.0,再用
的锥形瓶中继续加入一定量过量的EDTA标准溶液,调节溶液pH至5.0~6.0,再用 标准溶液滴定到终点。
标准溶液滴定到终点。 不影响
不影响 滴定的原因是
滴定的原因是___________ 。
 、
、 、
、 等离子的浓度。
等离子的浓度。(1)测定原理:EDTA(
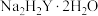 )可与
)可与 、
、 、
、 等多种金属离子形成络合物,如下表。其中
等多种金属离子形成络合物,如下表。其中 是乙二胺四乙酸根(
是乙二胺四乙酸根( )的简写。
)的简写。| 络合反应 | 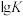 (K为平衡常数) |
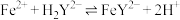 | 14.3 |
 | 16.5 |
 | 25.1 |
②表中最稳定的金属络合物是
(2)测定过程:已知EDTA标准溶液滴定
 的相关信息如下表:
的相关信息如下表:| 滴定对象 |  |
| 滴定时溶液pH范围 | 1.5~2.0 |
| 指示剂 | 磺基水杨酸 |
| 滴定终点现象 | 紫红色→亮黄色 |
 、
、 、
、 的浓度,具体步骤如下:
的浓度,具体步骤如下:I.先测定
 (
( 、
、 不影响Fe3+的滴定):
不影响Fe3+的滴定):请补充完整实验方案:
①按规定操作分别将0.01000
 EDTA标准溶液和待测溶液[其中
EDTA标准溶液和待测溶液[其中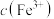 约为0.01
约为0.01 ]装入如图所示的滴定管中;
]装入如图所示的滴定管中;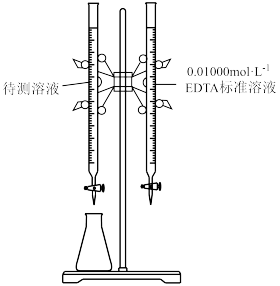
③实验测得
 的浓度偏大,其原因可能是
的浓度偏大,其原因可能是II.再测定
 :在
:在 的锥形瓶中继续加入适量过硫酸铵
的锥形瓶中继续加入适量过硫酸铵 ,轻微摇晃使
,轻微摇晃使 转化为
转化为 ,继续用EDTA标准溶液滴定到终点。写出
,继续用EDTA标准溶液滴定到终点。写出 转化为
转化为 的离子方程式:
的离子方程式:III.最后测定
 :在
:在 的锥形瓶中继续加入一定量过量的EDTA标准溶液,调节溶液pH至5.0~6.0,再用
的锥形瓶中继续加入一定量过量的EDTA标准溶液,调节溶液pH至5.0~6.0,再用 标准溶液滴定到终点。
标准溶液滴定到终点。 不影响
不影响 滴定的原因是
滴定的原因是
您最近一年使用:0次
4 . 反应 是汽车尾气无害化处理中的反应之一、下列说法正确的是
是汽车尾气无害化处理中的反应之一、下列说法正确的是
 是汽车尾气无害化处理中的反应之一、下列说法正确的是
是汽车尾气无害化处理中的反应之一、下列说法正确的是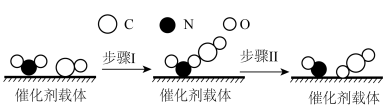
A.该反应的 , , |
B.该反应的平衡常数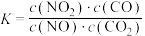 |
C.如图所示的反应机理中,步骤I可理解为 和CO仅在一定方向上才发生有效碰撞 和CO仅在一定方向上才发生有效碰撞 |
D.反应中每消耗22.24L  ,转移电子的数目为 ,转移电子的数目为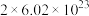 |
您最近一年使用:0次
5 . 反应2SO2(g) + O2(g) 2SO3(g) ΔH =-196.6 kJ·mol−1因SO2在催化剂表面与O2接触而得名,反应过程示意图如图:
2SO3(g) ΔH =-196.6 kJ·mol−1因SO2在催化剂表面与O2接触而得名,反应过程示意图如图:
 2SO3(g) ΔH =-196.6 kJ·mol−1因SO2在催化剂表面与O2接触而得名,反应过程示意图如图:
2SO3(g) ΔH =-196.6 kJ·mol−1因SO2在催化剂表面与O2接触而得名,反应过程示意图如图:
| A.反应①的活化能比反应②高 |
| B.使用催化剂能改变反应途径,降低反应的焓变 |
| C.图示过程中既有S-O的断裂,又有S-O的形成 |
| D.其他条件不变,升高体系的温度,该反应的平衡常数K增大 |
您最近一年使用:0次
6 . 纳米级材料Cu2O有非常优良的催化性能。工业上在高温条件下用炭粉还原CuO制得: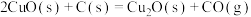
 。下列说法正确的是
。下列说法正确的是
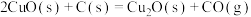
 。下列说法正确的是
。下列说法正确的是| A.该反应在任何温度下均可自发进行 |
| B.该反应的平衡常数K=c(CO) |
| C.其他条件相同,加入更多的炭粉,可以提高CuO的平衡转化率 |
| D.反应中生成22.4L,转移的电子数目为2×6.02×1023 |
您最近一年使用:0次
2024·江苏·模拟预测
7 . 对于二氧化硫的催化氧化反应:2SO2(g)+O2(g) 2SO3(g),下列有关说法正确的是
2SO3(g),下列有关说法正确的是
 2SO3(g),下列有关说法正确的是
2SO3(g),下列有关说法正确的是| A.该反应的ΔS>0 |
B.该反应平衡常数的表达式为K=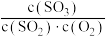 |
| C.反应中每消耗22.4LO2(标准状况),转移电子数约为2×6.02×1023 |
| D.温度不变,提高O2的起始浓度或增大反应压强,均能提高反应速率和SO2的转化率 |
您最近一年使用:0次
8 . 在一定容积的密闭容器中,进行如下化学反应: ,其化学平衡常数K和温度T的关系如表所示:
,其化学平衡常数K和温度T的关系如表所示:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=____________ 。
(2)该反应为________ (填“吸热”或“放热”)反应。
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________ ℃。该温度下加入1 mol CO2(g)和1 mol H2(g),充分反应,达到平衡时,CO2的转化率为________ 。
 ,其化学平衡常数K和温度T的关系如表所示:
,其化学平衡常数K和温度T的关系如表所示:T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=
(2)该反应为
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
您最近一年使用:0次
名校
解题方法
9 . 一定条件下CO2与NH3合成尿素:2NH3(g)+CO2(g)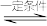 CO(NH2)2(s)+H2O(l) ΔH,其反应过程中能量变化如图所示,下列有关说法正确的是
CO(NH2)2(s)+H2O(l) ΔH,其反应过程中能量变化如图所示,下列有关说法正确的是
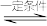 CO(NH2)2(s)+H2O(l) ΔH,其反应过程中能量变化如图所示,下列有关说法正确的是
CO(NH2)2(s)+H2O(l) ΔH,其反应过程中能量变化如图所示,下列有关说法正确的是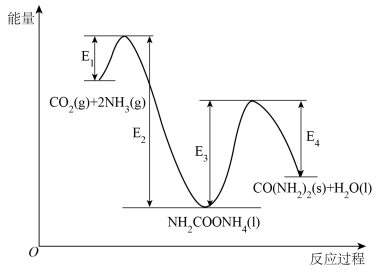
| A.ΔH>0 |
B.该反应平衡常数K=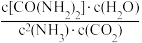 |
| C.升高温度,可分离得到更多的NH2COONH4(l) |
| D.合成尿素的反应快慢主要取决于NH2COONH4(l)的分解速率 |
您最近一年使用:0次
名校
解题方法
10 . 对于反应2SO2(g)+O2(g) 2SO3(g) ΔH<0,在其他条件相同时,下列说法正确的是
2SO3(g) ΔH<0,在其他条件相同时,下列说法正确的是
 2SO3(g) ΔH<0,在其他条件相同时,下列说法正确的是
2SO3(g) ΔH<0,在其他条件相同时,下列说法正确的是| A.增大压强,平衡正向移动,化学平衡常数增大 |
| B.加入V2O5,改变了反应的活化能,平衡不发生移动 |
| C.升高温度,v(逆)增大,v(正)减小,平衡逆向移动 |
| D.当c(SO2)∶c(O2)=2∶1时,可以判断该反应一定已经达到化学平衡 |
您最近一年使用:0次



