名校
解题方法
1 . 煤和石油是重要的能源物质,一方面对其开发利用推动人类社会快速进入工业文明时代,另一方面化石燃料燃烧产生 带来的环境问题日益凸显,“碳中和”已成为新时代绿色发展理念。煤经汽化、液化后再利用,可提高效能、降低污染,其常见原理为:
带来的环境问题日益凸显,“碳中和”已成为新时代绿色发展理念。煤经汽化、液化后再利用,可提高效能、降低污染,其常见原理为:
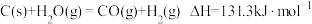
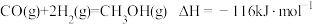
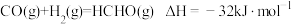
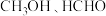 等产物在化工生产中都有广泛用途。对于反应
等产物在化工生产中都有广泛用途。对于反应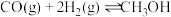 ,下列说法
,下列说法不 正确的是
 带来的环境问题日益凸显,“碳中和”已成为新时代绿色发展理念。煤经汽化、液化后再利用,可提高效能、降低污染,其常见原理为:
带来的环境问题日益凸显,“碳中和”已成为新时代绿色发展理念。煤经汽化、液化后再利用,可提高效能、降低污染,其常见原理为: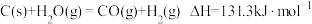
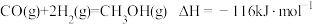
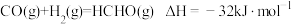
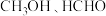 等产物在化工生产中都有广泛用途。对于反应
等产物在化工生产中都有广泛用途。对于反应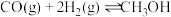 ,下列说法
,下列说法A.反应的平衡常数可表示为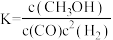 |
B.反应活化能: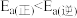 |
C. 和 和 充分反应,转移电子数目约为 充分反应,转移电子数目约为 个 个 |
D.平衡后增大容器的体积, 、 、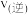 都减小 都减小 |
您最近一年使用:0次
2022-05-14更新
|
550次组卷
|
4卷引用:江苏省盐城市2022届高三第三次模拟考试化学试题
江苏省盐城市2022届高三第三次模拟考试化学试题(已下线)2022年江苏卷高考真题变式题1-13江苏省南京市中华中学2022-2023学年高三上学期期末考试化学试题(已下线)江苏省2022年普通高中学业水平选择性考试变式题(选择题6-10)
2 . CO用途广泛,工业应用时离不开平衡思想的指导:
Ⅰ.在某一容积为5 L的体积不变的密闭容器内,加入0.3 mol 的CO和0.3 mol的H2O,在有催化剂存在和800 ℃的条件下加热,发生如下反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如图:
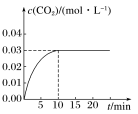
(1)若保持温度和容器的体积不变,向上述平衡体系中,再充入0.3 mol的水蒸气,重新达到平衡后,H2O的转化率___________ (填“升高”“降低”或“不变”)。
(2)在催化剂存在和800 ℃的条件下,在某一时刻测得c(CO)=c(H2O)=0.09 mol·L-1;c(CO2)=c(H2)=0.13 mol·L-1,则此时正、逆反应速率的大小: 正
正 ___________  逆(填“>”“<”或“=”)。
逆(填“>”“<”或“=”)。
Ⅱ.还原法炼铅,包含反应PbO (s)+CO(g)=Pb(s)+CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表:
(3)该反应的ΔH___________ 0(填“>”“<”或“=”)。
(4)当lg K=1,在恒容密闭容器中加入PbO并通入CO,达平衡时,混合气体中CO的体积分数为___________ (保留两位有效数字);若向容器中充入一定量的CO气体后,平衡发生移动,再次达到平衡时,CO的百分含量___________ (填“增大”“减小”或“不变”)。
Ⅰ.在某一容积为5 L的体积不变的密闭容器内,加入0.3 mol 的CO和0.3 mol的H2O,在有催化剂存在和800 ℃的条件下加热,发生如下反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如图:

(1)若保持温度和容器的体积不变,向上述平衡体系中,再充入0.3 mol的水蒸气,重新达到平衡后,H2O的转化率
(2)在催化剂存在和800 ℃的条件下,在某一时刻测得c(CO)=c(H2O)=0.09 mol·L-1;c(CO2)=c(H2)=0.13 mol·L-1,则此时正、逆反应速率的大小:
 正
正  逆(填“>”“<”或“=”)。
逆(填“>”“<”或“=”)。Ⅱ.还原法炼铅,包含反应PbO (s)+CO(g)=Pb(s)+CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表:
| 温度/℃ | 300 | 727 | 1 227 |
| lg K | 6.17 | 2.87 | 1.24 |
(4)当lg K=1,在恒容密闭容器中加入PbO并通入CO,达平衡时,混合气体中CO的体积分数为
您最近一年使用:0次
3 . 天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷。
(1)①已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ∆H1;
CO(g)+H2O(g)=CO2(g)+H2(g) ∆H2;
2CO(g)+O2(g)=2CO2(g) ∆H3;
则CO2(g)+CH4(g)=2CO(g)+2H2(g)的∆H=___________ 。
②天然气中的少量H2S杂质常用氨水吸收,产物为NH4HS。向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式___________ 。
(2)天然气的一个重要用途是制取H2,其原理为:CO2(g)+CH4(g) 2CO(g)+2H2(g)。该反应的平衡常数表达式为
2CO(g)+2H2(g)。该反应的平衡常数表达式为___________ ;在密闭容器中通入物质的量浓度均为0.1 mol/L的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如图20-1所示。则压强P1___________ P2(填“大于”或“小于");压强为P2时,在Y点:v(正)___________ v(逆)(填“大于”“小于”或“等于”)。
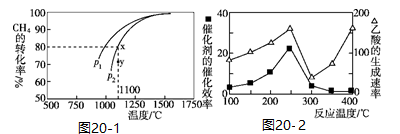
(3)CH4和CO2合成乙酸,某工业生产中以CuAlO2为合成的催化剂,在不同温度下催化剂的催化效率与乙酸的生成速率如图20-2所示。250℃~300℃时,温度升高而乙酸的生成速率降低的原因是___________ ,将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为___________ 。
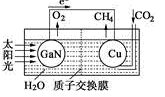
(4)科学家用氮化镓材料与铜组装如下图所示人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4.写出铜电极表面的电极反应式___________ 。
(1)①已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ∆H1;
CO(g)+H2O(g)=CO2(g)+H2(g) ∆H2;
2CO(g)+O2(g)=2CO2(g) ∆H3;
则CO2(g)+CH4(g)=2CO(g)+2H2(g)的∆H=
②天然气中的少量H2S杂质常用氨水吸收,产物为NH4HS。向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式
(2)天然气的一个重要用途是制取H2,其原理为:CO2(g)+CH4(g)
 2CO(g)+2H2(g)。该反应的平衡常数表达式为
2CO(g)+2H2(g)。该反应的平衡常数表达式为
(3)CH4和CO2合成乙酸,某工业生产中以CuAlO2为合成的催化剂,在不同温度下催化剂的催化效率与乙酸的生成速率如图20-2所示。250℃~300℃时,温度升高而乙酸的生成速率降低的原因是
(4)科学家用氮化镓材料与铜组装如下图所示人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4.写出铜电极表面的电极反应式

您最近一年使用:0次
名校
4 . CO用途广泛,工业应用时离不开平衡思想的指导:
Ⅰ.在某一容积为5 L的体积不变的密闭容器内,加入0.3 mol 的CO和0.3 mol的H 2O,在催化剂存在和800 ℃的条件下加热,发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如下图:
CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如下图:
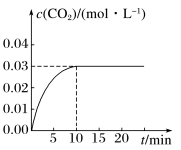
(1)根据图上数据,该温度(800 ℃)下的平衡常数K=________ 。
(2)在体积不变的条件下,改变下列条件能使平衡常数K增大的有______ (填字母)。
A 升高温度 B 降低温度 C 增大压强 D 减小压强 E 加入催化剂 G 移出一氧化碳气体
(3)若保持温度和容器的体积不变,在(1)中上述平衡体系中,再充入0.3 mol的水蒸气,重新达到平衡后,H2O的转化率________ (填“升高”“降低”或“不变”)。
(4)在催化剂存在和800 ℃的条件下,在某一时刻测得c(CO)=c(H2O)=0.09 mol·L-1;c(CO2)=c(H2)=0.13 mol·L-1,则此时正、逆反应速率的大小:v正___ v逆(填“>”“<”或“=”)。
Ⅱ.还原法炼铅,包含反应PbO(s)+CO(g)=Pb(s)+CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表:
(5)该反应的ΔH____ 0(填“>”“<”或“=”)。
(6)当lg K=1,在恒容密闭容器中放入PbO并通入CO,达平衡时,混合气体中CO的体积分数为______ (保留两位有效数字);若向容器中充入一定量的CO气体后,平衡发生移动,再次达到平衡时,CO的百分含量______ (填“增大”“减小”或“不变”)。
Ⅰ.在某一容积为5 L的体积不变的密闭容器内,加入0.3 mol 的CO和0.3 mol的H 2O,在催化剂存在和800 ℃的条件下加热,发生如下反应:CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如下图:
CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如下图:
(1)根据图上数据,该温度(800 ℃)下的平衡常数K=
(2)在体积不变的条件下,改变下列条件能使平衡常数K增大的有
A 升高温度 B 降低温度 C 增大压强 D 减小压强 E 加入催化剂 G 移出一氧化碳气体
(3)若保持温度和容器的体积不变,在(1)中上述平衡体系中,再充入0.3 mol的水蒸气,重新达到平衡后,H2O的转化率
(4)在催化剂存在和800 ℃的条件下,在某一时刻测得c(CO)=c(H2O)=0.09 mol·L-1;c(CO2)=c(H2)=0.13 mol·L-1,则此时正、逆反应速率的大小:v正
Ⅱ.还原法炼铅,包含反应PbO(s)+CO(g)=Pb(s)+CO2(g) ΔH,该反应的平衡常数的对数值与温度的关系如下表:
| 温度/℃ | 300 | 727 | 1 227 |
| lg K | 6.17 | 2.87 | 1.24 |
(6)当lg K=1,在恒容密闭容器中放入PbO并通入CO,达平衡时,混合气体中CO的体积分数为
您最近一年使用:0次
2020-11-05更新
|
118次组卷
|
6卷引用:江苏省无锡市太湖高级中学2021-2022学年高二下学期3月月考化学试题



