1 . 在一定温度下,将3molA和1molB两种气体相混合于1L的密闭容器中,发生以下反应: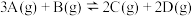 。2min末反应达到平衡状态,生成了1.2molD。(用三段式解题)
。2min末反应达到平衡状态,生成了1.2molD。(用三段式解题)
(1)A的转化率为多少_______ ?
(2)求此温度下的平衡常数_______ ?
(3)求平衡时D的体积分数_______ (即物质的量分数)?
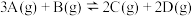 。2min末反应达到平衡状态,生成了1.2molD。(用三段式解题)
。2min末反应达到平衡状态,生成了1.2molD。(用三段式解题)(1)A的转化率为多少
(2)求此温度下的平衡常数
(3)求平衡时D的体积分数
您最近一年使用:0次
2 . 在一定条件下,向容积为2 L的恒容密闭容器中充入1 mol CH3OH(g)和3 mol H2O(g),CH3OH(g)+H2O(g) CO2(g)+3H2(g) △H=+49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
CO2(g)+3H2(g) △H=+49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
(1)该条件下反应的化学平衡常数表达式为K=___________ 。
(2)平衡时升高温度,化学平衡常数的变化为___________ (填“变大”、“变小”或“不变”)。
(3)该条件下反应到达平衡时,CH3OH的转化率为___________ ,混合气体的压强是反应前的___________ 倍。
(4)该条件下判断该反应达平衡状态的依据是(填序号)___________ 。
a.v正(CH3OH)=v逆(CO2) b.混合气体的密度不变
c.c(CH3OH)=c(H2O) d.混合气体的总物质的量不变
(5)将体积压缩为原来的一半,下列描述正确的是( )
a.正反应速率减小,逆反应速率增大 b.正反应速率增大,逆反应速率增大
c.正反应速率小于逆反应速率 d.c(CO2)减小
 CO2(g)+3H2(g) △H=+49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
CO2(g)+3H2(g) △H=+49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则(1)该条件下反应的化学平衡常数表达式为K=
(2)平衡时升高温度,化学平衡常数的变化为
(3)该条件下反应到达平衡时,CH3OH的转化率为
(4)该条件下判断该反应达平衡状态的依据是(填序号)
a.v正(CH3OH)=v逆(CO2) b.混合气体的密度不变
c.c(CH3OH)=c(H2O) d.混合气体的总物质的量不变
(5)将体积压缩为原来的一半,下列描述正确的是
a.正反应速率减小,逆反应速率增大 b.正反应速率增大,逆反应速率增大
c.正反应速率小于逆反应速率 d.c(CO2)减小
您最近一年使用:0次
2021-01-13更新
|
308次组卷
|
2卷引用:广东省佛山市实验中学2022-2023学年高二上学期第一次段考化学试题
名校
3 . 已知可逆反应CO(g)+H2O(g) CO2(g)+H2(g),达到平衡时,K=
CO2(g)+H2(g),达到平衡时,K= ,K是常数,只与温度有关,与浓度无关。
,K是常数,只与温度有关,与浓度无关。
(1)830K时,若起始时c(CO)=2mol·L-1,c(H2O)=3mol·L-1,平衡时CO的转化率为60%,水蒸气的转化率为___ ;K值为___ 。
(2)830K时,若只将起始时c(H2O)改为6mol·L-1,则水蒸气的转化率为___ 。
(3)若830K时,起始加入物质为CO和H2O,起始浓度c(CO)=amol·L-1,c(H2O)=bmol·L-1,过段时间,达到平衡时H2的平衡浓度c(H2)=cmol·L-1
①a、b、c之间的关系式是___ ;
②当a=b时,a=___ c。
 CO2(g)+H2(g),达到平衡时,K=
CO2(g)+H2(g),达到平衡时,K= ,K是常数,只与温度有关,与浓度无关。
,K是常数,只与温度有关,与浓度无关。(1)830K时,若起始时c(CO)=2mol·L-1,c(H2O)=3mol·L-1,平衡时CO的转化率为60%,水蒸气的转化率为
(2)830K时,若只将起始时c(H2O)改为6mol·L-1,则水蒸气的转化率为
(3)若830K时,起始加入物质为CO和H2O,起始浓度c(CO)=amol·L-1,c(H2O)=bmol·L-1,过段时间,达到平衡时H2的平衡浓度c(H2)=cmol·L-1
①a、b、c之间的关系式是
②当a=b时,a=
您最近一年使用:0次
2020-10-20更新
|
544次组卷
|
11卷引用:广东省惠州市龙门县高级中学2023-2024学年高二上学期期中考试化学试题
广东省惠州市龙门县高级中学2023-2024学年高二上学期期中考试化学试题2014-2015河北枣强中学高二上学期期末考试化学试卷2016-2017学年新疆哈密地区第二中学高二上学期期末考试化学试卷北京市昌平临川育人学校2017-2018学年高二上学期期中考试化学试题吉林省梅河口市朝鲜族中学2019-2020学年高二上学期期末考试化学试题陕西省黄陵县中学2020-2021学年高二上学期期中考试化学试题(高新部)鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第2节 化学反应的限度课时1 化学平衡常数 平衡转化率人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 课时2 化学平衡常数及相关计算江苏省南菁高级中学2020-2021学年度高二上学期第一次阶段性考试化学(强化班)试题选择性必修1(SJ)专题2第二单元课时3 化学平衡常数平衡转化率2.2.3化学平衡常数 课后
4 . 将HI(g)置于密闭容器中,某温度下发生下列变化:2HI(g)⇌H2(g)+I2(g) △H<0
(1)该反应平衡常数的表达式为K=___ 。
(2)当反应达到平衡时c(I2)=0.5mol/L,c(HI)=4mol/L,则c(H2)为____ ,HI的分解率为____ 。
(3)若该反应800℃时达到平衡状态,且平衡常数为1.0,某时刻,测得容器内各物质的溶度分别为c(HI)=2.0mol/L,c(I2)=1.0mol/L,c(H2)=1.0mol/L,则该时刻,反应向____ (填“正向”或“逆向”,下同)进行。
(1)该反应平衡常数的表达式为K=
(2)当反应达到平衡时c(I2)=0.5mol/L,c(HI)=4mol/L,则c(H2)为
(3)若该反应800℃时达到平衡状态,且平衡常数为1.0,某时刻,测得容器内各物质的溶度分别为c(HI)=2.0mol/L,c(I2)=1.0mol/L,c(H2)=1.0mol/L,则该时刻,反应向
您最近一年使用:0次
名校
5 . 800K时,将0.1 mo A(g)和0.2 molB(g)充人体积为1 L的固定容积反应器中,发生如下反应:A(g)+2B(g)⇌2 C(g)+D(g),达到平衡时A的物质的量分数为20%。
(1)求达平衡时B的转化率α(B)___________ ;
(2)求该温度下的平衡常数K___________ ;
(3)若起始A的分压为10 kPa,求Kp___________ 。
(4)若在体积固定的某容器中充入0.2 mol A、0.1 mol B、0.1 mol C、0.5 mol D,则此时是否为平衡状态,请计算说明___________ 。
(1)求达平衡时B的转化率α(B)
(2)求该温度下的平衡常数K
(3)若起始A的分压为10 kPa,求Kp
(4)若在体积固定的某容器中充入0.2 mol A、0.1 mol B、0.1 mol C、0.5 mol D,则此时是否为平衡状态,请计算说明
您最近一年使用:0次
解题方法
6 . 在一定温度下,向10L密闭容器中充入5.2molNO2,达到平衡时,c(N2O4)=0.16mol·L-1。
请计算该温度下此反应的平衡常数K(请用三段式的方法写出计算过程)。
请计算该温度下此反应的平衡常数K(请用三段式的方法写出计算过程)。
您最近一年使用:0次



