名校
1 . 完全燃烧某气态烷烃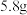 ,得到
,得到 二氧化碳和
二氧化碳和 水。求:
水。求:
(1)此烷烃的相对分子质量_____ 。
(2)此烷烃的化学式_____ 。
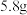 ,得到
,得到 二氧化碳和
二氧化碳和 水。求:
水。求:(1)此烷烃的相对分子质量
(2)此烷烃的化学式
您最近一年使用:0次
解题方法
2 . 完成下列题目:
(1)铝原子的个数约为 ,该铝原子的质量为
,该铝原子的质量为__________ 。
(2) 的质量为
的质量为___________ 。
(3) 含有的氢分子(
含有的氢分子( )数为
)数为__________ 。
(4)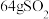 的物质的量为
的物质的量为__________ ;原子总数为__________ 。
(5)0.01mol某物质质量为1.08g,该物质的摩尔质量为__________ 。
(1)铝原子的个数约为
 ,该铝原子的质量为
,该铝原子的质量为(2)
 的质量为
的质量为(3)
 含有的氢分子(
含有的氢分子( )数为
)数为(4)
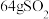 的物质的量为
的物质的量为(5)0.01mol某物质质量为1.08g,该物质的摩尔质量为
您最近一年使用:0次
3 . 饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: 。请回答下列问题:
。请回答下列问题:
(1)上述反应中,被氧化的元素是___________ ,还原产物是___________ 。
(2)用“双线桥法”表示反应中电子转移的方向和数目:___________ 。

(3)反应中每生成1个 ,转移
,转移___________ 个电子。
(4)请配平下列离子方程式:___________ 。
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
(5)已知 、
、 、
、 、
、 、
、 均有还原性,它们在酸性溶液中还原性的强弱顺序为:
均有还原性,它们在酸性溶液中还原性的强弱顺序为: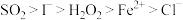 ,则下列反应不能发生的是:___________。
,则下列反应不能发生的是:___________。
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: 。请回答下列问题:
。请回答下列问题:(1)上述反应中,被氧化的元素是
(2)用“双线桥法”表示反应中电子转移的方向和数目:

(3)反应中每生成1个
 ,转移
,转移(4)请配平下列离子方程式:
___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________
(5)已知
 、
、 、
、 、
、 、
、 均有还原性,它们在酸性溶液中还原性的强弱顺序为:
均有还原性,它们在酸性溶液中还原性的强弱顺序为: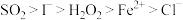 ,则下列反应不能发生的是:___________。
,则下列反应不能发生的是:___________。A.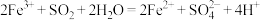 |
B. |
C.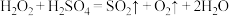 |
D. |
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题。
(1)等质量的CO和CO2,物质的量之比为___________ ;氧原子个数之比为___________ 。
(2)1.5 mol H2SO4的质量是___________ g,其中含有___________ mol H。
(3)9.03×1023个氨分子含___________ mol NH3,___________ mol电子。
(1)等质量的CO和CO2,物质的量之比为
(2)1.5 mol H2SO4的质量是
(3)9.03×1023个氨分子含
您最近一年使用:0次
名校
解题方法
5 . 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。二氧化碳加氢制甲醇的总反应可表示为:


该反应一般认为通过如下步骤来实现:
反应①

反应②

回答下列问题:
(1)
___________ 
(2)有利于提高 转化为
转化为 平衡转化率的措施有
平衡转化率的措施有___________ (填编号)。
A.升高温度 B.降低温度 C.增大压强
D.降低压强 E.使用催化剂 F.增大 和
和 的初始投料比
的初始投料比
(3)二氧化碳加氢制甲醇的总反应按 投料,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
投料,在不同条件下达到平衡,设体系中甲醇的物质的量分数为 ,在
,在 下的
下的 随温度
随温度 变化,在
变化,在 下的
下的 随压强
随压强 变化如图所示。
变化如图所示。
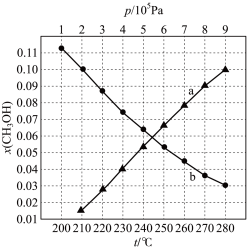
①图中对应在 下的
下的 随温度
随温度 变化的等压过程的曲线是
变化的等压过程的曲线是___________ (填“ ”或“
”或“ ”)。判断理由是
”)。判断理由是___________ 。
② 时,反应条件可能为
时,反应条件可能为___________ 或___________ 。
③ 时,计算
时,计算 的平衡转化率,写出计算过程
的平衡转化率,写出计算过程___________ 。


该反应一般认为通过如下步骤来实现:
反应①


反应②


回答下列问题:
(1)


(2)有利于提高
 转化为
转化为 平衡转化率的措施有
平衡转化率的措施有A.升高温度 B.降低温度 C.增大压强
D.降低压强 E.使用催化剂 F.增大
 和
和 的初始投料比
的初始投料比(3)二氧化碳加氢制甲醇的总反应按
 投料,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
投料,在不同条件下达到平衡,设体系中甲醇的物质的量分数为 ,在
,在 下的
下的 随温度
随温度 变化,在
变化,在 下的
下的 随压强
随压强 变化如图所示。
变化如图所示。
①图中对应在
 下的
下的 随温度
随温度 变化的等压过程的曲线是
变化的等压过程的曲线是 ”或“
”或“ ”)。判断理由是
”)。判断理由是②
 时,反应条件可能为
时,反应条件可能为③
 时,计算
时,计算 的平衡转化率,写出计算过程
的平衡转化率,写出计算过程
您最近一年使用:0次
名校
解题方法
6 . 请根据物质的量的相关概念及计算公式,完成下列各题:
(1)请填写下表:
(2)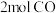 与
与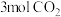 的质量之比
的质量之比__________ ;分子数之比为__________ ;含氧原子的数目之比为__________ 。
(3)将含杂质软锰矿粉末 与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得
与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得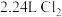 (标准状况下)。请回答下列问题:
(标准状况下)。请回答下列问题:
反应中被氧化的 的物质的量为
的物质的量为__________ mol,软锰矿中 的质量分数为
的质量分数为__________ 。
(1)请填写下表:
物质 | 摩尔质量 | 物质的量 | 质量 | 分子或离子数目 |
|
| |||
|
|
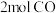 与
与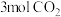 的质量之比
的质量之比(3)将含杂质软锰矿粉末
 与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得
与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得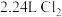 (标准状况下)。请回答下列问题:
(标准状况下)。请回答下列问题:反应中被氧化的
 的物质的量为
的物质的量为 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
7 . 为了防控疫情,家居、学校等公共场所都要定时进行消毒。
Ⅰ.工业上使用氯气与氢氧化钠反应制取“84消毒液”
(1)写出“84消毒液”中的有效成分___________ 。
(2)“84消毒液”使用时应按比例稀释,放置20~30min,放置过程中有生成碳酸氢钠,该反应的离子方程式为___________ 。
Ⅱ.“消毒液”中氯元素的存在形态与溶液的pH关系如表:
(3)写出pH降低时产生氯气的离子方程式___________ 。
Ⅲ.同学猜测“84消毒液”(以下简称“84”)可漂白米醋【米醋是一种用稻谷酿制的食用醋,含少量醋酸( ),因含有有机色素而成棕色】,进行了如下实验:
),因含有有机色素而成棕色】,进行了如下实验:
(4)实验二的目的是:
①排除米醋因为挥发产生刺激性气味气体的可能;
②___________ 。
(5)结合反应的方程式,解释实验一立即褪色的原因___________ 。
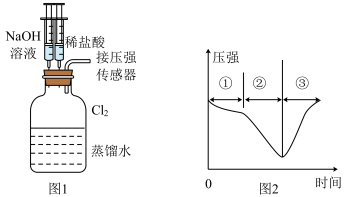
(6)若用氯气做如图1的实验,向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加NaOH溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是___________。
(7)若将一定量的氢气在氯气中燃烧,所得混合物用100mL 3.00 NaOH溶液恰好完全吸收,测得溶液中NaClO的物质的量浓度为0.6
NaOH溶液恰好完全吸收,测得溶液中NaClO的物质的量浓度为0.6 (忽略溶液体积的变化),则:
(忽略溶液体积的变化),则:
①所得溶液中 的物质的量浓度为
的物质的量浓度为___________ ;
②氯气和参加反应的氢气的物质的量之比为___________ 。
Ⅰ.工业上使用氯气与氢氧化钠反应制取“84消毒液”
(1)写出“84消毒液”中的有效成分
(2)“84消毒液”使用时应按比例稀释,放置20~30min,放置过程中有生成碳酸氢钠,该反应的离子方程式为
Ⅱ.“消毒液”中氯元素的存在形态与溶液的pH关系如表:
| 溶液pH | >9 | 5~6 | 4~5 | 2~3 | <2 |
| 主要成分 | NaClO | HCl与NaClO(少量) | HCl与 (少量) (少量) | HClO与 |  |
(3)写出pH降低时产生氯气的离子方程式
Ⅲ.同学猜测“84消毒液”(以下简称“84”)可漂白米醋【米醋是一种用稻谷酿制的食用醋,含少量醋酸(
 ),因含有有机色素而成棕色】,进行了如下实验:
),因含有有机色素而成棕色】,进行了如下实验:| 编号 | 实验一 | 实验二 |
| 实验操作 | 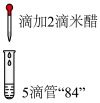 |  |
| 实验现象 | 滴入米醋后立即褪色,闻到刺激性气味 | 溶液为浅棕色,无刺激性气味 |
(4)实验二的目的是:
①排除米醋因为挥发产生刺激性气味气体的可能;
②
(5)结合反应的方程式,解释实验一立即褪色的原因
(6)若用氯气做如图1的实验,向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加NaOH溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是___________。

| A.阶段①说明氯气溶于水,溶于水的氯气全部与水反应 |
| B.阶段②的压强变小,该过程发生了氧化还原反应 |
C.阶段③的压强变大,该过程是NaClO分解产生 的原因 的原因 |
D.若将 换成 换成 ,所得的压强变化趋势与图2相似 ,所得的压强变化趋势与图2相似 |
(7)若将一定量的氢气在氯气中燃烧,所得混合物用100mL 3.00
 NaOH溶液恰好完全吸收,测得溶液中NaClO的物质的量浓度为0.6
NaOH溶液恰好完全吸收,测得溶液中NaClO的物质的量浓度为0.6 (忽略溶液体积的变化),则:
(忽略溶液体积的变化),则:①所得溶液中
 的物质的量浓度为
的物质的量浓度为②氯气和参加反应的氢气的物质的量之比为
您最近一年使用:0次
名校
8 . 反应: ,在密闭容器中达到平衡时
,在密闭容器中达到平衡时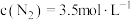 ,
,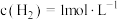 ,
,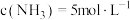 ,求:
,求:
(1) 和
和 的起始浓度
的起始浓度_________ 。
(2) 的转化率
的转化率_________ 。
(3)平衡时压强为开始时压强的百分之几_________ 。
(4)平衡时 占总体积的体积分数
占总体积的体积分数_________ 。
 ,在密闭容器中达到平衡时
,在密闭容器中达到平衡时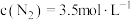 ,
,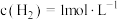 ,
,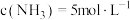 ,求:
,求:(1)
 和
和 的起始浓度
的起始浓度(2)
 的转化率
的转化率(3)平衡时压强为开始时压强的百分之几
(4)平衡时
 占总体积的体积分数
占总体积的体积分数
您最近一年使用:0次
名校
9 . Ⅰ.现用 固体配制100mL 0.1mol/L
固体配制100mL 0.1mol/L 溶液,可供选择的仪器有:玻璃棒、烧杯、电子天平、药匙、量筒、胶头滴管。回答下列问题:
溶液,可供选择的仪器有:玻璃棒、烧杯、电子天平、药匙、量筒、胶头滴管。回答下列问题:
(1)上述仪器中,还缺少的定量仪器是___________ 。
(2)经计算,需称取 固体质量为
固体质量为___________ g.
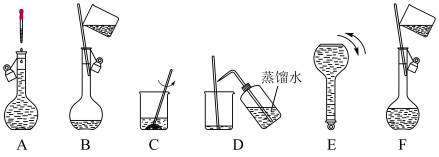
(3)将图中的实验步骤A~F按实验过程先后次序排列___→B→___→F→__→___;___________ 。
(4)将所配制的 溶液进行测定,发现浓度偏大,可能的原因是
溶液进行测定,发现浓度偏大,可能的原因是___________ 。
a.称量的 固体有杂质
固体有杂质
b.称量的 固体已经部分失去结晶水
固体已经部分失去结晶水
c.转移时没有洗涤烧杯和玻璃棒
d.定容时,加蒸馏水未到刻度线就停止滴加蒸馏水
(5)下列溶液中,与100mL 0.1mol/L 溶液中的
溶液中的 物质的量浓度相同的是
物质的量浓度相同的是______ 。
a.200mL 0.05mol/L 溶液 b.200mL 0.1mol/L NaCl溶液
溶液 b.200mL 0.1mol/L NaCl溶液
c.300mL 0.1mol/L 溶液 d.100mL 0.2mol/L NaOH溶液
溶液 d.100mL 0.2mol/L NaOH溶液
Ⅱ.回答下列问题:
(6)标准状况下,88g 的体积为
的体积为___________ L。
(7)___________ g 中的H原子数目与3mol
中的H原子数目与3mol 中的H原子数目相同。
中的H原子数目相同。
 固体配制100mL 0.1mol/L
固体配制100mL 0.1mol/L 溶液,可供选择的仪器有:玻璃棒、烧杯、电子天平、药匙、量筒、胶头滴管。回答下列问题:
溶液,可供选择的仪器有:玻璃棒、烧杯、电子天平、药匙、量筒、胶头滴管。回答下列问题:(1)上述仪器中,还缺少的定量仪器是
(2)经计算,需称取
 固体质量为
固体质量为(3)将图中的实验步骤A~F按实验过程先后次序排列___→B→___→F→__→___;

(4)将所配制的
 溶液进行测定,发现浓度偏大,可能的原因是
溶液进行测定,发现浓度偏大,可能的原因是a.称量的
 固体有杂质
固体有杂质b.称量的
 固体已经部分失去结晶水
固体已经部分失去结晶水c.转移时没有洗涤烧杯和玻璃棒
d.定容时,加蒸馏水未到刻度线就停止滴加蒸馏水
(5)下列溶液中,与100mL 0.1mol/L
 溶液中的
溶液中的 物质的量浓度相同的是
物质的量浓度相同的是a.200mL 0.05mol/L
 溶液 b.200mL 0.1mol/L NaCl溶液
溶液 b.200mL 0.1mol/L NaCl溶液c.300mL 0.1mol/L
 溶液 d.100mL 0.2mol/L NaOH溶液
溶液 d.100mL 0.2mol/L NaOH溶液Ⅱ.回答下列问题:
(6)标准状况下,88g
 的体积为
的体积为(7)
 中的H原子数目与3mol
中的H原子数目与3mol 中的H原子数目相同。
中的H原子数目相同。
您最近一年使用:0次
名校
10 . 回答下列问题:
(1) 个
个 的物质的量为
的物质的量为_______  ,质量为
,质量为_______  ,含有电子的物质的量为
,含有电子的物质的量为_______  ,这些
,这些 与
与_______ 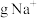 含有的电子数相同。
含有的电子数相同。
(2) 中含
中含 ,则
,则 的摩尔质量是
的摩尔质量是_______ 。R的相对原子质量约是_______ 。
(1)
 个
个 的物质的量为
的物质的量为 ,质量为
,质量为 ,含有电子的物质的量为
,含有电子的物质的量为 ,这些
,这些 与
与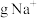 含有的电子数相同。
含有的电子数相同。(2)
 中含
中含 ,则
,则 的摩尔质量是
的摩尔质量是
您最近一年使用:0次