名校
解题方法
1 . 请根据物质的量的相关概念及计算公式,完成下列各题:
(1)请填写下表:
(2)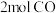 与
与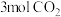 的质量之比
的质量之比__________ ;分子数之比为__________ ;含氧原子的数目之比为__________ 。
(3)将含杂质软锰矿粉末 与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得
与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得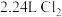 (标准状况下)。请回答下列问题:
(标准状况下)。请回答下列问题:
反应中被氧化的 的物质的量为
的物质的量为__________ mol,软锰矿中 的质量分数为
的质量分数为__________ 。
(1)请填写下表:
物质 | 摩尔质量 | 物质的量 | 质量 | 分子或离子数目 |
|
| |||
|
|
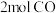 与
与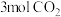 的质量之比
的质量之比(3)将含杂质软锰矿粉末
 与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得
与足量浓盐酸共热(杂质不与盐酸反应),完全反应后,制得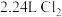 (标准状况下)。请回答下列问题:
(标准状况下)。请回答下列问题:反应中被氧化的
 的物质的量为
的物质的量为 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
2 . 氮的化合物是化学研究的热点之一,请回答下列问题:
(1)汽车尾气中的 、
、 在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出
在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出 被
被 还原的化学方程式
还原的化学方程式_______ ,并用双线桥法标出电子转移的方向和数目。
(2)氮氧化物是造成雾霾天气的主要原因之一,利用 和
和 的溶液处理氮氧化物的反应过程如下:
的溶液处理氮氧化物的反应过程如下:
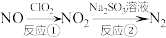
反应①的化学方程式是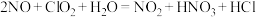 ,反应②的离子方程式是
,反应②的离子方程式是_______ ;若有1.4g 生成,需消耗
生成,需消耗
_______ g。
亚硝酸钠有咸味,有毒。已知: 。
。
(3)上述反应的还原剂为_______ (填化学式);若反应中有1分子 气体生成,则转移电子的数目为
气体生成,则转移电子的数目为_______ 。
(4)在酸性条件下,高锰酸钾可将 氧化为
氧化为 ,所得溶液中锰元素仅以
,所得溶液中锰元素仅以 形式存在,写出此反应的离子方程式:
形式存在,写出此反应的离子方程式:_______ 。
(1)汽车尾气中的
 、
、 在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出
在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出 被
被 还原的化学方程式
还原的化学方程式(2)氮氧化物是造成雾霾天气的主要原因之一,利用
 和
和 的溶液处理氮氧化物的反应过程如下:
的溶液处理氮氧化物的反应过程如下: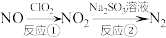
反应①的化学方程式是
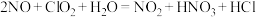 ,反应②的离子方程式是
,反应②的离子方程式是 生成,需消耗
生成,需消耗
亚硝酸钠有咸味,有毒。已知:
 。
。(3)上述反应的还原剂为
 气体生成,则转移电子的数目为
气体生成,则转移电子的数目为(4)在酸性条件下,高锰酸钾可将
 氧化为
氧化为 ,所得溶液中锰元素仅以
,所得溶液中锰元素仅以 形式存在,写出此反应的离子方程式:
形式存在,写出此反应的离子方程式:
您最近一年使用:0次
2023-10-15更新
|
235次组卷
|
2卷引用:广东北江实验学校2023—2024学年高一上学期10月月考化学试题
名校
解题方法
3 . 在空气中灼烧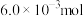 的
的 ,完全转化为
,完全转化为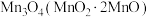 ,将其溶解于
,将其溶解于 溶有
溶有 的稀
的稀 溶液中,锰被还原为+2价。过量的
溶液中,锰被还原为+2价。过量的 需要
需要 的
的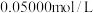 的
的 滴定,计算实验加入的
滴定,计算实验加入的 的质量(注:
的质量(注: 的相对分子质量为392)
的相对分子质量为392) _______ 。
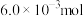 的
的 ,完全转化为
,完全转化为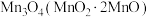 ,将其溶解于
,将其溶解于 溶有
溶有 的稀
的稀 溶液中,锰被还原为+2价。过量的
溶液中,锰被还原为+2价。过量的 需要
需要 的
的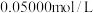 的
的 滴定,计算实验加入的
滴定,计算实验加入的 的质量(注:
的质量(注: 的相对分子质量为392)
的相对分子质量为392)
您最近一年使用:0次
解题方法
4 . 现将2.3克的金属钠投入到过量水中,完全反应,按照下列要求进行计算(可能用到的相对原子质量:H—1,O—16,Na—23)
(1)生成的氢气质量为多少?___________
(2)若最终有100克溶液,此时氢氧化钠的质量分数为多少?___________
(1)生成的氢气质量为多少?
(2)若最终有100克溶液,此时氢氧化钠的质量分数为多少?
您最近一年使用:0次
名校
5 . 完成下列问题
(1)某温度(t ℃)时水中的离子浓度图象如下图,a点离子积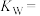
_______ ;该温度下, 的NaOH与
的NaOH与 的
的 等体积混合,溶液显
等体积混合,溶液显_______ 性。

(2)已知室温下, 的电离常数
的电离常数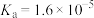 ,若初始时,醋酸中
,若初始时,醋酸中 的浓度为
的浓度为 ,则达到电离平衡时溶液中的
,则达到电离平衡时溶液中的 为
为_______ 。向其中加入少量 固体,当固体溶解后,测得溶液pH
固体,当固体溶解后,测得溶液pH_______ (填“增大”、“减小”或“不变”)。
(1)某温度(t ℃)时水中的离子浓度图象如下图,a点离子积
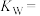
 的NaOH与
的NaOH与 的
的 等体积混合,溶液显
等体积混合,溶液显
(2)已知室温下,
 的电离常数
的电离常数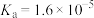 ,若初始时,醋酸中
,若初始时,醋酸中 的浓度为
的浓度为 ,则达到电离平衡时溶液中的
,则达到电离平衡时溶液中的 为
为 固体,当固体溶解后,测得溶液pH
固体,当固体溶解后,测得溶液pH
您最近一年使用:0次
解题方法
6 . 苯甲酸作为食品如香肠、蕃茄酱、芥末、其他调味剂,和黄油及其许多其他产品的防腐剂被广泛使用。苯甲酸能抑制霉菌、酵母和其他一些细菌的繁殖。苯甲酸对人体无害,其通过代谢为马尿酸被排出体外,因而不会在体内积累。越橘、野生黄莓等含有较多的苯甲酸。当pH低于5时,苯甲酸具有防腐效果。
(1)写出苯甲酸在水中的质子转移反应方程式_______ 。
(2)已知苯甲酸的Ka= 6.31 ×10-5。当苯甲酸的浓度c为0.012 mol·L-1时,计算该溶液的pH=_______ 。
(3)分别确定pH=4.00和pH=6.00的水果汁中苯甲酸离子与苯甲酸浓度的比值_______ 、_______ 。
(4)当pH=_______ 时苯甲酸溶液具有最佳的缓冲能力。
(5)将25 mL、浓度为0.0150 mol·L-1的苯甲酸溶液加到浓度为0.0120 mol·L-1的17 mL氢氧化钠溶液中,计算该混合溶液的pH=_______ 。
(1)写出苯甲酸在水中的质子转移反应方程式
(2)已知苯甲酸的Ka= 6.31 ×10-5。当苯甲酸的浓度c为0.012 mol·L-1时,计算该溶液的pH=
(3)分别确定pH=4.00和pH=6.00的水果汁中苯甲酸离子与苯甲酸浓度的比值
(4)当pH=
(5)将25 mL、浓度为0.0150 mol·L-1的苯甲酸溶液加到浓度为0.0120 mol·L-1的17 mL氢氧化钠溶液中,计算该混合溶液的pH=
您最近一年使用:0次
名校
7 . 2021年5月8日,美国化学文摘社(CAS)注册了第1.5亿个独特的化学物质-2-氨基嘧啶甲腈衍生物,新的有机化合物仍在源源不断地被发现或合成出来。有机化合物种类繁多,结构和性质都有其特点。请对下列问题按要求填空。
(1)烷烃A在同温、同压下蒸气的密度是H2的43倍,其分子式为_______ 。
(2)0.1mol炔烃B完全燃烧,消耗8.96L标准状况下的O2,其分子式为_______ 。
(3)某单烯烃与氢气加成后产物的结构简式如图,则该烯烃可能的结构有_______ 种(不考虑立体异构体)。
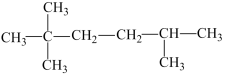
(4)某有机物的结构简式为 ,其名称是
,其名称是_______ 。
(5)已知萘分子的结构简式为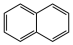 ,则它的六氯代物有
,则它的六氯代物有_______ 种。
(6)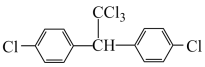 分子中最多有
分子中最多有_______ 个碳原子共面。
(1)烷烃A在同温、同压下蒸气的密度是H2的43倍,其分子式为
(2)0.1mol炔烃B完全燃烧,消耗8.96L标准状况下的O2,其分子式为
(3)某单烯烃与氢气加成后产物的结构简式如图,则该烯烃可能的结构有
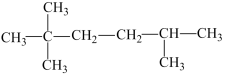
(4)某有机物的结构简式为
 ,其名称是
,其名称是(5)已知萘分子的结构简式为
 ,则它的六氯代物有
,则它的六氯代物有(6)
 分子中最多有
分子中最多有
您最近一年使用:0次
2021-07-18更新
|
975次组卷
|
2卷引用:广东省普宁市华侨中学2021-2022学年高二下学期期中考试化学试题
解题方法
8 . 计算
(1)焦炭与CO、CO2、H2均是重要的化工原料。由CO2制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-49.58 kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+41.19 kJ·mol-1
反应Ⅲ:CO(g)+2H2(g)=CH3OH(g) ΔH3
则反应Ⅲ的ΔH3=___________ 。
(2)低能耗高效率的合成氨技术开发是实现氨燃料化利用的基础。探索新型合成氨技术是研究热点之一。回答下列问题:
哈伯合成氨在较高温度下以氢气做氢源,氢气可由天然气制备。CH4(g)+H2O(g) CO(g)+3H2(g)
CO(g)+3H2(g)
下表列出了几种化学键的键能:【CO的结构 】
】
298 K时,上述反应的ΔH=___________ 。
(1)焦炭与CO、CO2、H2均是重要的化工原料。由CO2制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-49.58 kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+41.19 kJ·mol-1
反应Ⅲ:CO(g)+2H2(g)=CH3OH(g) ΔH3
则反应Ⅲ的ΔH3=
(2)低能耗高效率的合成氨技术开发是实现氨燃料化利用的基础。探索新型合成氨技术是研究热点之一。回答下列问题:
哈伯合成氨在较高温度下以氢气做氢源,氢气可由天然气制备。CH4(g)+H2O(g)
 CO(g)+3H2(g)
CO(g)+3H2(g)下表列出了几种化学键的键能:【CO的结构
 】
】| 化学键 | H-H | C-H | H-O |  |
| 键能kJ/mol | 436 | 413 | 467 | 1072 |
您最近一年使用:0次