1 . 将标准状况下 溶于
溶于 水中,计算生成的硝酸浓度
水中,计算生成的硝酸浓度_____ (忽略溶液体积的变化)。
 溶于
溶于 水中,计算生成的硝酸浓度
水中,计算生成的硝酸浓度
您最近一年使用:0次
名校
解题方法
2 . 某兴趣小组的同学模拟侯德榜制碱法制取纯碱,流程如图:

(1)向饱和NaCl溶液中通入 和氨气时,应先通入
和氨气时,应先通入___________ (填化学式)。操作①的名称为___________ 。
(2)写出反应①的化学方程式:___________ 。
(3)该流程中可循环利用的物质是___________ (填化学式)。
(4)现将 和
和 的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中
的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为___________ 。
(5)下列选项中哪种方法可以鉴别 溶液和
溶液和 溶液___________。
溶液___________。
(6)下列实验方案中,不能测定出 和
和 的混合物中
的混合物中 质量分数的是_______。
质量分数的是_______。
(7)钠是一种典型的碱金属元素,下列性质的递变规律正确,且能作为碱金属元素金属性递变规律判断依据的是___________(填字母)。

(1)向饱和NaCl溶液中通入
 和氨气时,应先通入
和氨气时,应先通入(2)写出反应①的化学方程式:
(3)该流程中可循环利用的物质是
(4)现将
 和
和 的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中
的固体均匀混合分成两等份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为(5)下列选项中哪种方法可以鉴别
 溶液和
溶液和 溶液___________。
溶液___________。| A.加入澄清石灰水 | B.加入氢氧化钠溶液 |
| C.加热 | D.逐滴加入稀盐酸 |
(6)下列实验方案中,不能测定出
 和
和 的混合物中
的混合物中 质量分数的是_______。
质量分数的是_______。| A.取ag混合物充分加热,质量减少bg |
| B.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体 |
| C.取ag混合物与足量NaOH溶液充分反应,得到bg溶液 |
| D.取ag混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加bg |
(7)钠是一种典型的碱金属元素,下列性质的递变规律正确,且能作为碱金属元素金属性递变规律判断依据的是___________(填字母)。
| A.Li、Na、K的原子半径和密度都随原子序数的增加而增大 |
B.碱性: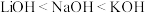 |
C.还原性: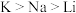 ,故K可以从NaCl溶液中置换出金属钠 ,故K可以从NaCl溶液中置换出金属钠 |
D.熔、沸点: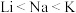 |
您最近一年使用:0次
2023-12-23更新
|
144次组卷
|
3卷引用:安徽省阜阳市第三中学2023-2024学年高一上学期1月期末化学试题
3 . 一氧化氮可用作人造丝的漂白剂及丙烯和二甲醚的安定剂。一定温度下,在2L恒容密闭容器中充入1molNO、1mol ,发生反应
,发生反应 ,起始时体系压强为aMPa,tmin时反应达到平衡,此时测得
,起始时体系压强为aMPa,tmin时反应达到平衡,此时测得 的物质的量分数为25%。
的物质的量分数为25%。
(1)平衡时,体系压强p=___________ MPa。
(2)平衡时,
___________ 。
(3)该反应平衡常数表达式为___________ ,该温度下时,平衡常数K=___________ 。
 ,发生反应
,发生反应 ,起始时体系压强为aMPa,tmin时反应达到平衡,此时测得
,起始时体系压强为aMPa,tmin时反应达到平衡,此时测得 的物质的量分数为25%。
的物质的量分数为25%。(1)平衡时,体系压强p=
(2)平衡时,

(3)该反应平衡常数表达式为
您最近一年使用:0次
名校
4 . 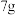 粗锌放在烧杯中,加入
粗锌放在烧杯中,加入 稀硫酸,待完全反应后(杂质与稀硫酸不反应,且不溶于水),称量,烧杯内物质总质量为
稀硫酸,待完全反应后(杂质与稀硫酸不反应,且不溶于水),称量,烧杯内物质总质量为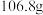 ,试计算反应后所得溶液的溶质质量分数(小数点后保留一位数字)
,试计算反应后所得溶液的溶质质量分数(小数点后保留一位数字)___________ 。
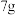 粗锌放在烧杯中,加入
粗锌放在烧杯中,加入 稀硫酸,待完全反应后(杂质与稀硫酸不反应,且不溶于水),称量,烧杯内物质总质量为
稀硫酸,待完全反应后(杂质与稀硫酸不反应,且不溶于水),称量,烧杯内物质总质量为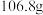 ,试计算反应后所得溶液的溶质质量分数(小数点后保留一位数字)
,试计算反应后所得溶液的溶质质量分数(小数点后保留一位数字)
您最近一年使用:0次
名校
解题方法
5 . 化学学科中由于物质种类和反应的多样性,通过类别思想和价态规律来分析物质的性质成为重要的学习思路,同时需要将定性和学科知识进行定量的计算。结合所学完成下面问题。
(1)与标准状况下5.6L 所含氧原子数目相同的水的质量是
所含氧原子数目相同的水的质量是_______ 。
(2)12.4g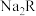 含0.4mol
含0.4mol ,则
,则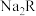 的摩尔质量为
的摩尔质量为_______ 。
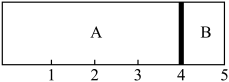
(3)某密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左侧A中充入1mol ,右侧B中充入CO和
,右侧B中充入CO和 的混合气体共8g时,隔板处于如图位置(左、右两侧温度,相同),右侧B中CO与
的混合气体共8g时,隔板处于如图位置(左、右两侧温度,相同),右侧B中CO与 分子数之比为
分子数之比为_______ 。
(4)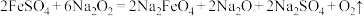 ,每生成8g氧气,反应中转移电子的物质的量为
,每生成8g氧气,反应中转移电子的物质的量为_______ 。
(5)某元素的核素 ,1.11g该核素的氯化物
,1.11g该核素的氯化物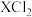 配成的溶液需用20 mL 1
配成的溶液需用20 mL 1  的
的 溶液才能把
溶液才能把 完全沉淀下来,已知此核素中质子数与中子数相等,则:
完全沉淀下来,已知此核素中质子数与中子数相等,则:
① 的质量数A是
的质量数A是_______ 。
②37g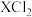 中所含质子数的物质的量为
中所含质子数的物质的量为_______ 。
(6)密闭容器中装有1mol 和0.6mol
和0.6mol  ,充分加热待完全反应后,容器内残留固体的成分为
,充分加热待完全反应后,容器内残留固体的成分为_______ 。
(1)与标准状况下5.6L
 所含氧原子数目相同的水的质量是
所含氧原子数目相同的水的质量是(2)12.4g
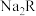 含0.4mol
含0.4mol ,则
,则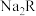 的摩尔质量为
的摩尔质量为(3)某密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左侧A中充入1mol
 ,右侧B中充入CO和
,右侧B中充入CO和 的混合气体共8g时,隔板处于如图位置(左、右两侧温度,相同),右侧B中CO与
的混合气体共8g时,隔板处于如图位置(左、右两侧温度,相同),右侧B中CO与 分子数之比为
分子数之比为
(4)
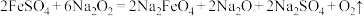 ,每生成8g氧气,反应中转移电子的物质的量为
,每生成8g氧气,反应中转移电子的物质的量为(5)某元素的核素
 ,1.11g该核素的氯化物
,1.11g该核素的氯化物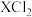 配成的溶液需用20 mL 1
配成的溶液需用20 mL 1  的
的 溶液才能把
溶液才能把 完全沉淀下来,已知此核素中质子数与中子数相等,则:
完全沉淀下来,已知此核素中质子数与中子数相等,则:①
 的质量数A是
的质量数A是②37g
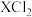 中所含质子数的物质的量为
中所含质子数的物质的量为(6)密闭容器中装有1mol
 和0.6mol
和0.6mol  ,充分加热待完全反应后,容器内残留固体的成分为
,充分加热待完全反应后,容器内残留固体的成分为
您最近一年使用:0次
名校
6 . 已知 2FeCl3+Fe=3FeCl2。在 FeCl3 溶液中加入一定量的 Fe,当反应进行到氯化铁和氯化亚铁的质量分数相等时,求此刻已参加反应的氯化铁和剩余的氯化铁的质量比_______ 。(相对分子质量 FeCl3:162.5 FeCl2:127 )
您最近一年使用:0次
解题方法
7 . I.某双原子分子构成的气体,其摩尔质量为Mg/mol,该气体的质量为mg。设阿伏加德罗常数的值为 ,则:
,则:
(1)该气体在标准状况下的体积为_______ L;
(2)该气体在标准状况下的密度为_______ g/L;
(3)该气体所含的原子总数为_______ ;
(4)一个该气体分子的质量为_______ g;
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为_______  。
。
II.实验室需要0.1mol/LNaOH溶液480mL。根据溶液的配制情况回答下列问题。
(6)由NaOH固体配制溶液,在如图所示仪器中,配制上述溶液肯定不需要的是_______ (填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是_______ 。
A. B.
B. C.
C. D.
D. E.
E.
(7)下列操作会导致所配溶液浓度偏高的是_______ (填字母)。
A.配制氢氧化钠溶液时,称量时间过长
B.转移溶液前容量瓶中存在少量蒸馏水
C.定容前未洗涤烧杯和玻璃棒
D.配制氢氧化钠溶液时,将称量好的氢氧化钠固体在小烧杯中溶解后,未冷却立即转移到容量瓶中并定容
E.定容时俯视容量瓶刻度线
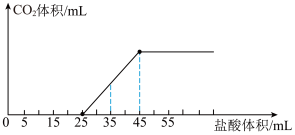
(8)取配制好的NaOH溶液100mL,然后向其通入一定量的 气体,再向所得溶液A中逐滴缓慢加入一定物质的量浓度的HCl溶液,产生的
气体,再向所得溶液A中逐滴缓慢加入一定物质的量浓度的HCl溶液,产生的 气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示。A溶液中溶质及物质的量之比为
气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示。A溶液中溶质及物质的量之比为_______ 。
 ,则:
,则:(1)该气体在标准状况下的体积为
(2)该气体在标准状况下的密度为
(3)该气体所含的原子总数为
(4)一个该气体分子的质量为
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为
 。
。II.实验室需要0.1mol/LNaOH溶液480mL。根据溶液的配制情况回答下列问题。
(6)由NaOH固体配制溶液,在如图所示仪器中,配制上述溶液肯定不需要的是
A.
 B.
B. C.
C. D.
D. E.
E.
(7)下列操作会导致所配溶液浓度偏高的是
A.配制氢氧化钠溶液时,称量时间过长
B.转移溶液前容量瓶中存在少量蒸馏水
C.定容前未洗涤烧杯和玻璃棒
D.配制氢氧化钠溶液时,将称量好的氢氧化钠固体在小烧杯中溶解后,未冷却立即转移到容量瓶中并定容
E.定容时俯视容量瓶刻度线
(8)取配制好的NaOH溶液100mL,然后向其通入一定量的
 气体,再向所得溶液A中逐滴缓慢加入一定物质的量浓度的HCl溶液,产生的
气体,再向所得溶液A中逐滴缓慢加入一定物质的量浓度的HCl溶液,产生的 气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示。A溶液中溶质及物质的量之比为
气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示。A溶液中溶质及物质的量之比为
您最近一年使用:0次
名校
解题方法
8 . 填空。
(1)CH4、CO2和碳酸都是碳的重要化合物,实现碳及其化合物的相互转化。对开发新能源和降低碳排放意义重大。
已知:①
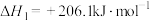
②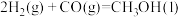
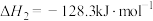
③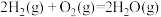
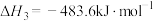
写出由甲烷和氧气合成液态甲醇的热化学方程式:_______ 。
(2)已知: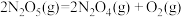
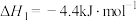
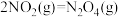
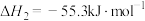
则反应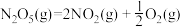 的△H=
的△H=_______ kJ∙mol-1。
(3)若将NaHSO4与Ba(OH)2在溶液中按物质的量之比为1:1混合,化学反应的离子方程式是_______ 。
(4)实验室现欲用质量分数为98%,密度为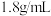 包的浓H2SO4溶液配制450 mL浓度为
包的浓H2SO4溶液配制450 mL浓度为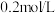 的稀H2SO4溶液,用量筒量取所需浓H2SO4溶液的体积是
的稀H2SO4溶液,用量筒量取所需浓H2SO4溶液的体积是_______ mL。
(1)CH4、CO2和碳酸都是碳的重要化合物,实现碳及其化合物的相互转化。对开发新能源和降低碳排放意义重大。
已知:①

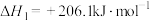
②
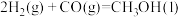
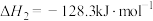
③
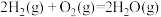
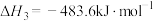
写出由甲烷和氧气合成液态甲醇的热化学方程式:
(2)已知:
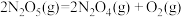
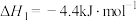
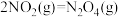
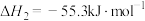
则反应
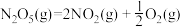 的△H=
的△H=(3)若将NaHSO4与Ba(OH)2在溶液中按物质的量之比为1:1混合,化学反应的离子方程式是
(4)实验室现欲用质量分数为98%,密度为
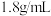 包的浓H2SO4溶液配制450 mL浓度为
包的浓H2SO4溶液配制450 mL浓度为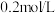 的稀H2SO4溶液,用量筒量取所需浓H2SO4溶液的体积是
的稀H2SO4溶液,用量筒量取所需浓H2SO4溶液的体积是
您最近一年使用:0次
9 . 化学计量是研究化学的重要工具。回答下列有关问题:
(1)28g氮气中含有的原子数约为_______ 个,标准状况下的体积为_______ L。
(2)7.8g 固体中含有离子的总物质的量为
固体中含有离子的总物质的量为_______ mol。
(3)在含有 、
、 、
、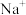 、
、 、
、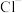 的溶液中,
的溶液中, ,若
,若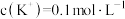 ,则
,则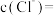
_______  。
。
(4)某气体纯净物在标准状况下的密度为1.25 ,且每个气体分子中含有两个相同原子,则该气体的名称是
,且每个气体分子中含有两个相同原子,则该气体的名称是_______ 。
(5)27g某二价金属氯化物中含有0.4mol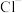 ,则该物质的化学式为
,则该物质的化学式为_______ 。
(6)标准状况下,由CO与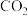 组成的混合气体密度为
组成的混合气体密度为 ,则该混合气体中
,则该混合气体中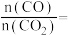
_______ (用含 的分式表示,不需要化简)。
的分式表示,不需要化简)。
(1)28g氮气中含有的原子数约为
(2)7.8g
 固体中含有离子的总物质的量为
固体中含有离子的总物质的量为(3)在含有
 、
、 、
、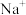 、
、 、
、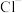 的溶液中,
的溶液中, ,若
,若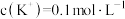 ,则
,则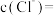
 。
。(4)某气体纯净物在标准状况下的密度为1.25
 ,且每个气体分子中含有两个相同原子,则该气体的名称是
,且每个气体分子中含有两个相同原子,则该气体的名称是(5)27g某二价金属氯化物中含有0.4mol
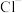 ,则该物质的化学式为
,则该物质的化学式为(6)标准状况下,由CO与
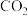 组成的混合气体密度为
组成的混合气体密度为 ,则该混合气体中
,则该混合气体中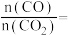
 的分式表示,不需要化简)。
的分式表示,不需要化简)。
您最近一年使用:0次
名校
解题方法
10 . 回答下列问题:
(1)某化工厂用氯气与石灰乳生产漂白粉,该厂出厂产品说明书如下:

漂白粉的主要成分是CaCl2和Ca(ClO)2,其中有效成分为Ca(ClO)2,长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式_______ ,_______ 。
(2)若用43.50g二氧化锰与足量浓盐酸(质量分数为63.50%)完全反应,制取氯气。求:
①所得气体的质量为_______ 。
②若将所得气体全部用石灰乳吸收,所制得的漂白粉中所含有效成分的质量为_______ 。
(已知MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O ,本题要求写出计算步骤,答案保留2位小数)
MnCl2+Cl2↑+2H2O ,本题要求写出计算步骤,答案保留2位小数)
(1)某化工厂用氯气与石灰乳生产漂白粉,该厂出厂产品说明书如下:

漂白粉的主要成分是CaCl2和Ca(ClO)2,其中有效成分为Ca(ClO)2,长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式
(2)若用43.50g二氧化锰与足量浓盐酸(质量分数为63.50%)完全反应,制取氯气。求:
①所得气体的质量为
②若将所得气体全部用石灰乳吸收,所制得的漂白粉中所含有效成分的质量为
(已知MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O ,本题要求写出计算步骤,答案保留2位小数)
MnCl2+Cl2↑+2H2O ,本题要求写出计算步骤,答案保留2位小数)
您最近一年使用:0次



