名校
解题方法
1 . 某实验小组用氯酸钾和二氧化锰为原料制取氧气,在试管中加入少量二氧化锰和适量氯酸钾,反应过程中测量的有关数据记录如下:
(1)反应到___________ min时,氯酸钾就完全分解。
(2)计算反应前氯酸钾的质量是多少?__________ (写出解题步骤)
| 反应时间(min) | 0 | 1 | 2 | 3 | 4 |
| 试管中固体质量(g) | 14.25 | 12.65 | 11.05 | 9.45 | 9.45 |
(2)计算反应前氯酸钾的质量是多少?
您最近一年使用:0次
2 . 硫氧粉(Na2SO3)可用作染漂脱氧剂,常因氧化变质生成Na2SO4。向18.4 g可能被氧化的样品中,加入质量分数为10%的稀硫酸至恰好不再产生气泡(假设气体全部逸出),消耗稀硫酸98 g。
已知: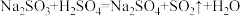 。
。
(1)三种钠盐:①Na2SO4、②Na2SO3、③Na2S2O3,其中含钠量由大到小的顺序是_______ (填序号)。
(2)求反应后溶液中溶质的质量分数(结果精确到0.1%)_______ 。(写出计算过程)
已知:
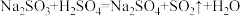 。
。(1)三种钠盐:①Na2SO4、②Na2SO3、③Na2S2O3,其中含钠量由大到小的顺序是
(2)求反应后溶液中溶质的质量分数(结果精确到0.1%)
您最近一年使用:0次
名校
3 . 向100mL含 、
、 、HCl的溶液中滴加一定浓度的NaOH溶液至过量,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。
、HCl的溶液中滴加一定浓度的NaOH溶液至过量,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。___________ ;
(2)依据表格中信息,计算滴加氢氧化钠溶液的物质的量浓度为___________ :(保留一位小数)
(3)原溶液中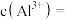
___________ ,
___________ ;
(4)将最终生成的沉淀过滤、洗涤、干燥后,放入坩埚中灼烧,得到的固体质量为4.9克。若灼烧后的固体为 ,则x的值为多少?
,则x的值为多少?___________ (无计算过程不给分)。
 、
、 、HCl的溶液中滴加一定浓度的NaOH溶液至过量,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。
、HCl的溶液中滴加一定浓度的NaOH溶液至过量,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。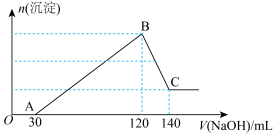
(2)依据表格中信息,计算滴加氢氧化钠溶液的物质的量浓度为
| 分子式:NaOH 相对分子质量:40 密度:  NaOH的质量分数:16.7% |
(3)原溶液中
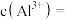

(4)将最终生成的沉淀过滤、洗涤、干燥后,放入坩埚中灼烧,得到的固体质量为4.9克。若灼烧后的固体为
 ,则x的值为多少?
,则x的值为多少?
您最近一年使用:0次
4 . t ℃时,将2mol A 和 6 mol B 充入容积固定为 2 L 的密闭容器中发生反应: A(g)+2B(g)  2C(g)。 反应 2 min 时测得 C 的浓度为 0.4 mol·L- 1 ,4 min 末反应达到平衡, B 的转化率为 50%。试计算:
2C(g)。 反应 2 min 时测得 C 的浓度为 0.4 mol·L- 1 ,4 min 末反应达到平衡, B 的转化率为 50%。试计算:
(1)第 2 min 到第 4 min 内 A 的平均反应速率为_______
(2)t ℃时该反应的平衡常数为_______
(3)若从反应开始到建立平衡时放出热量 353.88 kJ,则该反应的 ΔH=_______ 。(写出三个题 完整计算过程,无计算过程不给分)
 2C(g)。 反应 2 min 时测得 C 的浓度为 0.4 mol·L- 1 ,4 min 末反应达到平衡, B 的转化率为 50%。试计算:
2C(g)。 反应 2 min 时测得 C 的浓度为 0.4 mol·L- 1 ,4 min 末反应达到平衡, B 的转化率为 50%。试计算:(1)第 2 min 到第 4 min 内 A 的平均反应速率为
(2)t ℃时该反应的平衡常数为
(3)若从反应开始到建立平衡时放出热量 353.88 kJ,则该反应的 ΔH=
您最近一年使用:0次
名校
5 . 太空很神秘,水的世界也深不可测,从水作溶剂、水分子运动到水的电离、水与活泼金属反应等等。结合书本知识,回答下列问题:
(1)标准状况下, 的
的 溶液的
溶液的
_______ (填“>”“<”或“=”,下同)12,该温度下,水的离子积常数
_______ 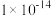 。
。
(2)某温度下,纯水中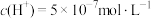 ,则此时纯水中的
,则此时纯水中的
_______  ;若温度不变,滴入稀硫酸使
;若温度不变,滴入稀硫酸使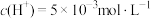 ,则
,则
_______  。
。
(3)T℃下,水的离子积曲线如图所示。_______ (填字母)。
a.T℃小于
b.A点溶液
c.B点溶液呈碱性
d.保持温度不变,加入少量的酸可以实现从B点到C点的变化
②该温度下,将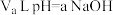 溶液与
溶液与 硫酸混合。
硫酸混合。
若所得混合溶液呈中性,且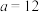 ,
, ,则
,则
_______ ;若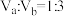 ,且
,且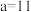 ,
,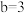 ,则所得混合溶液的
,则所得混合溶液的
_______ 。
(1)标准状况下,
 的
的 溶液的
溶液的

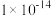 。
。(2)某温度下,纯水中
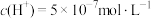 ,则此时纯水中的
,则此时纯水中的
 ;若温度不变,滴入稀硫酸使
;若温度不变,滴入稀硫酸使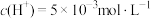 ,则
,则
 。
。(3)T℃下,水的离子积曲线如图所示。

a.T℃小于

b.A点溶液

c.B点溶液呈碱性
d.保持温度不变,加入少量的酸可以实现从B点到C点的变化
②该温度下,将
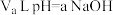 溶液与
溶液与 硫酸混合。
硫酸混合。若所得混合溶液呈中性,且
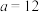 ,
, ,则
,则
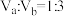 ,且
,且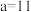 ,
,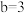 ,则所得混合溶液的
,则所得混合溶液的
您最近一年使用:0次
2022-12-16更新
|
318次组卷
|
2卷引用:四川省成都市石室中学2023-2024学年高一下学期竞赛班期末考试化学试题
名校
解题方法
6 . 回答下列问题:
(1)常温下,将pH=9的NaOH溶液稀释1000倍,溶液中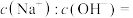
______
(2)常温下,已知醋酸的电离常数为Ka,向100mL0.1mol/L的醋酸溶液中,加入______ mL0.1mol/L的NaOH,可使反应所得的溶液pH=7(用含Ka的式子表达)
(3)常温下,100mLpH=0盐酸和硫酸的混合溶液中加入200mLpH=13的 ,恰好沉淀完全,则原溶液中c(HCl)=
,恰好沉淀完全,则原溶液中c(HCl)=______
(4)常温下,设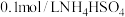 溶液的pH为a,则
溶液的pH为a,则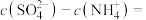
______ (用含a的精确式子表达)
(1)常温下,将pH=9的NaOH溶液稀释1000倍,溶液中
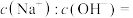
(2)常温下,已知醋酸的电离常数为Ka,向100mL0.1mol/L的醋酸溶液中,加入
(3)常温下,100mLpH=0盐酸和硫酸的混合溶液中加入200mLpH=13的
 ,恰好沉淀完全,则原溶液中c(HCl)=
,恰好沉淀完全,则原溶液中c(HCl)=(4)常温下,设
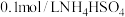 溶液的pH为a,则
溶液的pH为a,则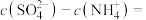
您最近一年使用:0次
7 . 回答下列问题
(1)1.5molH2SO4的质量是_______ ,其中含有_______ molH,含有_______ g氧。
(2)4.4gCO2的物质的量是_______ ,其中含有二氧化碳分子_______ 个,电子_______ 个,它在标况下占有的体积为_______ 。
(3)等质量的HCl、NH3、CO2、O2四种气体,在相同温度和相同压强条件下,体积最大的是_______ 。
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ 。
(5)实验室需要0.1mol/L的氢氧化钠溶液100mL,其中需要2mol/L的氢氧化钠溶液_______ mL,将71 g Na2SO4溶于水配成1 L溶液,该溶液中Na2 SO4的物质的量浓度为_______ ,溶液中Na+的物质的量浓度为_______
(1)1.5molH2SO4的质量是
(2)4.4gCO2的物质的量是
(3)等质量的HCl、NH3、CO2、O2四种气体,在相同温度和相同压强条件下,体积最大的是
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
(5)实验室需要0.1mol/L的氢氧化钠溶液100mL,其中需要2mol/L的氢氧化钠溶液
您最近一年使用:0次
8 . 计算
(1)3.01×1023个H2O的物质的量为_______ mol,其中,所含原子的物质的量为_______ mol,所含电子的物质的量为_______ mol。
(2)_______ g H2O中的氧原子数目与标准状况下22.4 LCO2中的氧原子数目相同。
(3)2g NaOH溶于水配制成_______ mL溶液时其物质的量浓度为2mol/L。
(4)在相同的条件下,等质量的N2、CO2、NH3的体积由大到小的顺序为_______ ,在相同条件下,等体积的N2、CO2、NH3的质量由大到小的顺序为_______ ,在相同条件下,等体积的N2、CO2、NH3密度由大到小的顺序为_______ 。
(5)某硫酸铝溶液中所含铝离子浓度为3mol/L,则硫酸根离子浓度为_______
(6)电解1.8 g H2O所得的H2在标准状况下的体积为_______
(1)3.01×1023个H2O的物质的量为
(2)
(3)2g NaOH溶于水配制成
(4)在相同的条件下,等质量的N2、CO2、NH3的体积由大到小的顺序为
(5)某硫酸铝溶液中所含铝离子浓度为3mol/L,则硫酸根离子浓度为
(6)电解1.8 g H2O所得的H2在标准状况下的体积为
您最近一年使用:0次
解题方法
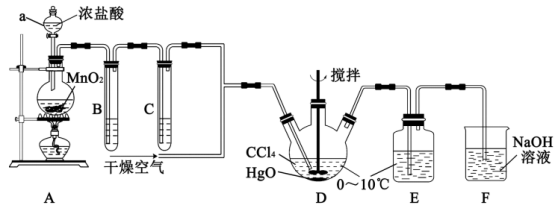
9 . 次氯酸 具有强氧化性,能起到杀菌消毒的作用。实验室制备
具有强氧化性,能起到杀菌消毒的作用。实验室制备 的反应原理为
的反应原理为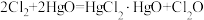 ,其制备装置如图所示,E中得到次氯酸
,其制备装置如图所示,E中得到次氯酸 。回答下列问题:
。回答下列问题:
已知:① 气体
气体 时可分解,且可与水反应生成
时可分解,且可与水反应生成 ;
;
②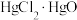 是难溶于水的固体。
是难溶于水的固体。
(1)仪器a的名称是___________ 。写出装置A中反应的离子方程式___________ 。
(2)装置B的作用是___________ ,装置C中盛装的试剂是___________ 。
(3)D中通入 与
与 反应制得
反应制得 ,则E中生成
,则E中生成 的化学反应方程式为
的化学反应方程式为___________ 。
(4)有效含氯量常用来衡量消毒剂的消毒能力,用 标准溶液滴定法测定某市售含氯消毒片的有效氯含量,实验步骤如下:
标准溶液滴定法测定某市售含氯消毒片的有效氯含量,实验步骤如下:
①称取含氯消毒片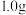 ,用容量瓶配制成
,用容量瓶配制成 溶液,定容时,用
溶液,定容时,用___________ 加蒸馏水至刻度线;
②配置 溶液及浓度标定:称取
溶液及浓度标定:称取 晶体
晶体 于烧杯中,取
于烧杯中,取 蒸馏水溶解均匀,转入
蒸馏水溶解均匀,转入___________ 色试剂瓶中,置于暗处放置7~14天后,用酸性 标准溶液标定上述
标准溶液标定上述 溶液的浓度为
溶液的浓度为 ;
;
③用滴定管量取 待测消毒溶液,置于
待测消毒溶液,置于 碘量瓶中,加入
碘量瓶中,加入 的硫酸
的硫酸 ,10%碘化钾溶液
,10%碘化钾溶液 ,此时溶液出现棕色,用
,此时溶液出现棕色,用 溶液滴定游离碘,边滴边摇匀,待溶液呈浅棕黄色时,加入1~2滴10%淀粉指示剂,继续滴定至
溶液滴定游离碘,边滴边摇匀,待溶液呈浅棕黄色时,加入1~2滴10%淀粉指示剂,继续滴定至___________ 即为终点。记录消耗的 溶液的体积;
溶液的体积;
④重复上述操作三次。四次测定的数据如下表:
根据 溶液的用量,计算消毒片的有效氯含量,已知
溶液的用量,计算消毒片的有效氯含量,已知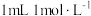 的硫代硫酸钠相当于
的硫代硫酸钠相当于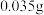 有效氯,则该市售含氯消毒片的有效氯含量为
有效氯,则该市售含氯消毒片的有效氯含量为___________ %。
 具有强氧化性,能起到杀菌消毒的作用。实验室制备
具有强氧化性,能起到杀菌消毒的作用。实验室制备 的反应原理为
的反应原理为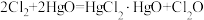 ,其制备装置如图所示,E中得到次氯酸
,其制备装置如图所示,E中得到次氯酸 。回答下列问题:
。回答下列问题:
已知:①
 气体
气体 时可分解,且可与水反应生成
时可分解,且可与水反应生成 ;
;②
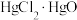 是难溶于水的固体。
是难溶于水的固体。(1)仪器a的名称是
(2)装置B的作用是
(3)D中通入
 与
与 反应制得
反应制得 ,则E中生成
,则E中生成 的化学反应方程式为
的化学反应方程式为(4)有效含氯量常用来衡量消毒剂的消毒能力,用
 标准溶液滴定法测定某市售含氯消毒片的有效氯含量,实验步骤如下:
标准溶液滴定法测定某市售含氯消毒片的有效氯含量,实验步骤如下:①称取含氯消毒片
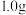 ,用容量瓶配制成
,用容量瓶配制成 溶液,定容时,用
溶液,定容时,用②配置
 溶液及浓度标定:称取
溶液及浓度标定:称取 晶体
晶体 于烧杯中,取
于烧杯中,取 蒸馏水溶解均匀,转入
蒸馏水溶解均匀,转入 标准溶液标定上述
标准溶液标定上述 溶液的浓度为
溶液的浓度为 ;
;③用滴定管量取
 待测消毒溶液,置于
待测消毒溶液,置于 碘量瓶中,加入
碘量瓶中,加入 的硫酸
的硫酸 ,10%碘化钾溶液
,10%碘化钾溶液 ,此时溶液出现棕色,用
,此时溶液出现棕色,用 溶液滴定游离碘,边滴边摇匀,待溶液呈浅棕黄色时,加入1~2滴10%淀粉指示剂,继续滴定至
溶液滴定游离碘,边滴边摇匀,待溶液呈浅棕黄色时,加入1~2滴10%淀粉指示剂,继续滴定至 溶液的体积;
溶液的体积;④重复上述操作三次。四次测定的数据如下表:
| 实验序号 | 1 | 2 | 3 | 4 |
消耗 溶液的体积/ 溶液的体积/ | 20.05 | 20.00 | 19.95 | 20.45 |
 溶液的用量,计算消毒片的有效氯含量,已知
溶液的用量,计算消毒片的有效氯含量,已知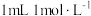 的硫代硫酸钠相当于
的硫代硫酸钠相当于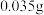 有效氯,则该市售含氯消毒片的有效氯含量为
有效氯,则该市售含氯消毒片的有效氯含量为
您最近一年使用:0次
名校
解题方法
10 . 回答下列问题:
(1)3.6gH2O的物质的量是_______ ,含有氢原子的数目是_______ 。
(2)1.5molCO2和_______ gCH4在标准状况下占有相同的体积,其体积为_______ 。
(3)100mL气体A2跟50mL气体B2恰好完全反应生成100mL气体C(体积均在相同条件下测定)则C的化学式为_______ 。
(4)标准状况下,一烧瓶HCl气体倒扣在水槽中,假设溶液没有损失,则所得溶液的物质的量浓度为_______ 。
(5)将4gNaOH溶解在10mL水中,再稀释成1L,从中取出10mL,这10mL溶液的物质的量浓度为_______ 。
(1)3.6gH2O的物质的量是
(2)1.5molCO2和
(3)100mL气体A2跟50mL气体B2恰好完全反应生成100mL气体C(体积均在相同条件下测定)则C的化学式为
(4)标准状况下,一烧瓶HCl气体倒扣在水槽中,假设溶液没有损失,则所得溶液的物质的量浓度为
(5)将4gNaOH溶解在10mL水中,再稀释成1L,从中取出10mL,这10mL溶液的物质的量浓度为
您最近一年使用:0次



