名校
1 . 某实验小组对草酸亚铁晶体(FeC2O4∙xH2O)进行热分解研究时,按下图装置将草酸亚铁晶体样品加热,使其完全分解,对所得气体产物进行探究(装置中各试剂均足量)。_______ 之间(填字母)。
(2)装置E中试剂可以是_______ (填名称)。
(3)若利用上述装置所得数据进行定量分析,存在的明显缺陷是_______ 。
(4)文献显示,FeC2O4∙xH2O受热分解时,固体的质量随温度变化的曲线如下图所示:_______ 。
②从300℃到400℃,隔绝空气加热固体时,发生反应的化学方程式:_______ 。
③从400℃到500℃,在敞口环境中充分加热,C处得到的固体质量为_______ 。
④500℃后,固体质量减小是因为有氧气生成,试写出反应的化学方程式:_______ 。
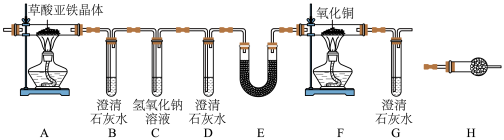
(2)装置E中试剂可以是
(3)若利用上述装置所得数据进行定量分析,存在的明显缺陷是
(4)文献显示,FeC2O4∙xH2O受热分解时,固体的质量随温度变化的曲线如下图所示:

②从300℃到400℃,隔绝空气加热固体时,发生反应的化学方程式:
③从400℃到500℃,在敞口环境中充分加热,C处得到的固体质量为
④500℃后,固体质量减小是因为有氧气生成,试写出反应的化学方程式:
您最近半年使用:0次
名校
解题方法
2 . 现有铁及其氧化物粉末7.04g,加入100mL1 的稀硫酸恰好完全溶解,并收集到标准状况下气体224mL。向反应后的溶液中滴加KSCN溶液,无明显变化。若将等质量的该混合物在高温下与足量的CO充分反应,生成CO2的质量为
的稀硫酸恰好完全溶解,并收集到标准状况下气体224mL。向反应后的溶液中滴加KSCN溶液,无明显变化。若将等质量的该混合物在高温下与足量的CO充分反应,生成CO2的质量为
 的稀硫酸恰好完全溶解,并收集到标准状况下气体224mL。向反应后的溶液中滴加KSCN溶液,无明显变化。若将等质量的该混合物在高温下与足量的CO充分反应,生成CO2的质量为
的稀硫酸恰好完全溶解,并收集到标准状况下气体224mL。向反应后的溶液中滴加KSCN溶液,无明显变化。若将等质量的该混合物在高温下与足量的CO充分反应,生成CO2的质量为| A.1.65g | B.2.20g | C.3.96g | D.4.40g |
您最近半年使用:0次
名校
解题方法
3 . A常温常压下为无色液体,B、C是无色无味的气体,M、R是两种常见的金属,且M是地壳中含量最多的金属元素的单质,T是淡黄色固体,E是具有磁性的黑色晶体,G和H组成元素相同。各物质在一定条件下有如下转化关系。
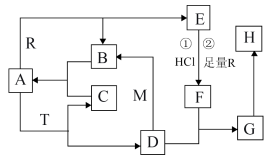
(1)物质T的电子式为____________ 。16.8g R与足量的A反应生成E和B转移的电子数目为___________ (用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(2)D和M在溶液中反应生成B的离子反应方程式为___________________________ 。
(3)G向H转化的实验现象为________________________ 。
(4)T和F反应只生成C、H和一种盐,其化学反应方程式为__________________ 。
(5)若向E和R的混合物中加入100mL 1mol/L的盐酸,恰好使混合物完全溶解,生成 并放出448mL(标准状况)气体。若用足量的CO在高温下还原相同质量的上述混合物,得到的固体质量为
并放出448mL(标准状况)气体。若用足量的CO在高温下还原相同质量的上述混合物,得到的固体质量为____________ g。

(1)物质T的电子式为
 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(2)D和M在溶液中反应生成B的离子反应方程式为
(3)G向H转化的实验现象为
(4)T和F反应只生成C、H和一种盐,其化学反应方程式为
(5)若向E和R的混合物中加入100mL 1mol/L的盐酸,恰好使混合物完全溶解,生成
 并放出448mL(标准状况)气体。若用足量的CO在高温下还原相同质量的上述混合物,得到的固体质量为
并放出448mL(标准状况)气体。若用足量的CO在高温下还原相同质量的上述混合物,得到的固体质量为
您最近半年使用:0次
解题方法
4 . 化学研究源于实验与理论的结合,得益于科学的推断与探究。
(1)一个体重50kg的健康人含铁2g,这2g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
①服用维生素C,可使食物中的铁离子转化成亚铁离子,有利于铁的吸收,以下为常见铁元素的几种微粒,其中既有氧化性又有还原性的是______ 。
A.Fe B.Fe2+ C.Fe3+
②工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是将人体内的Fe2+转化为Fe3+而失去了与O2结合的能力,这说明NaNO2具有______ 性。
③工业盐中毒后,可服用维生素C来缓解中毒症状,这说明维生素C具有______ 性。
(2)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。脱氧中的一步主要反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,该脱氧反应中还原剂是______ 。
(3)某化学兴趣小组用食品脱氧剂(2g铁粉、0.5g活性炭、0.5g氯化钠)进行如图两个实验。
实验I:
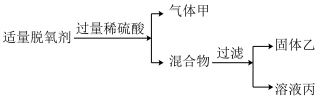
请回答:
①溶液丙中一定含有的金属阳离子是______ (写离子符号)。
②检验溶液丙中Cl-的方案是______ 。
③实验Ⅱ:将乙烘干后进行如图实验,物质之间的转化关系如图(部分产物省略)
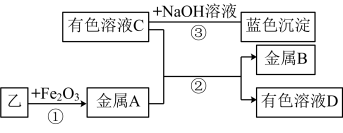
写出②的离子方程式______ ,若反应消耗16.8g金属A,转移电子的数目为______ 。(阿伏加德罗常数用NA表示)
(4)在铁的氧化物和氧化铝组成的混合物中加入2mol/L硫酸62.5mL,恰好完全反应,所得溶液Fe2+能被标准状况下224mL氯气氧化。则原混合物中金属元素和氧元素的原子个数之比为______ 。
(1)一个体重50kg的健康人含铁2g,这2g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
①服用维生素C,可使食物中的铁离子转化成亚铁离子,有利于铁的吸收,以下为常见铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
②工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是将人体内的Fe2+转化为Fe3+而失去了与O2结合的能力,这说明NaNO2具有
③工业盐中毒后,可服用维生素C来缓解中毒症状,这说明维生素C具有
(2)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。脱氧中的一步主要反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,该脱氧反应中还原剂是
(3)某化学兴趣小组用食品脱氧剂(2g铁粉、0.5g活性炭、0.5g氯化钠)进行如图两个实验。
实验I:

请回答:
①溶液丙中一定含有的金属阳离子是
②检验溶液丙中Cl-的方案是
③实验Ⅱ:将乙烘干后进行如图实验,物质之间的转化关系如图(部分产物省略)

写出②的离子方程式
(4)在铁的氧化物和氧化铝组成的混合物中加入2mol/L硫酸62.5mL,恰好完全反应,所得溶液Fe2+能被标准状况下224mL氯气氧化。则原混合物中金属元素和氧元素的原子个数之比为
您最近半年使用:0次
5 . 混合物M由铁和氧化铜组成。取一定质量的M粉末放入足量稀硫酸中,充分反应后产生0.6g气体,并得到6.4g残留固体。则取用的M粉末质量为
| A.24.8g | B.30.4g | C.36.0g | D.51.6g |
您最近半年使用:0次
6 . 现有一包由5.6g铁、7.2g镁、1.5g碳混合而成的粉末,把它加入一定量的 溶液中。实验结束后,测得剩余固体中含有三种物质,则剩余固体的质量可能是
溶液中。实验结束后,测得剩余固体中含有三种物质,则剩余固体的质量可能是
 溶液中。实验结束后,测得剩余固体中含有三种物质,则剩余固体的质量可能是
溶液中。实验结束后,测得剩余固体中含有三种物质,则剩余固体的质量可能是| A.24.8g | B.25.8g | C.26.8g | D.27.8g |
您最近半年使用:0次
解题方法
7 . “孤蓬自振”学习小组向一定质量的Fe、FeO、Fe2O3的混合物中,加入100mL1.0mol/L的盐酸,恰好使混合物完全溶解并放出约224mL(标准状况)气体,溶液体积仍为100mL,所得溶液中滴加几滴KSCN溶液,溶液未显红色。请回答:
(1)加盐酸后所得溶液的溶质是______ (填化学式),物质的量浓度是______ mol/L。
(2)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量是______ g。
(3)该混合物中铁、氧两种元素的粒子个数比N(Fe):N(O)=______ 。
(1)加盐酸后所得溶液的溶质是
(2)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量是
(3)该混合物中铁、氧两种元素的粒子个数比N(Fe):N(O)=
您最近半年使用:0次
8 . 在一定量铁的氧化物 (铁只有+2、+3价)中,加入100mL
(铁只有+2、+3价)中,加入100mL  稀盐酸,恰好使固体完全溶解,再向所得溶液中通入标准状况下280mL氯气,恰好能使溶液中
稀盐酸,恰好使固体完全溶解,再向所得溶液中通入标准状况下280mL氯气,恰好能使溶液中 完全转化为
完全转化为 (发生的反应为
(发生的反应为 ),则
),则 为
为
 (铁只有+2、+3价)中,加入100mL
(铁只有+2、+3价)中,加入100mL  稀盐酸,恰好使固体完全溶解,再向所得溶液中通入标准状况下280mL氯气,恰好能使溶液中
稀盐酸,恰好使固体完全溶解,再向所得溶液中通入标准状况下280mL氯气,恰好能使溶液中 完全转化为
完全转化为 (发生的反应为
(发生的反应为 ),则
),则 为
为| A.1:1 | B.2:3 | C.3:4 | D.4:5 |
您最近半年使用:0次
名校
解题方法
9 . 现有m g由Fe、FeO、Fe2O3和Fe3O4组成的固体混合物,将该固体混合物全部加入VLcmol⋅L-1稀硫酸中,固体恰好完全溶解,且所得的溶液中仅含有一种溶质。若等质量的上述固体混合物用H2充分还原,则所得到的铁的质量为
| A.56cVg | B.(m﹣16)g | C. | D.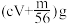 |
您最近半年使用:0次
10 . 将一定量的Fe、 、CuO的混合物放入100mL
、CuO的混合物放入100mL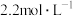 的
的 溶液中,充分反应后生成896ml。气体(标准状况下),得到不溶固体1.28g,过滤后,滤液中的金属离子只有
溶液中,充分反应后生成896ml。气体(标准状况下),得到不溶固体1.28g,过滤后,滤液中的金属离子只有 (假设滤液体积仍为100mL)。向滤液中滴加
(假设滤液体积仍为100mL)。向滤液中滴加 NaOH溶液,直至40mL时开始出现沉淀。下列说法错误的是
NaOH溶液,直至40mL时开始出现沉淀。下列说法错误的是
 、CuO的混合物放入100mL
、CuO的混合物放入100mL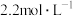 的
的 溶液中,充分反应后生成896ml。气体(标准状况下),得到不溶固体1.28g,过滤后,滤液中的金属离子只有
溶液中,充分反应后生成896ml。气体(标准状况下),得到不溶固体1.28g,过滤后,滤液中的金属离子只有 (假设滤液体积仍为100mL)。向滤液中滴加
(假设滤液体积仍为100mL)。向滤液中滴加 NaOH溶液,直至40mL时开始出现沉淀。下列说法错误的是
NaOH溶液,直至40mL时开始出现沉淀。下列说法错误的是| A.CuO的质量为1.6g |
B.未滴加NaOH溶液前滤液中 的物质的量浓度为 的物质的量浓度为 |
C.溶液中 和 和 消耗铁的物质的量之比为2:1 消耗铁的物质的量之比为2:1 |
| D.Fe在溶液中共参与了三个反应 |
您最近半年使用:0次



