名校
解题方法
1 . 二氧化碲( )是一种性能优良的声光晶体材料,一种以铜碲渣(主要成分为
)是一种性能优良的声光晶体材料,一种以铜碲渣(主要成分为 ,还含有少量
,还含有少量 、
、 )为原料制备
)为原料制备 并获得海绵铜的工艺流程如图所示。
并获得海绵铜的工艺流程如图所示。 是不溶于水的固体;碱浸液的主要成分为
是不溶于水的固体;碱浸液的主要成分为 和
和 。
。
请回答下列问题:
(1)浸渣 的主要成分为
的主要成分为______ (填化学式)。
(2)“氧化酸浸”时,为了加快反应速率,除将铜碲渣粉碎外,还可以采取的措施为______ (写一种即可);配平该过程中发生反应的离子方程式_______ :
______ +______
+______ +______
+______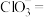 ______
______ +______
+______ +______
+______ +______
+______
若用稀硝酸代替 ,不足之处可能是
,不足之处可能是______ 。
(3)“净化中和”时, 转化为
转化为 反应的化学方程式为
反应的化学方程式为______ ;“过滤”弃去中和废液后,须洗涤沉淀,洗涤的操作为______ 。
(4)工业上制备的海绵铜中含有杂质 和
和 ,可以用______除去海绵铜中的杂质(填标号)。
,可以用______除去海绵铜中的杂质(填标号)。
 )是一种性能优良的声光晶体材料,一种以铜碲渣(主要成分为
)是一种性能优良的声光晶体材料,一种以铜碲渣(主要成分为 ,还含有少量
,还含有少量 、
、 )为原料制备
)为原料制备 并获得海绵铜的工艺流程如图所示。
并获得海绵铜的工艺流程如图所示。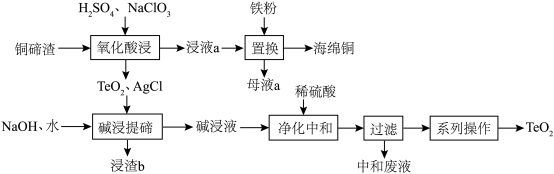
 是不溶于水的固体;碱浸液的主要成分为
是不溶于水的固体;碱浸液的主要成分为 和
和 。
。请回答下列问题:
(1)浸渣
 的主要成分为
的主要成分为(2)“氧化酸浸”时,为了加快反应速率,除将铜碲渣粉碎外,还可以采取的措施为
______
 +______
+______ +______
+______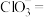 ______
______ +______
+______ +______
+______ +______
+______
若用稀硝酸代替
 ,不足之处可能是
,不足之处可能是(3)“净化中和”时,
 转化为
转化为 反应的化学方程式为
反应的化学方程式为(4)工业上制备的海绵铜中含有杂质
 和
和 ,可以用______除去海绵铜中的杂质(填标号)。
,可以用______除去海绵铜中的杂质(填标号)。| A.稀硝酸 | B.稀盐酸 | C. 溶液 溶液 | D. 溶液 溶液 |
您最近半年使用:0次
2 . 加碘食盐中的碘以碘酸钾 的形式存在。已知在溶液中
的形式存在。已知在溶液中 与
与 可发生反应:
可发生反应: ,根据上述反应,可用试纸和一些常见试剂进行实验,证明食盐中存在
,根据上述反应,可用试纸和一些常见试剂进行实验,证明食盐中存在 。可供选用的物质有:①蒸馏水②蓝色石蕊试纸③碘化钾淀粉试纸④淀粉⑤蔗糖⑥白醋(主要成分醋酸
。可供选用的物质有:①蒸馏水②蓝色石蕊试纸③碘化钾淀粉试纸④淀粉⑤蔗糖⑥白醋(主要成分醋酸 )⑦乙醇
)⑦乙醇
进行上述实验时必须使用的物质是___________ (填编号)。
 的形式存在。已知在溶液中
的形式存在。已知在溶液中 与
与 可发生反应:
可发生反应: ,根据上述反应,可用试纸和一些常见试剂进行实验,证明食盐中存在
,根据上述反应,可用试纸和一些常见试剂进行实验,证明食盐中存在 。可供选用的物质有:①蒸馏水②蓝色石蕊试纸③碘化钾淀粉试纸④淀粉⑤蔗糖⑥白醋(主要成分醋酸
。可供选用的物质有:①蒸馏水②蓝色石蕊试纸③碘化钾淀粉试纸④淀粉⑤蔗糖⑥白醋(主要成分醋酸 )⑦乙醇
)⑦乙醇进行上述实验时必须使用的物质是
您最近半年使用:0次
名校
3 . 化学与生产生活密切相关,下列应用中没有涉及到氧化还原反应的是
| A.化学烫发时头发中的蛋白质发生化学反应 | B.维生素C用作水果罐头的抗氧化剂 |
| C.使用含氟牙膏预防龋齿 | D.由烷烃通过气相沉积法制备宝石级钻石 |
您最近半年使用:0次
4 . 化学与生活密切相关,下列描述合理的是
| A.纯碱可用于治疗胃酸过多 |
| B.ClO2、O3能够杀死水体中的细菌,从而起到消毒作用 |
| C.利用维生素C的氧化性将Fe3+转化为易被人体吸收的Fe2+ |
| D.漂白粉可用于食品漂白 |
您最近半年使用:0次
名校
解题方法
5 . 化学创造美好生活。下列生产活动与对应化学原理解释不正确的是
| 选项 | 生产活动 | 化学原理 |
| A | 用氢氧化铝治疗胃酸过多 | 氢氧化铝有弱碱性 |
| B | 用ClO2作饮用水杀菌消毒剂 | ClO2具有强氧化性 |
| C | 凡酸坏之酒,皆可蒸烧 | 物质的溶解性不同 |
| D | 用Fe3O4作录音磁带 | Fe3O4具有磁性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
6 . 新冠病毒使人意识到学习化学的重要性。75%酒精、含氯消毒剂、过氧乙酸、苯酚等均能有效灭杀该病毒。下列说法不正确的是
| A.外出返家,可用75%的酒精对手、衣服等部位进行消毒 |
| B.为增强“84”消毒液的消毒效果,可加入稀盐酸 |
| C.过氧乙酸灭活新冠肺炎病毒是利用其氧化性 |
| D.药皂中掺有少量硫,使其具有杀菌的作用 |
您最近半年使用:0次
7 . 浩瀚的海洋中蕴藏着丰富的资源,其中海水提溴工艺流程如下所示:不正确 的是
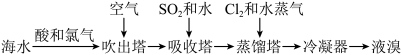
| A.吹出塔中利用了溴单质的挥发性将溴分离出来 |
| B.吸收塔中Br2与SO2发生反应以达到富集目的 |
| C.蒸馏塔中利用物质沸点不同进行分离 |
| D.吸收时可用Fe2(SO4)3溶液代替SO2和水 |
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
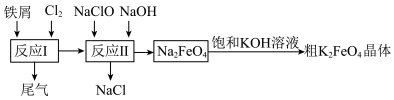
8 . 高铁酸钾(K2FeO4)有强氧化性,是一种环保、高效、多功能饮用水处理剂,受热易分解,酸性环境中易变质。制备流程如图所示:
(1)K2FeO4中铁的化合价为______ ,提纯K2FeO4的实验方法是______ 。
(2)铁屑需事先用Na2CO3溶液洗涤,目的是______ 。
(3)K2FeO4处理饮用水的原理是______ 。
(4)已知K2FeO4难溶于乙醇,可溶于水,故洗涤K2FeO4晶体时,先使用冷水洗涤,再使用乙醇洗涤,简述用乙醇洗涤K2FeO4晶体的操作______ 。
(1)K2FeO4中铁的化合价为
(2)铁屑需事先用Na2CO3溶液洗涤,目的是
(3)K2FeO4处理饮用水的原理是
(4)已知K2FeO4难溶于乙醇,可溶于水,故洗涤K2FeO4晶体时,先使用冷水洗涤,再使用乙醇洗涤,简述用乙醇洗涤K2FeO4晶体的操作
您最近半年使用:0次
名校
解题方法
9 . 废旧电池镍钴锰酸锂三元正极材料的主要成分为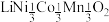 ,通过高温氢化和湿法冶金的方法回收其中的镍、钴、锰、锂,其工艺流程如图所示。
,通过高温氢化和湿法冶金的方法回收其中的镍、钴、锰、锂,其工艺流程如图所示。
②M2+(Co2+或Ni2+)的萃取原理:2HR(有机相)+M2+(水相)⇌MR2(有机相)+2H+(水相)。
回答下列问题:
(1)“高温氢化”时固体产物为Co、Ni、MnO和LiOH,该反应的化学方程式为___________ 。
(2)若“洗液”中c(Li+)=2.0mol•L-1,加入Na2CO3固体后,为使沉淀Li2CO3中Li元素含量不小于Li元素总量的95%,则1.0L“洗液”中至少需要加入Na2CO3的物质的量为___________ [忽略溶液体积变化,Ksp(Li2CO3)=2.2×10-3]。
(3)“沉锰"过程中 对金属沉淀率的影响如图所示。
对金属沉淀率的影响如图所示。 的离子方程式为
的离子方程式为___________ 。
② 时,有少量钴、镍析出,可能的原因是
时,有少量钴、镍析出,可能的原因是___________ 。
(4)“反萃取”的目的是将有机层中 转移到水层。
转移到水层。
①试剂 为
为___________ 。(填试剂名称)
②为使 尽可能多地转移到水层,应采取的实验操作有
尽可能多地转移到水层,应采取的实验操作有___________ 。
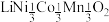 ,通过高温氢化和湿法冶金的方法回收其中的镍、钴、锰、锂,其工艺流程如图所示。
,通过高温氢化和湿法冶金的方法回收其中的镍、钴、锰、锂,其工艺流程如图所示。
②M2+(Co2+或Ni2+)的萃取原理:2HR(有机相)+M2+(水相)⇌MR2(有机相)+2H+(水相)。
回答下列问题:
(1)“高温氢化”时固体产物为Co、Ni、MnO和LiOH,该反应的化学方程式为
(2)若“洗液”中c(Li+)=2.0mol•L-1,加入Na2CO3固体后,为使沉淀Li2CO3中Li元素含量不小于Li元素总量的95%,则1.0L“洗液”中至少需要加入Na2CO3的物质的量为
(3)“沉锰"过程中
 对金属沉淀率的影响如图所示。
对金属沉淀率的影响如图所示。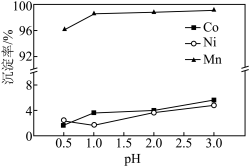
 的离子方程式为
的离子方程式为②
 时,有少量钴、镍析出,可能的原因是
时,有少量钴、镍析出,可能的原因是(4)“反萃取”的目的是将有机层中
 转移到水层。
转移到水层。①试剂
 为
为②为使
 尽可能多地转移到水层,应采取的实验操作有
尽可能多地转移到水层,应采取的实验操作有
您最近半年使用:0次
解题方法
10 .  是有毒的污染性气体,可将其与氧气的混合气体通入
是有毒的污染性气体,可将其与氧气的混合气体通入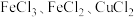 的混合溶液中进行处理,其物质转化如图所示。下列说法正确的是
的混合溶液中进行处理,其物质转化如图所示。下列说法正确的是
 是有毒的污染性气体,可将其与氧气的混合气体通入
是有毒的污染性气体,可将其与氧气的混合气体通入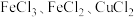 的混合溶液中进行处理,其物质转化如图所示。下列说法正确的是
的混合溶液中进行处理,其物质转化如图所示。下列说法正确的是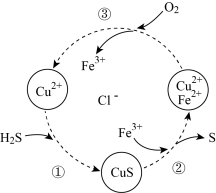
| A.过程①中发生的反应是复分解反应 |
B.过程②中每生成 转移 转移 个电子 个电子 |
C.过程③中每转化 ,需 ,需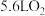 |
D.总反应为 |
您最近半年使用:0次



