2024高三·全国·专题练习
1 . 以Fe(NO3)3作为铁源制备高铁酸钾(K2FeO4),可用于去除水体中的As( )。已知:K2FeO4微溶于水,在酸性或中性溶液中迅速氧化H2O产生O2,在碱性溶液中较稳定,在Fe3+和Fe(OH)3催化作用下发生分解。
)。已知:K2FeO4微溶于水,在酸性或中性溶液中迅速氧化H2O产生O2,在碱性溶液中较稳定,在Fe3+和Fe(OH)3催化作用下发生分解。
(1)制备高铁酸钾。
向KOH和KClO混合溶液中加入Fe(NO3)3,过滤得到K2FeO4固体。
① 制备K2FeO4的化学方程式为___________ 。
② 过滤所得的滤液中加入稀硫酸产生Cl2,原因可能是酸性条件下K2FeO4氧化了Cl-,还可能是___________ 。
(2)测定 K2FeO4的纯度。
准确称取0.528 0 g K2FeO4样品置于锥形瓶中,用KOH溶液溶解,加入过量KCr(OH)4溶液,再加入硫酸酸化配成待测液,用0.3000 mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准液20.00 mL,计算样品中K2FeO4的纯度___________ (写出计算过程)。
测定过程中涉及的离子反应有(未配平):Cr(OH) +FeO
+FeO →Fe(OH)3+CrO
→Fe(OH)3+CrO +OH-;CrO
+OH-;CrO +H+→Cr2O
+H+→Cr2O +H2O;Cr2O
+H2O;Cr2O +Fe2++H+→Cr3++Fe3++H2O。
+Fe2++H+→Cr3++Fe3++H2O。
(3)K2FeO4的应用。
某水样中As元素主要以As( )存在,As(
)存在,As( )可被K2FeO4氧化为As(
)可被K2FeO4氧化为As( ),再通过Fe(
),再通过Fe( )吸附去除。
)吸附去除。
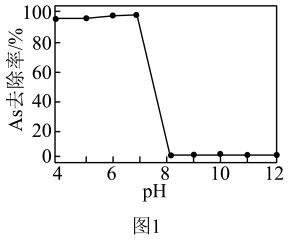
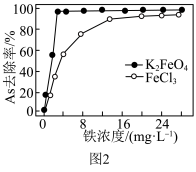
①K2FeO4对水中As元素的去除率随pH变化如图1所示,当pH大于7时,As去除率迅速下降的原因是___________ 。___________ 。 ,纳米铁还原废水中NO
,纳米铁还原废水中NO 的可能反应机理如图3所示。
的可能反应机理如图3所示。 的过程可描述为
的过程可描述为___________ 。
②经检验,污水经处理后,水体中NO 、NO
、NO 浓度很小,但水中总氮浓度下降不明显,原因是
浓度很小,但水中总氮浓度下降不明显,原因是___________ 。
 )。已知:K2FeO4微溶于水,在酸性或中性溶液中迅速氧化H2O产生O2,在碱性溶液中较稳定,在Fe3+和Fe(OH)3催化作用下发生分解。
)。已知:K2FeO4微溶于水,在酸性或中性溶液中迅速氧化H2O产生O2,在碱性溶液中较稳定,在Fe3+和Fe(OH)3催化作用下发生分解。(1)制备高铁酸钾。
向KOH和KClO混合溶液中加入Fe(NO3)3,过滤得到K2FeO4固体。
① 制备K2FeO4的化学方程式为
② 过滤所得的滤液中加入稀硫酸产生Cl2,原因可能是酸性条件下K2FeO4氧化了Cl-,还可能是
(2)测定 K2FeO4的纯度。
准确称取0.528 0 g K2FeO4样品置于锥形瓶中,用KOH溶液溶解,加入过量KCr(OH)4溶液,再加入硫酸酸化配成待测液,用0.3000 mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准液20.00 mL,计算样品中K2FeO4的纯度
测定过程中涉及的离子反应有(未配平):Cr(OH)
 +FeO
+FeO →Fe(OH)3+CrO
→Fe(OH)3+CrO +OH-;CrO
+OH-;CrO +H+→Cr2O
+H+→Cr2O +H2O;Cr2O
+H2O;Cr2O +Fe2++H+→Cr3++Fe3++H2O。
+Fe2++H+→Cr3++Fe3++H2O。(3)K2FeO4的应用。
某水样中As元素主要以As(
 )存在,As(
)存在,As( )可被K2FeO4氧化为As(
)可被K2FeO4氧化为As( ),再通过Fe(
),再通过Fe( )吸附去除。
)吸附去除。①K2FeO4对水中As元素的去除率随pH变化如图1所示,当pH大于7时,As去除率迅速下降的原因是
 ,纳米铁还原废水中NO
,纳米铁还原废水中NO 的可能反应机理如图3所示。
的可能反应机理如图3所示。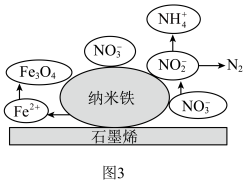
 的过程可描述为
的过程可描述为②经检验,污水经处理后,水体中NO
 、NO
、NO 浓度很小,但水中总氮浓度下降不明显,原因是
浓度很小,但水中总氮浓度下降不明显,原因是
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
2 . 下列物质的应用中与该物质的氧化性或还原性无关的是
| A.过氧化钠用作供氧剂 | B.液氨用作制冷剂 |
| C.葡萄酒中添加二氧化硫 | D.铁粉用于食品保存 |
您最近半年使用:0次
解题方法
3 . 化学与生产生活息息相关,下列生产生活实例与所述化学知识没有关联的是
| 选项 | 生产生活实例 | 化学知识 |
| A | 补铁剂与维生素C同时服用效果更佳 | 维生素C具有还原性 |
| B | 用小苏打作发泡剂烘焙面包 | NaHCO3可与酸反应产生气体 |
| C | 用Na2S标准液检测污水中Cu2+含量 | CuS属于难溶电解质 |
| D | 用聚乙烯塑料制作食品保鲜膜 | 聚乙烯燃烧能生成CO2和H2O |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
4 . 高铁酸钾(K2FeO4)有强氧化性,是一种环保、高效、多功能饮用水处理剂,受热易分解,酸性环境中易变质。制备流程如图所示:
(1)K2FeO4中铁的化合价为______ ,提纯K2FeO4的实验方法是______ 。
(2)铁屑需事先用Na2CO3溶液洗涤,目的是______ 。
(3)K2FeO4处理饮用水的原理是______ 。
(4)已知K2FeO4难溶于乙醇,可溶于水,故洗涤K2FeO4晶体时,先使用冷水洗涤,再使用乙醇洗涤,简述用乙醇洗涤K2FeO4晶体的操作______ 。
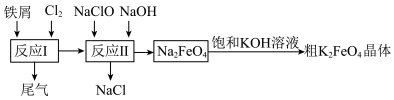
(1)K2FeO4中铁的化合价为
(2)铁屑需事先用Na2CO3溶液洗涤,目的是
(3)K2FeO4处理饮用水的原理是
(4)已知K2FeO4难溶于乙醇,可溶于水,故洗涤K2FeO4晶体时,先使用冷水洗涤,再使用乙醇洗涤,简述用乙醇洗涤K2FeO4晶体的操作
您最近半年使用:0次
2024·湖南益阳·三模
解题方法
5 . 今年春晚长沙分会场的焰火璀璨夺目,燃放烟花时发生反应: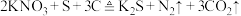 ,同时在火药中会加入
,同时在火药中会加入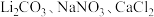 等物质。下列说法正确的是
等物质。下列说法正确的是
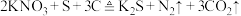 ,同时在火药中会加入
,同时在火药中会加入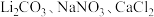 等物质。下列说法正确的是
等物质。下列说法正确的是A.该反应中,氧化产物与还原产物物质的量之比为 |
B.每生成 ,被S氧化的C的物质的量为 ,被S氧化的C的物质的量为 |
C.火药中的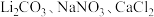 均不参与化学反应 均不参与化学反应 |
| D.燃放烟花对环境没有污染 |
您最近半年使用:0次
2024·广东·一模
6 . 化学与人类生产、生活、科研密切相关,下列有关说法正确的是
A.PM2.5是指空气中直径接近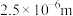 的颗粒物,其分散在空气中形成胶体 的颗粒物,其分散在空气中形成胶体 |
| B.维生素C用作食品中的防腐剂,是因为维生素C有较强的氧化性 |
| C.蒸馏“地沟油”可以获得汽油 |
| D.推广使用可降解塑料,能减少白色污染 |
您最近半年使用:0次
名校
解题方法
7 . 葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过如下实验流程制得:
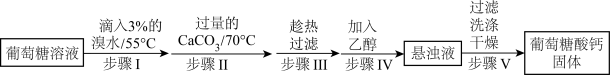
已知:a.反应原理: 。
。
b.相关物质的溶解性如下表:
c.相关物质的酸性:氢溴酸>葡萄糖酸>碳酸。
回答下列问题:
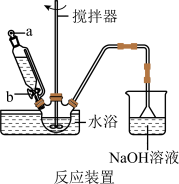
(1)步骤I中溴水氧化葡萄糖时采用了如图所示反应装置,你认为缺少的仪器是___________ ,恒压滴液漏斗使用时需要打开的活塞或玻璃塞是___________ (填“a”“b”或“a和b”)。烧杯中 溶液水浴的作用是
溶液水浴的作用是___________ 。
(2)制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其他试剂,下列物质中最适合的是___________(填序号)。
(3)步骤Ⅱ中加入过量的 ,生成葡萄糖酸钙的化学方程式为
,生成葡萄糖酸钙的化学方程式为___________ 。加入过量的 除了能提高葡萄糖酸的转化率,还有的作用是
除了能提高葡萄糖酸的转化率,还有的作用是___________ 。
(4)洗涤操作中最合适的洗涤剂是___________ (填序号),理由是___________ 。
A.冷水 B.热水 C.乙醇
(5)利用重结晶法可除去葡萄糖酸钙粗品中的杂质,提高产品的质量,选出葡萄糖酸钙重结晶过程中合理的操作并排序:___________ (填序号,操作步骤不可重复使用)。
①蒸发浓缩至溶液表面出现晶膜
②待晶体充分析出后,减压过滤
③将滤液冷却至室温,加入 95%的乙醇溶液并搅拌,促进晶体析出
95%的乙醇溶液并搅拌,促进晶体析出
④趁热减压过滤,除去不溶物
⑤在50℃下用恒温干燥箱烘干,称重
⑥取烧杯加入 蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液

已知:a.反应原理:
 。
。b.相关物质的溶解性如下表:
| 物质的名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 |
| 在水中的溶解性 | 可溶于冷水,易溶于热水 | 可溶 | 极易溶 |
| 在乙醇中的溶解性 | 微溶 | 微溶 | 可溶 |
回答下列问题:
(1)步骤I中溴水氧化葡萄糖时采用了如图所示反应装置,你认为缺少的仪器是
 溶液水浴的作用是
溶液水浴的作用是
(2)制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其他试剂,下列物质中最适合的是___________(填序号)。
A.新制 悬浊液 悬浊液 | B.酸性 溶液 溶液 |
C. /葡萄糖氧化酶 /葡萄糖氧化酶 | D. 溶液 溶液 |
(3)步骤Ⅱ中加入过量的
 ,生成葡萄糖酸钙的化学方程式为
,生成葡萄糖酸钙的化学方程式为 除了能提高葡萄糖酸的转化率,还有的作用是
除了能提高葡萄糖酸的转化率,还有的作用是(4)洗涤操作中最合适的洗涤剂是
A.冷水 B.热水 C.乙醇
(5)利用重结晶法可除去葡萄糖酸钙粗品中的杂质,提高产品的质量,选出葡萄糖酸钙重结晶过程中合理的操作并排序:
①蒸发浓缩至溶液表面出现晶膜
②待晶体充分析出后,减压过滤
③将滤液冷却至室温,加入
 95%的乙醇溶液并搅拌,促进晶体析出
95%的乙醇溶液并搅拌,促进晶体析出④趁热减压过滤,除去不溶物
⑤在50℃下用恒温干燥箱烘干,称重
⑥取烧杯加入
 蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
您最近半年使用:0次
22-23高一上·广西柳州·期末
名校
解题方法
8 . 化学与生产、生活密切相关。下列对应关系错误的是
| A.湿手不可以直接接触电源——电解质溶液能够导电 |
| B.食物腐败——涉及氧化还原反应 |
C.漂白液可作消毒剂——漂白液的有效成分是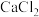 |
| D.下水井盖由生铁铸造——生铁硬度高于纯铁 |
您最近半年使用:0次
解题方法
9 . 化学与生活密切相关。下列各类物质中具有强氧化性的是
| A.净水剂:明矾 | B.消毒剂:过氧乙酸 |
| C.去氧剂:活性铁粉 | D.干燥剂:生石灰 |
您最近半年使用:0次
2024-02-25更新
|
356次组卷
|
3卷引用:2024届陕西省安康市高三下学期一模考试理科综合试题-高中化学
2024届陕西省安康市高三下学期一模考试理科综合试题-高中化学(已下线)专题01 基本概念-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)2024届陕西省西安博爱国际学校高三下学期第一次模拟考试理科综合试卷-高中化学
2024·黑龙江齐齐哈尔·一模
10 .  广泛用于冶金、化工等行业,主要用于冶炼钒铁.以钒矿石为原料制备
广泛用于冶金、化工等行业,主要用于冶炼钒铁.以钒矿石为原料制备 的工艺流程如下:
的工艺流程如下: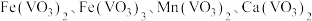 ;“酸浸”后钒以
;“酸浸”后钒以 形式存在,“中和、还原”后钒以
形式存在,“中和、还原”后钒以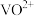 形式存在.
形式存在.
ii.有机溶剂 对四价钒
对四价钒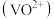 具有高选择性,且萃取
具有高选择性,且萃取 而不萃取
而不萃取 .
.
iii.多钒酸铵微溶于冷水,易溶于热水.
iv.该工艺条件下,溶液中金属离子(浓度均为 )开始沉淀和完全沉淀的
)开始沉淀和完全沉淀的 如下表所示:
如下表所示:
回答下列问题:
(1)“破碎”的目的是_____________________________________ .
(2)“中和、还原”时, 参与反应的离子方程式为
参与反应的离子方程式为_________________________________ .
(3)洗涤多钒酸铵时要用冰水洗涤,目的是______________________________ . 的空间结构为
的空间结构为_______________ 形.
(4)“氧化”时,每消耗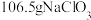 (本身被还原为
(本身被还原为 ),可得到
),可得到
_______________  .
.
(5)流程中可循环使用的物质有__________________________________ .
(6)“萃取”分离后,所得“水相”中含有丰富的金属资源,经三道工序可回收 溶液.请根据题给信息,参照上述工艺流程,将下列工艺流程补充完整(可供选用的试剂:
溶液.请根据题给信息,参照上述工艺流程,将下列工艺流程补充完整(可供选用的试剂: 溶液、
溶液、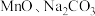 溶液、
溶液、 溶液).
溶液).
 广泛用于冶金、化工等行业,主要用于冶炼钒铁.以钒矿石为原料制备
广泛用于冶金、化工等行业,主要用于冶炼钒铁.以钒矿石为原料制备 的工艺流程如下:
的工艺流程如下: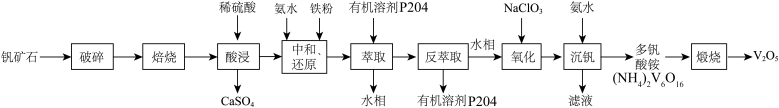
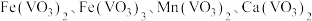 ;“酸浸”后钒以
;“酸浸”后钒以 形式存在,“中和、还原”后钒以
形式存在,“中和、还原”后钒以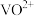 形式存在.
形式存在.ii.有机溶剂
 对四价钒
对四价钒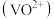 具有高选择性,且萃取
具有高选择性,且萃取 而不萃取
而不萃取 .
.iii.多钒酸铵微溶于冷水,易溶于热水.
iv.该工艺条件下,溶液中金属离子(浓度均为
 )开始沉淀和完全沉淀的
)开始沉淀和完全沉淀的 如下表所示:
如下表所示:金属离子 |
|
|
|
|
开始沉淀 | 1.9 | 7.0 | 11.9 | 8.1 |
完全沉淀 | 3.2 | 9.0 | 13.9 | 10.1 |
(1)“破碎”的目的是
(2)“中和、还原”时,
 参与反应的离子方程式为
参与反应的离子方程式为(3)洗涤多钒酸铵时要用冰水洗涤,目的是
 的空间结构为
的空间结构为(4)“氧化”时,每消耗
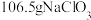 (本身被还原为
(本身被还原为 ),可得到
),可得到
 .
.(5)流程中可循环使用的物质有
(6)“萃取”分离后,所得“水相”中含有丰富的金属资源,经三道工序可回收
 溶液.请根据题给信息,参照上述工艺流程,将下列工艺流程补充完整(可供选用的试剂:
溶液.请根据题给信息,参照上述工艺流程,将下列工艺流程补充完整(可供选用的试剂: 溶液、
溶液、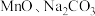 溶液、
溶液、 溶液).
溶液).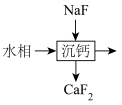
您最近半年使用:0次





